DNA-Reparatur mit Fehlertoleranz
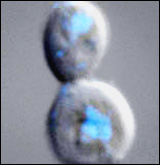
Fluoreszenzmikroskopische Aufnahme einer Hefezelle bei der Zellteilung. Die akkurate Weitergabe des genetischen Materials, hier blau angefärbt, von der Mutter- zur Tochterzelle ist für die Stabilität der Erbinformation von entscheidender Bedeutung. <br>Foto: Max-Planck-Institut für terrestrische Mikrobiologie
Marburger Max-Planck-Forscher haben entdeckt, wie Zellen nicht nur die Effizienz, sondern auch die Genauigkeit von DNA-Reparaturen steuern können
Für die Verdopplung unseres Erbgutes sind spezielle Enzyme verantwortlich, die so genannten DNA-Polymerasen. Ihre Kopiergenauigkeit trägt entscheidend zur akkuraten Weitergabe der genetischen Information einer Zelle bei. Beschädigungen der DNA blockieren jedoch diese Enzyme und würden die Zellteilung verhindern, wenn die Zelle nicht über eine Reihe anderer DNA-Polymerasen verfügen würde, die auf die Überwindung derartiger Blockaden spezialisiert sind. Diese „Notfall-Spezialisten“ sind jedoch wegen ihrer Toleranz gegenüber beschädigter DNA weniger genau und können dadurch unerwünschte, im schlimmsten Falle krebsauslösende Mutationen verursachen. In der neuesten Ausgabe der Fachzeitschrift Nature (Nature, 11. September 2003) berichten jetzt Helle Ulrich und Philipp Stelter vom Max-Planck-Institut für terrestrische Mikrobiologie in Marburg von der Entdeckung eines Signalweges, der die Aktivität der Notfall-Polymerasen reguliert und so die Genauigkeit der Erbgutverdopplung mitbestimmt.
Die DNA, der Träger unserer Erbinformation, ist ein reaktives Molekül, das durch diverse Umwelteinflüsse wie UV-Licht oder Chemikalien, aber auch ohne äußere Einwirkungen ständig in seiner Stabilität gefährdet ist. Um sich gegen den drohenden Verlust von Erbinformation zu wehren, haben die Zellen ausgefeilte Mechanismen zur Reparatur ihres genetischen Materials entwickelt, die in allen Organismen sehr ähnlich ablaufen. Die Wissenschaftler in der Arbeitsgruppe von Dr. Helle Ulrich am Marburger Max-Planck-Institut für terrestrische Mikrobiologie forschen dazu an der Bäckerhefe, einem einzelligen Pilz, um herauszufinden, wie sich Zellen vor den Folgen von DNA-Schädigungen schützen.
Da die DNA ein doppelsträngiges Molekül ist, trägt sie sämtliche Information in zweifacher Form. Dies ermöglicht es, Schäden in einem der beiden Stränge fehlerfrei mit Hilfe der Information des intakten gegenüberliegenden Stranges zu reparieren. Kritisch wird die Situation für eine Zelle während der Replikation, also der Verdopplung der DNA dann, wenn sich die beiden Stränge voneinander trennen. Denn DNA-Polymerasen, also jene Enzyme, die für die Replikation verantwortlich sind, können geschädigte Abschnitte nicht überwinden, da hier die genetische Information für sie nicht ablesbar ist. Bleibt jedoch die DNA-Replikation stecken, kann sich die Zelle selbst nicht mehr vermehren.
In diesem Fall steht der Zelle allerdings ein Notprogramm zur Verfügung. Dieses erlaubt ihr, trotz des DNA-Schadens die Verdopplung des Genoms zu vollenden. Dazu übernehmen alternative DNA-Polymerasen zeitweilig die Replikation, die weniger „penibel“ sind und es hinsichtlich ihrer Kopiervorlage nicht so genau nehmen. Diese „Notfallkopierer“ arbeiten allerdings auf Kosten der Genauigkeit, denn ihre Toleranz gegenüber DNA-Schäden erkaufen sich diese Enzyme durch eine wesentlich höhere Fehlerrate beim Kopieren. So entstehen durch ihre Aktivität Mutationen im Genom, die in höheren Organismen eine unkontrollierte Vermehrung der Zelle auslösen und damit einen wesentlichen Beitrag zur Krebsentstehung leisten können.
Die Notfall-Polymerasen sind also ein zweischneidiges Schwert: Auf der einen Seite sorgen sie dafür, dass eine Zelle sich selbst unter ungünstigen Bedingungen noch erfolgreich vermehren kann. Auf der anderen Seite nimmt der Organismus damit unerwünschte Mutationen in Kauf, die in der Zukunft Gesundheit und Funktionstüchtigkeit seiner selbst sowie seiner Nachkommen beeinträchtigen könnten. Deshalb ist es nicht überraschend, dass eine Zelle den Einsatz dieser Spezialisten sehr genau überwacht und sie nicht unkontrolliert agieren lässt. Philipp Stelter und Helle Ulrich haben nun einen Signalweg entdeckt, der bei Bedarf die schadenstoleranten Polymerasen aktiviert und so die Replikation geschädigter DNA ermöglicht.
Erste Hinweise auf einen verwandten Regulationsmechanismus hatten im Jahr 2002 Zellbiologen am Max-Planck-Institut für Biochemie in Martinsried gefunden (Nature, Band 419, 12. September 2002 und Presseinformation „Schutzschalter gegen Erbschäden“). Die Forscher hatten damals gezeigt, dass ein Protein namens PCNA, das in der Zelle als Helfer der DNA-Polymerasen fungiert, durch Verknüpfung mit einem weiteren Protein, dem Ubiquitin, verändert wird, wenn die Zellen DNA-schädigenden Agenzien ausgesetzt sind. Diese Veränderung erfolgt durch die schrittweise Ankopplung von mehreren Ubiquitin-Molekülen zu einer Kette und fördert die Reparatur von DNA-Schäden, ohne die Notfall-Polymerasen in Anspruch zu nehmen.
Die Marburger Forscher fanden jetzt überraschend, dass die Notfall-Polymerasen jedoch bei der Verknüpfung von PCNA mit nur einem einzigen Ubiquitin-Molekül zur Mitwirkung an der Replikation herangezogen werden. Wenn die Wissenschaftler diese Art der Verknüpfung durch gentechnische Veränderung verhinderten, konnten DNA-Schäden in den entsprechenden Zellen ihre mutationsauslösende Wirkung nicht mehr entfalten. Sogar die Entstehung von spontanen Mutationen ohne äußere Einwirkung von erbgutschädigenden Faktoren ist vom Zustand des PCNA-Proteins abhängig. Wie die beiden Wissenschaftler berichten, konnte eine der Notfall-Polymerasen nicht nur durch die Verknüpfung von PCNA mit Ubiquitin, sondern auch durch Anhängen eines Ubiquitin-ähnlichen Proteins namens SUMO aktiviert werden. Diese Form der Verknüpfung tritt tatsächlich regelmäßig während der Verdopplung der DNA auf und trägt damit zu spontanen Erbgutveränderungen bei.
Diese Ergebnisse, die am Marburger Max-Planck-Institut mit Hilfe eines einfachen Modellorganismus und überwiegend mit Methoden der klassischen Genetik erarbeitet wurden, erlauben Rückschlüsse auf jene molekularen Vorgänge, die die stabile Weitergabe genetischer Information von Zellgeneration zu Zellgeneration beeinflussen. Offensichtlich helfen die vielfältigen Modifikationen am PCNA-Protein der Zelle, sowohl die Effizienz als auch die Genauigkeit der Replikation von unversehrter oder beschädigter DNA zu steuern und damit differenziert auf verschiedenste Umweltbedingungen zu reagieren.
Die Marburger Max-Planck-Wissenschaftler hoffen, mit ihren Forschungsergebnissen einen Weg gefunden zu haben, der in Zellen die Entstehung unerwünschter Mutationen verhindert, ohne dass dadurch wichtige fehlerfreie Reparaturvorgänge beeinträchtigt werden. Das könnte ein wichtiger neuer Schritt zur Bekämpfung der Krebsentstehung sein.
Weitere Informationen erhalten Sie von:
Dr. Helle Ulrich
Max-Planck-Institut für terrestrische Mikrobiologie, Marburg
Tel.: 06421 178 – 601, Fax: – 609
E-Mail: hulrich@staff.uni-marburg.de
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Wolken bedecken die Nachtseite des heißen Exoplaneten WASP-43b
Ein Forschungsteam, darunter Forschende des MPIA, hat mit Hilfe des Weltraumteleskops James Webb eine Temperaturkarte des heißen Gasriesen-Exoplaneten WASP-43b erstellt. Der nahe gelegene Mutterstern beleuchtet ständig eine Hälfte des Planeten…
Neuer Regulator des Essverhaltens identifiziert
Möglicher Ansatz zur Behandlung von Übergewicht… Die rapide ansteigende Zahl von Personen mit Übergewicht oder Adipositas stellt weltweit ein gravierendes medizinisches Problem dar. Neben dem sich verändernden Lebensstil der Menschen…

Maschinelles Lernen optimiert Experimente mit dem Hochleistungslaser
Ein Team von internationalen Wissenschaftlerinnen und Wissenschaftlern des Lawrence Livermore National Laboratory (LLNL), des Fraunhofer-Instituts für Lasertechnik ILT und der Extreme Light Infrastructure (ELI) hat gemeinsam ein Experiment zur Optimierung…