SARS-CoV-2-Studie zum Infektionsmechanismus in den Lungenbläschen
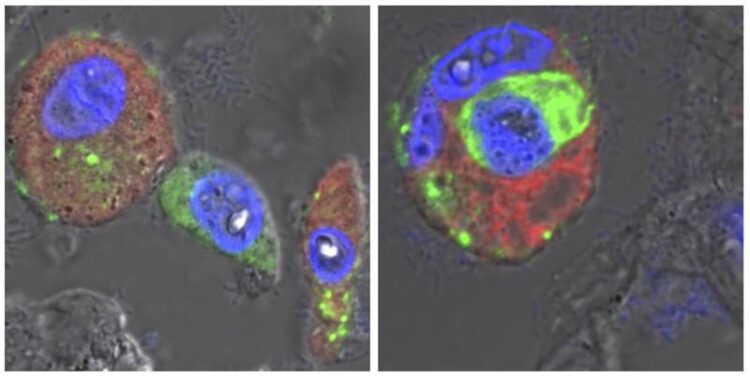
Mikroskopische Aufnahmen von Lungengewebe eines an COVID-19 Verstorbenen: Die Alveolarmakrophagen (rot, Zellkerne in blau) haben SARS-CoV-2-Virusmaterial (grün) aufgenommen (links). Die gestorbenen Zellen werden von den Makrophagen aufgenommen (rechts).
Bild: Andreas Hocke / Charité
Charité-Forschende simulieren Coronainfektion an menschlichen Lungen und Organoiden.
Einer Berliner Forschungsgruppe unter Leitung der Charité – Universitätsmedizin Berlin ist es gelungen, die Infektion mit SARS-CoV-2 an menschlichen Lungen zu simulieren und somit zentrale Erkenntnisse zum Infektionsmechanismus zu generieren. Anhand von im Labor kultivierten, lebenden Lungenproben zeigt sie, dass der COVID-19-Erreger in nur sehr begrenztem Maß in der Lage ist, die Zellen der menschlichen Lungenbläschen direkt zu infizieren. Hingegen wird der überwiegende Teil der in die Lunge gelangten Viren von Makrophagen – Zellen der angeborenen Immunabwehr – direkt aufgenommen und löst in diesen eine gezielte Immunaktivierung aus. Die Ergebnisse sind jetzt im Fachmagazin European Respiratory Journal* erschienen.
Nach wie vor forschen Wissenschaftler:innen weltweit daran, den Mechanismus hinter einer COVID-19-Infektion und der damit manchmal einhergehenden Lungenentzündung und Lungenschädigung besser zu verstehen. Forschende der Charité, des Berlin Institute of Health in der Charité (BIH), des Max-Delbrück-Centrums für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC), des Robert Koch-Instituts und der Freien Universität Berlin haben jetzt die Vermehrung und Immunaktivierung von SARS-CoV-2-Viren in menschlichen Lungen analysiert. Spezifisch haben sie dafür die Zellen der menschlichen Lungenbläschen, auch Alveolen genannt, sowie die Alveolarmakrophagen in den Blick genommen. Diese Fresszellen unseres angeborenen Immunsystems vernichten fremde Partikel, darunter auch Infektionserreger wie Viren und Bakterien, und sorgen so für die Reinigung der Lunge.
Unter der Leitung von Prof. Dr. Andreas Hocke von der Medizinischen Klinik mit Schwerpunkt Infektiologie und Pneumologie der Charité hat das Forschungsteam herausgefunden, dass SARS-CoV-2 nur sehr wenige Epithelzellen, die die Oberfläche der Lungenbläschen auskleiden, infiziert und damit auch nur einen sehr geringen, direkten Gewebeschaden verursacht. Das stellt einen entscheidenden Unterschied etwa zu MERS-Coronaviren oder Influenzaviren dar. Gleichzeitig konnten die Wissenschaftler:innen belegen, dass der für SARS-CoV-2 notwendige ACE2-Rezeptor, der als Einstiegspforte für die Viren dient, in nur sehr wenigen Alveolarepithelzellen nachweisbar ist. Das ergaben umfangreiche Analysen mittels spektraler Mikroskopie.
„Wir konnten die direkte Abhängigkeit von SARS-CoV-2 zu seinem Rezeptor in menschlichen Lungen sowie in Lungenorganoiden – das sind Modelle menschlicher Lungenbläschen, die wir aus Stammzellen des Lungengewebes gewonnen haben – zeigen und damit andere, alternative Rezeptoren ausschließen“, erklärt die Erstautorin der Studie Dr. Katja Hönzke von der Medizinischen Klinik mit Schwerpunkt Infektiologie und Pneumologie. Gelangen große Virusmengen aus dem oberen Atemweg in die Lungenbläschen, so vermehren sich diese demnach nicht in hohem Maß in den ansässigen Epithelzellen der Lunge, wie das bei anderen schweren Virusinfektionen oft der Fall ist, sondern werden direkt von den Fresszellen aufgenommen. „Wir haben mit detaillierten bioinformatischen Analysen sowie anhand von Autopsiegewebe von an COVID-19 verstorbenen Personen gesehen, dass sich die Fresszellen durch die Aufnahme der Coronaviren verändern“, sagt der zweite Erstautor der Studie Dr. Benedikt Obermayer-Wasserscheid vom BIH. Diese Wandlungen lösen wiederum unterschiedliche Reaktionen im Rahmen der Lungenentzündung aus: Die Fresszellen geben Entzündungsbotenstoffe ab und können zum Teil sehr starke Entzündungskaskaden anstoßen. Ebenso beobachteten die Forschenden, dass sich das Virus in den Immunzellen nicht vermehrt.
Prof. Hocke ordnet die Ergebnisse ein: „Unsere Studie deutet darauf hin, dass schwere Lungenschäden bei COVID-19 eher auf eine durch Makrophagen ausgelöste Immunaktivierung als auf eine direkte Zerstörung der Lungenbläschen durch das Virus zurückzuführen sind. Damit trägt sie wesentlich zum Verständnis der Entstehung von COVID-19 in der Frühphase einer möglichen Lungenentzündung bei und zeigt, warum SARS-CoV-2, im Gegensatz zu MERS-Coronaviren, in der Mehrzahl der Fälle einen eher moderaten Verlauf aufweist.“ Es lässt sich also davon ausgehen, dass die lokalen Immunmechanismen im Atemgewebe die SARS-CoV-2-Viren in den allermeisten Fällen sehr effizient beseitigen und die Entzündungsreaktion begrenzen. Geschieht das nicht, was möglicherweise durch individuelle Risikofaktoren beeinflusst wird, können in seltenen Fällen schwere und tödliche Verläufe entstehen. Prof. Hocke führt weiterhin aus: „Unsere eingesetzten Lungenmodelle zeigen in hervorragender Weise, wie Alternativen zu Tiermodellen, die auf menschlichen Zellen basieren, insbesondere bei der Erforschung zoonotischer Erkrankungen eingesetzt werden können. Das ist uns in enger Zusammenarbeit mit Charité 3R, unserer Einrichtung zur Entwicklung von Alternativen zu Tierversuchen, gelungen.“
Im Zentrum nachfolgender Arbeiten sollen nun Untersuchungen an patientenindividuellen Organoidmodellen folgen, um so den Einfluss von allgemeinen Risikofaktoren wie Alter, Geschlecht, Begleiterkrankungen und anderen Medikationen auf die Aktivierung der Entzündungsantwort vertiefend zu analysieren. Mit diesen Kenntnissen ließen sich dann mögliche Therapieansätze, die auf das Immunsystem abzielen, identifizieren.
Über die Studie
Gefördert wurde die Arbeit durch die Deutsche Forschungsgemeinschaft (DFG) im Sonderforschungsbereich „Angeborene Immunität der Lunge“ (SFB-TR84), der Einstein Stiftung Berlin (Einstein-Zentrum 3R) sowie im Rahmen des Verbundprojektes „Organspezifische Stratifikation bei COVID-19“ (Organo-Strat) durch das Bundesministerium für Bildung und Forschung (BMBF). Das Verbundprojekt ist Teil des Netzwerks Universitätsmedizin (NUM), das von der Charité initiiert wurde und koordiniert wird. Das NUM vereint die Kräfte der 36 Universitätsklinika in Deutschland.
*Hönzke K, Obermayer B, Mache C, et al. Human lungs show limited permissiveness for SARS-CoV-2 due to scarce ACE2 levels but virus-induced expansion of inflammatory macrophages. European Respiratory Journal (2022). doi: 10.1183/13993003.02725-2021
Wissenschaftliche Ansprechpartner:
Prof. Dr. Andreas Hocke
Medizinische Klinik mit Schwerpunkt Infektiologie und Pneumologie
Charité – Universitätsmedizin Berlin
t: +49 30 450 553 477
E-Mail: andreas.hocke@charite.de
Originalpublikation:
doi: 10.1183/13993003.02725-2021
Weitere Informationen:
https://erj.ersjournals.com/content/erj/early/2022/05/26/13993003.02725-2021.ful…
https://infektiologie-pneumologie.charite.de/
https://charite3r.charite.de/
https://www.netzwerk-universitaetsmedizin.de/
Media Contact
Alle Nachrichten aus der Kategorie: Studien Analysen
Hier bietet Ihnen der innovations report interessante Studien und Analysen u. a. aus den Bereichen Wirtschaft und Finanzen, Medizin und Pharma, Ökologie und Umwelt, Energie, Kommunikation und Medien, Verkehr, Arbeit, Familie und Freizeit.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















