Neuer Therapieansatz für chronisch-entzündliche Darmerkrankungen?
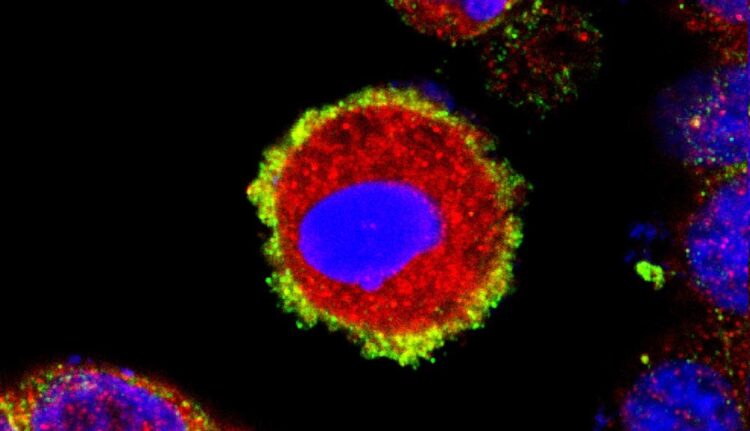
Mikroskopische Aufnahme einer kultivierten Darmepithelzelle deren Zelltodprogramm aktiviert ist (rot). Es bilden sich Poren in der Zellmembran (grün) wodurch die Zelle stirbt. Der Zellkern ist in blau dargestellt. (Bild: Jay Patankar/Uni-Klinikum Erlangen)
FAU-Forschungsteam: Botenstoff schützt Zellen im Darm.
Warum Menschen an chronisch-entzündlichen Darmerkrankungen (CED) wie der Colitis ulcerosa erkranken, ist nur bruchstückhaft verstanden. Man weiß jedoch, dass die Bakterien der Darmflora und eine Fehlsteuerung des Immunsystems eine wichtige Rolle spielen. Bei CED-Erkrankten sterben vermehrt Zellen in der Darmwand, die sogenannten Epithelzellen, ab. Daraufhin gelangen Bakterien aus dem Inneren des Darms in die geschädigte Darmwand, die dort Entzündungen hervorrufen. Diese Entzündungen wiederum führen zu einem weiteren Absterben von Epithelzellen. Die Darmbarriere, die Barriere zwischen dem Darminhalt und der Darmwand, wird durchlässiger. Mit zunehmendem Zelltod schreitet auch die Krankheit voran, denn in der geschädigten Darmwand siedeln sich weitere Bakterien an – ein Teufelskreis.
Ein Forschungsteam um Prof. Dr. Christoph Becker von der Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU) hat nun einen Mechanismus gefunden, der den Zelltod verhindern, den Teufelskreis unterbrechen und damit möglicherweise als Therapie bei entzündlichen Darmerkrankungen eingesetzt werden könnte. Die Ergebnisse der Wissenschaftler werden in der renommierten Fachzeitschrift Nature Cell Biology veröffentlicht.*
In Mäusen und an Geweben von Colitis-ulcerosa-Erkrankten zeigte sich, dass ein Botenstoff namens Prostaglandin E2 die Epithelzellen vor einer besonderen Form des Zelltods, der Nekroptose, bewahren kann. Prostaglandine sind hormonähnliche Botenstoffe und zeigen vielfältige Wirkungen im Organismus. Prostaglandine wie das Prostaglandin E2 werden im Körper bei Entzündungen freigesetzt. Wie sie Entzündungsprozesse regulieren, ist jedoch noch nicht vollständig verstanden.
In den vergangenen Jahren hatten die Forscherinnen und Forscher bereits zeigen können, dass die Fehlregulation der Nekroptose zu Zelltod und somit zu Löchern in der Darmbarriere führt. Prostaglandin E2 verhindert dies, indem es an auf den Epithelzellen vorhandene Rezeptoren mit der Bezeichnung EP4 bindet. Je mehr dieser Rezeptoren aktiviert werden, so das FAU-Team von der Medizinischen Klinik 1 – Gastroenterologie, Pneumologie und Endokrinologie – am Universitätsklinikum Erlangen, umso weniger Zellen sterben ab. Patientinnen und Patienten mit viel EP4 auf der Zelloberfläche zeigen einen milderen Krankheitsverlauf als Patienten mit wenig EP4.
Die Aktivierung der Rezeptoren durch Prostaglandin E2 wirkt somit dem Fortschreiten der Darmentzündung entgegen. Gemeinsam mit Kolleginnen und Kollegen in Kanada testeten sie ein künstlich hergestelltes Molekül, das wie Prostaglandin E2 den EP4-Rezeptor aktivieren kann. Tatsächlich konnte durch eine Behandlung mit diesem Molekül der exzessive Zelltod in der Darmbarriere verhindert werden und somit das Eindringen von Bakterien blockiert werden. Diese Erkenntnisse bieten einen möglichen neuen Behandlungsansatz für Colitis ulcerosa und andere chronisch-entzündliche Darmerkrankungen.
* https://doi.org/10.1038/s41556-021-00708-8
Ansprechpartner für Medien:
Prof. Dr. Christoph Becker
Tel.: 09131/85-35886
christoph.becker@uk-erlangen.de
Wissenschaftliche Ansprechpartner:
Prof. Dr. Christoph Becker
Tel.: 09131/85-35886
christoph.becker@uk-erlangen.de
Originalpublikation:
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Wie die Galvanotechnik durch Digitalisierung effizient wird
SurfaceTechnology GERMANY… Digitalisierung und Hartverchromung aus Chrom(III)-Elektrolyten: Das sind die beiden großen Themen, mit denen sich Forscherinnen und Forscher von der Abteilung Galvanotechnik am Fraunhofer IPA derzeit beschäftigen. Ihre Erkenntnisse…

Ersatz für Tierversuche – jetzt ganz ohne Tierleid
Erstes Gewebe-Modell der Leber völlig ohne Materialien tierischer Herkunft hergestellt. Wissenschaftler*innen der TU Berlin haben mit Hilfe von 3D-Biodruck erstmals ein Modell der Leber aus menschlichen Zellen hergestellt, ohne dabei…
Neue Wege zur mentalen Gesundheit
Magnetspule am Kopf sorgt für antidepressive Effekte… In der Klinik und Poliklinik für Psychiatrie und Psychotherapie am Universitätsklinikum Bonn (UKB) wird derzeit eine Studie zur Erforschung der antidepressiven Wirkung einer…





















Guten Abend,
der Ansatz ist sicherlich lobenwert, nur sollte man hier die Ursachen des Leaky Gut im Auge behalten. Diese sind nun wirklich kein Medikamenten-Mangel sondern i.d.R. auch folge dergleichen.
Weiterhin sind sicherlich toxische-metale, Mikroplastik, Antibiotika-Rückstände, Fehl-Magel-Ernährung mit der folge einer Bakterielen Dysbalance – Small intestinal bacterial overgrowth (SIBO) mindestens mit verantwortlich.
Auch die „Banalen“ Unverträglichkeiten = Gluten, Milcheiweiß/Lactose, Fruktoseintoleranz, sowie eine zu hohe, nicht ausreichend vorverdaute Eiweißmenge führen zu den Folgen des Sickerdarms.
In diesem Sinne; Der Tod sitzt im Darm