Hammer-Protein bei der Arbeit zugeschaut
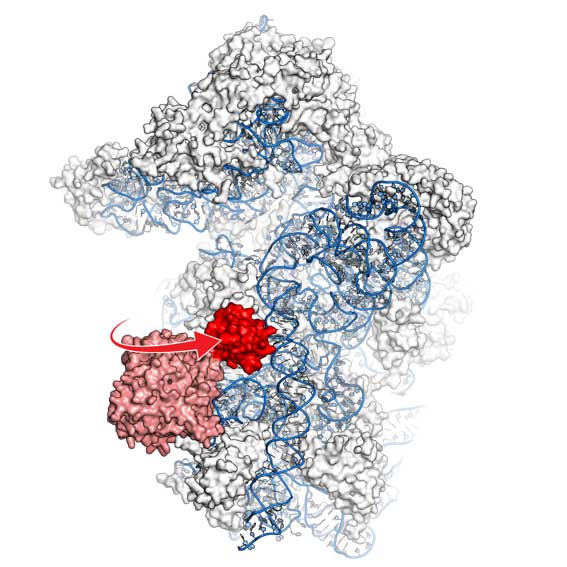
Struktur des Ribosoms nach der Spaltung mit gebundenem Motorprotein ABCE1 (hellrot). Der rotierende Hammerkopf ist rot gefärbt. Copyright: Arbeitsgruppe Tampé, Goethe-Universität
Die Gruppen von Prof. Robert Tampé vom Institut für Biochemie der Goethe-Universität und von Prof. Roland Beckmann am Genzentrum in München klärten die Struktur von ABCE1 an der kleinen ribosomalen Untereinheit mithilfe der Kryo-Elektronenmikroskopie auf.
Der strukturell hochaufgelöste Komplex ist sozusagen der Punkt am Satzende der Übersetzung und wird als Post-Spaltungskomplex bezeichnet. Zu ihrer Überraschung erkannten die Forscher, dass ein bestimmter Bereich von ABCE1 (die Eisen-Schwefel-Cluster Domäne) wie ein Hammerkopf geformt ist, der sich bei seiner Arbeit um 180-Grad dreht. Hierbei werden die beiden ribosomalen Einheiten auseinandergetrieben und deren Re-Assoziation verhindert. Dieser Prozess wird durch ATP, den Energieträger der Zelle, angetrieben.
Die in der aktuellen Ausgabe der Fachzeitschrift „Nature Structural and Molecular Biology“ publizierte Struktur zeigt den molekularen Motor ABCE1 in einer asymmetrischen Konformation. Dies erlaubt Rückschlüsse auf den fundamentalen Mechanismus der Protein-Biosynthese. Beim Menschen sind viele medizinisch relevante Prozesse, die Moleküle durch die Zellmembran transportieren, mit diesen asymmetrisch aufgebauten Motoren gekoppelt.
Weiterhin fanden die Forscher heraus, wie ABCE1 eine neue Runde der Translation einleitet. Lange war bekannt, dass ABCE1 mit so genannten Initiationsfaktoren wechselwirkt, welche die Protein-Biosynthese in Gang setzen. Jetzt konnten sie erstmals die Co-Assoziation mit spezifischen Komponenten des Initiationskomplexes aufzeigen.
Daraus ergibt sich für die weitere Forschung die Frage, wie ABCE1 mit der Rekrutierung von Initiationsfaktoren gekoppelt ist. Das erscheint durchaus wahrscheinlich, denn die Forscher haben mithilfe genetischer Ansätze herausgefunden: Wenn sie die Wechselwirkung von ABCE1 mit dem Ribosom nur geringfügig verändern, kann dies zu drastischen physiologischen Effekten führen.
„Gemeinsam konnten wir ein fehlendes Bindeglied in der Protein-Biosynthese, von einem Zyklus zum nächsten aufklären. Die Arbeit schließt den essentiellen Kreislauf des Lebens für die Homöostase, Differenzierung und Entwicklung von Zellen und Organismen“, fasst Robert Tampé die Bedeutung der Arbeit zusammen.
Publikation:
André Heuer, Milan Gerovac, Christian Schmidt, Simon Trowitzsch, Anne Preis, Peter Kötter, Otto Berninghausen, Thomas Becker, Roland Beckmann & Robert Tampé (2017): Structure of the 40S-ABCE1 post-splitting complex in ribosome recycling and translation initiation. Nature Structure and Molecular Biology, doi:10.1038/nsmb.3396
Information: Prof. Robert Tampé, Institut für Biochemie, Fachbereich 14, Campus Riedberg, Telefon: (069) 798-29475, tampe@em.uni-frankfurt.de
Informationen: Prof. Robert Tampé, Institut für Biochemie, Fachbereich , Goethe Universität Frankfurt, Telefon: (069) 798-29475, tampe@em.uni-frankfurt.de
Aktuelle Nachrichten aus Wissenschaft, Lehre und Gesellschaft in GOETHE-UNI online:
www.aktuelles.uni-frankfurt.de
Die Goethe-Universität ist eine forschungsstarke Hochschule in der europäischen Finanzmetropole Frankfurt. 1914 mit privaten Mitteln überwiegend jüdischer Stifter gegründet, hat sie seitdem Pionierleistungen erbracht auf den Feldern der Sozial-, Gesellschafts- und Wirtschaftswissenschaften, Medizin, Quantenphysik, Hirnforschung und Arbeitsrecht. Am 1. Januar 2008 gewann sie mit der Rückkehr zu ihren historischen Wurzeln als Stiftungsuniversität ein hohes Maß an Selbstverantwortung. Heute ist sie eine der zehn drittmittelstärksten und drei größten Universitäten Deutschlands mit drei Exzellenzclustern in Medizin, Lebenswissenschaften sowie Geistes- und Sozialwissenschaften. Zusammen mit der Technischen Universität Darmstadt und der Universität Mainz ist sie Partner der länderübergreifenden strategischen Universitätsallianz Rhein-Main. Internet: www.uni-frankfurt.de
Herausgeberin: Die Präsidentin der Goethe-Universität Redaktion: Dr. Anne Hardy, Referentin für Wissenschaftskommunikation, Abteilung PR & Kommunikation, Theodor-W.-Adorno-Platz 1, 60323 Frankfurt am Main, Tel: (069) 798-13035, Fax: (069) 798-763 12531, kaltenborn@pvw.uni-frankfurt.de
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Robotisch assistiertes Laserverfahren soll OP-Risiken minimieren
Eine Spinalkanalstenose – eine knöcherne Verengung des Wirbelkanals – kann für Betroffene zur Qual werden. Drückt sie auf das Rückenmark, drohen ihnen chronische Schmerzen und Lähmungserscheinungen. Häufig hilft dann nur…

Verbesserte Materialien für die Verbindungen von Mikrochips
Leistungsfähiger, stromsparender, komplexer – Hersteller von modernen Microchips sehen sich stetig neuen Herausforderungen gegenüber, auch in Bezug auf die dort notwendigen elektrischen Verbindungen. Das Fraunhofer IPMS und BASF widmen sich…

Inspiriert von der Natur: Biophysiker aus dem Projekt InCamS@BI entwickelt neuartige Mikroplastikfilter im Labor
Heutzutage ist es überall zu finden: Mikroplastik. Es wird insbesondere durch die Luft und durchs Wasser in die entlegensten Winkel der Erde transportiert. Eine der großen Fragen lautet: Wie können…



