Carbabenem-3-Carbonsäure-Derivate als Antibiotika und

Das Schutzrechtsportfolio beinhaltet eine Reihe von Wirkstoffkandidaten, welche einen immer relevanter werdenden Bedarf an Antibiotika gegen resistente Erregerstämme adressieren. Die Schutzrechte sind sehr breit internationalisiert und bis auf eine Ausnahme auch bereits erteilt.
Die Testung der Wirkstoffkandidaten ist im prä-klinischen Bereich erfolgreich abgeschlossen worden. Vergleichbare Transaktionen von Phase-l-validierten Wirkstoffen zeigt einerseits die Notwendigkeit auf, diese geschützten Wirkstoffe zum erfolgreichen Abschluss der klinischen Phase I weiterzuentwickeln. Anderseits zeigen vergleichbare Transaktionen am Markt, dass für derartig validierte Wirkstoffkandidaten bis zu siebenstellige Beträge gezahlt werden.
2. Technology
Im Jahr 2005 infizierten sich rund drei Millionen Europäer mit Keimen, die gegen bekannte Antibiotika resistent sind – 50.000 von ihnen starben daran. In den USA sind etwa 70% der in Krankenhäusern erworbenen infektiösen Keime resistent gegen mindestens ein Antibiotikum. Schätzungen des Centers for Disease Control and Prevention gehen für die USA von zwei Millionen im Krankenhaus erworbenen Infektionen für das Jahr 2004 aus, mit etwa 90.000 Todesfällen. Oft sind Patienten dabei mit Bakterienstämmen infiziert, die gegen mehrere Antibiotika resistent sind (Multiresistenz). Doch neben dieser Resistenz werden verstärkt aktive „Verteidigungsmechanismen“ der Erreger beobachtet. Beta-Laktamasen z.B. sind Enzyme, die von zahlreichen Bakterien wie S.aureus oder E.coli gebildet werden. Diese haben die Eigenschaft, weit verbreitete Beta-Laktam-Antibiotika zu inaktivieren. Zu diesen zählen die weltweit am häufigsten genutzten Antibiotika wie Peniciline oder Cephalosporine.
Um diese bedrohliche vollständige Wirkungslosigkeit der Antibiotika zu verhindern, wird seit einiger Zeit eine Kombination aus Antibiotika und Beta-Laktamasen-Inhibitoren wie Clavulansäure als Therapie gegeben. Doch auch diese Therapieoption sieht sich zunehmenden Resistenzen gegenüber. Darüber hinaus kommt es relativ häufig zu scheren Nebenwirkungen im Verdauungstrakt, was derzeit eine patientenfreundliche orale Gabe nicht zulässt. Aus diesen Umständen ergibt sich die Notwendigkeit nach neuartigen Antibiotika, deren Wirkungsspektrum auch resistente Stämme umfassen. Hierbei stellen die Carpabeneme die aussichtsreichste Klasse von Verbindungen dar.
Die durch das vorliegende Patentportfolio geschützte Wirkstoff-Klasse zählt zu den Carpabenemen, die gegen die meisten Penicillin und Cephalosporin-resistenten Stämme wirksam ist. Darüber hinaus zeigten sie bereits in-vitro eine hohe Wirksamkeit und können oral ohne Nebenwirkungen dem Patienten verabreicht werden. Ein weiterer Vorteil ist die im Vergleich zu anderen Antibiotika sehr einfache und kostengünstige Synthese.
3. Development Stage
Die Wirkstoffkandidaten aus der geschützten Klasse wurden bereits in-vitro und im Tiermodell (Maus, Hund) auf Ihre Wirksamkeit und Toxizität hin geprüft. Auch wurde bereits im Tiermodell die Effektivität der oralen Gabe erfolgreich unter Beweis gestellt. Die prä-klinischen Versuche können somit als erfolgreich abgeschlossen angesehen werden. Vollständig offen sind die noch die sog. klinischen Phasen, welche für die Zulassung als Medikament notwendig sind.
4. IP Status
Die Schutzrechte wurden in folgenden Ländern erteilt: Österreich, Belgien, Schweiz, Deutschland, Spanien, Frankreich, Großbritannien. Irland, Italien, Niederlande, Portugal, Schweden (EP1100800). Darüber hinaus sind die Schutzrechte in Australien, Kanada, China, USA, Südafrika, Israel, Mexiko und Neuseeland erteilt. Die Erteilung in Japan steht noch aus.
5. Commercialisation Model
Damit der geschützte Wirkstoff als Medikament direkt dem Patienten zugute kommt, müssen nach dem erfolgreichen Abschluss der prä-klinischen Tests die sog. klinischen Phasen erfolgreich realisiert werden, damit der Wirkstoff als Medikament zugelassen werden kann. Dabei handelt es sich um mindestens vier auf einander aufbauende Phasen.
Phase # Patienten Dauer Gegenstand Durchschnittliche Kosten
0 10-20 mehrere Wochen (12-16) Pharmakokinetik, Phar-makodynamik 1,5 Mio. US-$
I 20-80 mehrere Wochen (36-44) Verträglichkeit, Sicherheit 7-10 Mio. US-$
II 50-200 mehrere Monate Therapiekonzept, Dosierung 23 Mio. US-$
III 200-10.0000 2-5 Jahre Signifikanter Wirksamkeitsnachweis 86 Mio. US-$
DiMasi. J. A. et al. (2003): The pries o! Innovation: new estimates et drug development costs. In: J Health Econ. Bd. 22,
S. 151-185
Aus Verwertungssicht müssen nicht sämtliche Phasen vollständig durchlaufen werden. Vielmehr kann es schon möglich sein, durch einen ersten klinischen proof-of-concept (Phase I) Interessenten für die Schutzrechte und vor allem für die zugrunde liegenden Wirkstoff-Kandidaten zu finden. Ohne diesen Beleg der Wirksamkeit wird es sehr schwer, einen Interessenten zu finden, der zu einem angemessenen Preis die Schutzrechte übernimmt.
Das Ziel und somit das zu vermarktende Produkt sind dabei die Wirkstoffkandidaten mit einem erfolgreichen proof-of-concept, abgesichert durch die entsprechenden Schutzrechte. Die Schutzrechte könnten dann entweder direkt verkauft oder als exklusive Lizenz an Hersteller von Antibiotika, typischerweise große Pharmaunternehmen wie Sanofi-Aventis, Novartis, AstraZeneca oder BayerhealthCare vergeben werden. Die Betrachtung ähnlicher Vorgänge im Pharmabereich zeigen, dass häufig eine Kombination von up-front Zahlungen im sieben- bis achtstelligen Bereich zuzüglich einer umsatzabhängigen Lizenzgebühren gewählt wird.
Als Strategie zur Verwertung stellen sich folgende Schritte als notwendig dar: 1.) Durchführung der Tests gemäß Phase 0 (ggf. am Institut des Erfinders), 2.) Identifizierung eines wissenschaftlichen Partners für die Phase-I-Untersuchungen (i.d.R. Universitätsklinika) 2.) Rekrutierung und Screening passender Patienten 3.) Verpflichtung einer Contract Research Organisation (CRO) als durchführendes Organ der Studie 4.) Statistische Auswertung und Publikation der Ergebnisse (für Zulassung als auch Marketing). 5.) wenngleich parallel zu den vorherigen Schritten: Identifikation und Ansprache von potentiellen Interessenten aus dem Bereich der forschenden Pharmaunternehmen als Lizenznehmer/ -käufer.
Dauer und Kosten für diese Schritte dürften sich in der Größenordnung von mindestens einem Jahr und Barausgaben von rund 10 Mio. € belaufen (Prognose auf Basis von Erfahrungswelten). Um diese realisieren zu können, bedarf es einer Partnerschaft mit einem intermediären Forschungs- und Entwicklungspartner, der diese Arbeiten mitträgt und mitfinanziert. In Frage dafür kommt eine Partnerschaft mit beispielsweise der Lead Discovery Center GmbH, eine Ausgründung aus der Max-Planck-Gesellschaft, welche sich ausschließlich auf die Weiterentwicklung von Wirkstoffkandidaten von der Prä-Klinik in die klinischen Phasen spezialisiert hat. Dieser Partner könnte dann auch am Erfolg und Umfang der weiteren Kommerzialisierung partizipieren. Dieses würde geringere anfängliche Kosten bei der Beautragung und Durchführung der Arbeiten ermöglichen, und somit die anfänglich aufgeführten Kosten von 10 Mio.€ signifikant senken. Unterstützt werden können diese Arbeiten auch durch weitere Maßnahmen aus dem Bundesförderungsschwerpunktprogramm „BioPharma“.
6. Market / Opportunity
Als finanzieller Rahmen dieser Verwertungsstrategie kommt nicht primär die Verdienstmöglichkeit je Pa-Patient in Frage. Vielmehr sind ähnliche Transaktionen von Phase-I validierten Wirkstoffkandidaten zu großen Pharmaunternehmen als Referenz zu nutzen. Ein prominentes Beispiel ist ein validierter Impf-Wirkstoff (3151x, Affiris AG) gegen Alzheimer, welcher gegen Einmalzahlung und umsatzabhängigen Lizenzgebühren an GlaxoSmithKline auslizenziert wurde. Das Volumen der Einmalzahlung beträgt 22,5 Mio. €.
Jüngste weitere Transaktionen im Bereich der Wirkstoffkandidaten bewegen sich in einem ähnlichen Bereich (venture capital-backed): Globelmmune 41 Mio. US-$ (Immunsystem-Beeinflussung), Nereus Pharmaceuticals 45 Mio US-$ (Anti-Tumor-Wirkstoff, sogar vor Phase-I). Agensys Kauf durch Astella für 387 Mio. US-$. (monoklonaler Antikörper gegen Tumore).
7. Kontaktdaten
If you are interested in the described technology and/or further information on the Patent, please contact
engage – Key Technology Ventures AG
Mr. Moritz v. Grotthuss
Gerhart-Hauptmann-Strasse 23
D-18055 Rostock (Germany)
Tel. +49 (381) 49747-39
Fax. +49 (381) 49747-40
E-Mail: m.vongrotthuss@engage-ventures.com
Media Contact
Weitere Informationen:
http://www.pva-mv.deAlle Nachrichten aus der Kategorie: Technologieangebote
Neueste Beiträge
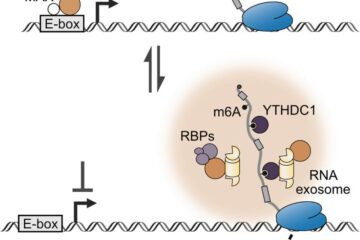
Forschende enthüllen neue Funktion von Onkoproteinen
Forschende der Uni Würzburg haben herausgefunden: Das Onkoprotein MYCN lässt Krebszellen nicht nur stärker wachsen, sondern macht sie auch resistenter gegen Medikamente. Für die Entwicklung neuer Therapien ist das ein…

Mit Kleinsatelliten den Asteroiden Apophis erforschen
In fünf Jahren fliegt ein größerer Asteroid sehr nah an der Erde vorbei – eine einmalige Chance, ihn zu erforschen. An der Uni Würzburg werden Konzepte für eine nationale Kleinsatellitenmission…

Zellskelett-Gene regulieren Vernetzung im Säugerhirn
Marburger Forschungsteam beleuchtet, wie Nervenzellen Netzwerke bilden. Ein Molekülpaar zu trennen, hat Auswirkungen auf das Networking im Hirn: So lässt sich zusammenfassen, was eine Marburger Forschungsgruppe jetzt über die Vernetzung…

















