Tumorzellen in den Tod treiben
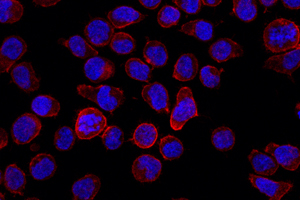
Zellen aus einem B-Zell-Tumor. Foto: Arbeitsgruppe Reth/Universität Freiburg
Die B-Zell-akute lymphoblastische Leukämie (B-ALL) ist die häufigste Tumorerkrankung im Kindesalter und tritt auch bei Erwachsenen auf. Sie entsteht, wenn die Signalleitung in unreifen B-Zellen, auch prä-B-Zellen genannt, gestört ist.
Das Team um Prof. Dr. Markus Müschen von der University of California in San Francisco/USA hat mit Unterstützung von Prof. Dr. Hassan Jumaa und Prof. Dr. Michael Reth vom Exzellenzcluster BIOSS Centre for Biological Signalling Studies der Universität Freiburg einen neuen Ansatz für die Therapie der B-ALL-Tumorerkrankung gefunden.
Ihre Untersuchungen könnten ein Umdenken in den klinischen Ansätzen für die Therapie der Tumorerkrankung bewirken. Die Wissenschaftlerinnen und Wissenschaftler haben ihre Ergebnisse in der Fachzeitschrift „Nature“ veröffentlicht.
B-Zellen gehören zu den weißen Blutkörperchen und produzieren Antikörper gegen Antigene, die das Immunsystem als Fremdstoffe erkennt. Die normale B-Zellentwicklung und -reifung wird über ein Gleichgewicht zwischen Kinasen und Phosphatasen gesteuert.
Diese Enzyme phosphorylieren oder dephosphorylieren die Signaluntereinheiten des B-Zell-Antigenrezeptors (BCR) auf der B-Zelle: Die Kinasen fügen dem BCR Phosphatgruppen hinzu, während die Phosphatasen diese entfernen. Nur der durch Kinasen phosphorylierte BCR ist voll aktiv und teilt der B-Zelle mit, dass es einen Fremdstoff gibt. Somit bestimmen die Kinasen und Phosphatasen die Signalstärke des Rezeptors.
Bei B-ALL Tumorzellen sind bestimmte Kinasen wie die Abelson-Tyrosinkinase (Abl-Kinase) verändert: Sie treiben als Onkogene das Tumorwachstum an. Die B-Zellen sind funktionsuntüchtig, aber teilen sich fortlaufend. Als Therapie gegen diese Erkrankung kommen Wirkstoffe zum Einsatz, welche die Abl-Kinase hemmen. Oft kommt es allerdings zu resistenten Abl-Mutanten und der Tumor wächst erneut.
Das deutsch-amerikanische Forschungsteam hat untersucht, wie genau die Signalleitung des BCR in den Tumoren reguliert ist. Sie entdeckten, dass bei B-ALL-Tumorzellen die Signaluntereinheiten des BCR wenig aktiv sind und auf der Oberfläche verstärkt hemmende Rezeptoren vorkommen.
Diese binden Phosphatasen und verhindern so, dass der BCR aktiviert wird. Wenn die Wissenschaftler die hemmenden Rezeptoren oder die assoziierten Phosphatasen ausschalteten, war der sofortige Tod der ALL-Zellen die Folge. Die Forscher zeigten auch, dass ein Hemmer der Phosphatasen im Tierexperiment die Tumorausbreitung verhindert.
Der Grund: Indem sie die Phosphatasen hemmten, öffneten die Forschenden sozusagen den Signalweg des BCR wieder, den die Abl-Kinase zuvor unterdrückt hatte. In einer B-Zelle, bei der übermäßig viele BCR-Rezeptoren aktiviert sind, sind Kinasen und Phosphatasen nicht mehr im Gleichgewicht. Die Therapie treibt sie somit in den Zelltod, auch Apoptosis genannt.
Zukünftige Therapien der B-ALL könnten statt der Abl-Kinase die Phosphatasen hemmen und somit die BCR-Signale verstärken. „Als Teil des BIOSS-Programms haben wir in den vergangenen Jahren die Bedeutung des Kinasen-Phosphatasen-Gleichgewichts für die normale Entwicklung der B-Lymphozyten untersucht. Jetzt sehen wir, dass dieses Gleichgewicht auch bei der Entstehung und Bekämpfung von B-Zelltumoren eine wichtige Rolle spielt“, sagt Reth.
Reth ist Sprecher des Exzellenzclusters BIOSS Centre for Biological Signalling Studies und Professor am Institut für Biologie III der Albert-Ludwigs-Universität. Zudem ist er Gruppenleiter am Freiburger Max-Planck-Institut für Immunbiologie und Epigenetik. Jumaa ist Professor am Institut für Immunologie der Universität Ulm und war Mitglied des BIOSS Centre for Biological Signalling Studies.
Originalpublikation:
Zhengshan Chen, Seyedmehdi Shojaee, Maike Buchner, Huimin Geng, Jae Woong Lee, Lars Klemm, Björn Titz, Thomas G. Graeber, Eugene Park, Ying Xim Tan, Anne Satterthwaite, Elisabeth Paietta, Stephen P. Hunger, Chery L Willman, Ari Melnick, Mignon L Loh, Jae U. Jung, John E. Coligan, Silvia Bolland, Tak W. Mak, Andre Limnander, Hassan Jumaa, Michael Reth, Arthur Weiss, Clifford A. Lowell and Markus Müschen (2015). Signaling thresholds and negative B cell selection in acute lymphoblastic leukemia. Nature. DOI: 10.1038/nature14231
Kontakt:
Prof. Dr. Michael Reth
BIOSS Centre for Biological Signalling Studies
Albert-Ludwigs-Universität Freiburg
Tel.: 0761/203-97663
E-Mail: michael.reth@bioss.uni-freiburg.de
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge
Experiment öffnet Tür für Millionen von Qubits auf einem Chip
Forschenden der Universität Basel und des NCCR SPIN ist es erstmals gelungen, eine kontrollierbare Wechselwirkung zwischen zwei Lochspin-Qubits in einem herkömmlichen Silizium-Transistor zu realisieren. Diese Entwicklung eröffnet die Möglichkeit, Millionen…

Stofftrennung trifft auf Energiewende
Trennkolonnen dienen der Separation von unterschiedlichsten Stoffgemischen in der chemischen Industrie. Die steigende Nutzung erneuerbarer Energiequellen bringt nun jedoch neue Anforderungen für einen flexibleren Betrieb mit sich. Im Projekt ColTray…

Kreuzfahrtschiff als Datensammler
Helmholtz-Innovationsplattform und HX Hurtigruten Expeditions erproben neue Wege in der Ozeanbeobachtung. Wissenschaftliche Forschung nicht nur von speziellen Forschungsschiffen aus zu betreiben, sondern auch von nicht-wissenschaftlichen Schiffen und marinen Infrastrukturen –…