Haifisch-Antikörper inspirieren Optimierung menschlicher Antikörper: Lernen vom Haifisch

Strukturelles Modell des IgNAR Hai-Antikörpers Bild: Janosch Hennig, TUM/Helmholtz Zentrum
Ein wichtiges Kriterium bei der Konstruktion geeigneter Antikörperfragmente ist ihre Stabilität. Beim Vergleich der Antikörper des evolutionsbiologisch sehr alten Haifischs mit denen des Menschen fand ein Wissenschaftlerteam der Technischen Universität München (TUM) und des Helmholtz Zentrums München Stabilisierungsmechanismen, die sich auch für maßgeschneiderte Antikörper zum Einsatz beim Menschen nutzen lassen.
Maßgeschneiderte Antikörper gelten als aussichtsreiche Mittel gegen eine Vielzahl schwerer Krankheiten. Da sie präzise bestimmte Strukturen auf der Oberfläche von Viren, Bakterien oder Krebszellen erkennen können, werden sie bereits erfolgreich in Krebsdiagnostik und -therapie sowie gegen eine Vielzahl anderer Krankheiten eingesetzt. Bei allen Schritten, von der Produktion über die Lagerung bis hin zum therapeutischen Einsatz, ist die Stabilität der empfindlichen Antikörper ein entscheidender Faktor.
Neue Ansätze zur Stabilisierung von Antikörpern erhoffte sich ein Team um Dr. Matthias J. Feige sowie die Professoren Linda Hendershot vom St. Jude Children’s Research Hospital in Memphis (Tennessee, USA), Michael Sattler (Inhaber des Lehrstuhls für biomolekulare NMR Spektroskopie an der TU München und Institut für Strukturbiologie des Helmholtz Zentrums München), Michael Groll (Inhaber des Lehrstuhls für Biochemie an der TU München) und Johannes Buchner (Inhaber des Lehrstuhls für Biotechnologie an der TU München) vom Vergleich von Säugetier-Antikörpern mit denen von Haifischen.
Haifische gibt es bereits seit 500 Millionen Jahren. Sie gehören entwicklungsbiologisch zu den ältesten Tieren, die über ein „modernes“ Immunsystem ähnlich dem des Menschen verfügen. Damit der Hai im Salzwasser überleben kann, enthält sein Blut große Mengen an Harnstoff. Dieser schützt den Hai zwar vor Wasserverlust, kann aber gleichzeitig auch empfindliche Proteinmoleküle wie die Antikörper destabilisieren.
„Menschliche Antikörper würden unter diesen Bedingungen zusammenbrechen. Hai-Antikörper müssen also strukturelle Eigenschaften besitzen, die sie besonders widerstandsfähig machen“, sagt Matthias J. Feige, Erstautor der Publikation. „Dieses Geheimnis wollten wir lüften.“
Für ihre Untersuchungen wählten sie den Haifisch-Antikörper IgNAR (Immunoglobulin New Antigen Receptor). Da es bisher kaum strukturelle Informationen über das Molekül gab und es sich nicht in Gänze kristallisieren ließ, entwickelten sie in detektivischer Puzzlearbeit ein Modell des Antikörpers.
Sie kristallisierten Teilstücke und ermittelten deren atomaren Aufbau mittels Röntgenstrukturanalyse, verglichen Teilabschnitte mit bereits bekannten Strukturen anderer Immunglobuline. Die Strukturen anderer Teile des Antikörpers wurden mittels Kernmagnetresonanz-Spektroskopie gelöst. Wieder und wieder verglichen sie die ermittelten Strukturen und räumlichen Abstände mit den Ergebnissen von Röntgenstreumessungen an natürlichen Hai-Antikörpern und konnten so schließlich ein vollständiges Modell des Antikörpers aufbauen.
Die genauere Betrachtung der Struktur dieses Proteins zeigte, dass sich die für Antikörper typische Ig-Faltung offenbar schon vor mehr als 500 Millionen Jahren entwickelt hat, da sie auch beim Haifisch schon zu finden ist. Auch den Grund für die hohe Stabilität der Haifisch-Antikörper konnten die Forscher aufklären: Sie resultiert aus einer zusätzlichen Salzbrücke zwischen strukturell wichtigen Aminosäureketten sowie einem besonders großen unpolaren Kern der Ig-Faltung im Hai-Antikörper.
Den Forschern gelang es, beide Stabilisierungsprinzipen in menschliche Antikörper einzubauen. Tatsächlich führte die Kombination beider Prinzipien zu deutlich stabileren menschlichen Antikörperfragmenten. Ihr Schmelzpunkt lag zehn Grad höher als der des ursprünglichen Moleküls.
Auch in Säugetierzellen, in denen therapeutische Antikörper normalerweise produziert werden, zeigte die höhere Stabilität positive Effekte: Die veränderten Antikörper wurden in deutlich größerer Menge produziert. In naher Zukunft, so hoffen die Forscher, werden diese Erkenntnisse dazu beitragen, verbesserte therapeutische und diagnostische Antikörper aufbauen zu können. Sie sollten sich einfacher herstellen und besser lagern lassen sowie im menschlichen Organismus länger aktiv bleiben um ihr ganzes therapeutisches Potential entfalten zu können.
Die Arbeiten wurden unterstützt mit Mitteln des National Institutes of Health (NIH), der Deutschen Forschungsgemeinschaft (DFG), des Exzellenzclusters Center for Integrated Protein Science Munich (CIPSM), der Deutschen Akademie der Naturforscher Leopoldina, des St. Jude Children’s Research Hospital, der Peter und Traudl Engelhorn Stiftung, der Studienstiftung des Deutschen Volkes, der European Molecular Biology Organization (EMBO), des Swedish Research Council sowie des Boehringer Ingelheim Fonds. NMR-Messungen wurden am Bayerischen NMR Zentrum (BNMRZ) durchgeführt. Röntgenstrukturdaten wurden an der Synchrotron-Strahlungsquelle des Paul Scherrer Instituts (Villigen, Schweiz) ermittelt.
Publikation:
The structural analysis of shark IgNAR antibodies reveals evolutionary principles of immunoglobulins
Matthias J. Feige, Melissa A. Graewert, Moritz Marcinowski, Janosch Hennig, Julia Behnke, David Ausländerb, Eva M. Herold, Jirka Peschek, Caitlin D. Castro, Martin Flajnik, Linda M. Hendershot, Michael Sattler, Michael Groll, and Johannes Buchner
PNAS, Early Edition, http://www.pnas.org/cgi/doi/10.1073/pnas.1321502111
(voraussichtlich online am 15. Mai 2014)
Kontakt:
Prof. Dr. Johannes Buchner
Technische Universität München
Fakultät für Chemie, Lehrstuhl für Biotechnologie
Lichtenbergstraße 4, 85748 Garching, Germany
Tel.: +49 89 289 13341 – E-Mail: Johannes.Buchner@tum.de
Internet: http://www.chemie.tu-muenchen.de/biotech/index.html
Media Contact
Weitere Informationen:
http://www.tum.deAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…
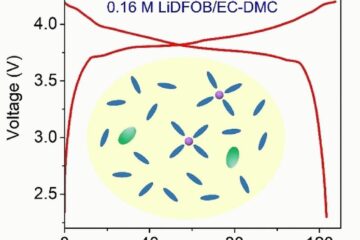
Für kostengünstigere, nachhaltigere Akkus
Ultraniedrig konzentrierter Elektrolyt für Lithium-Ionen-Batterien Lithium-Salze machen Akkumulatoren leistungsfähig, aber teuer. Ein ultraniedrig konzentrierter Elektrolyt auf Basis des Lithium-Salzes LiDFOB könnte eine kostengünstige und dabei nachhaltigere Alternative sein. Zellen mit…





















