Die Entschlüsselung der Struktur des Huntingtin Proteins
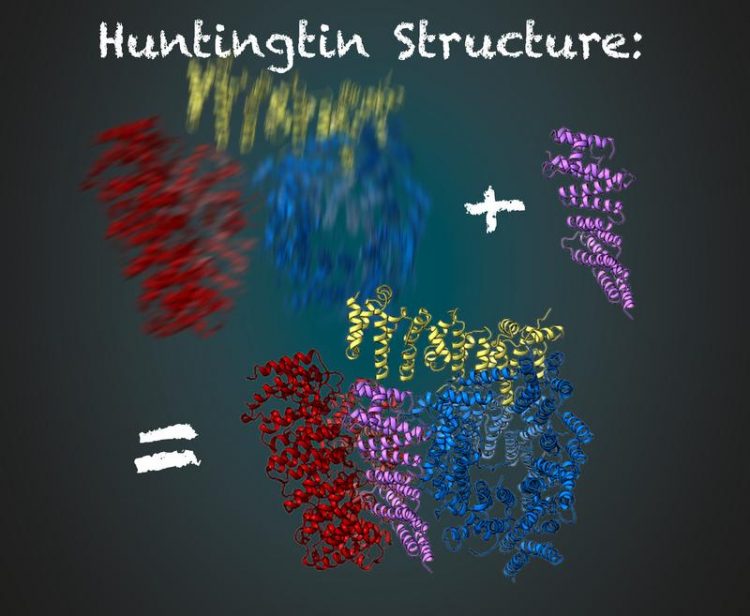
Huntingtin besteht aus drei flexiblen Bereichen (rot, gelb und blau). Stabilisiert durch HAP40 (violett) ist die Entschlüsselung der dreidimensionalen Struktur mithilfe der Kryo-EM möglich. Illustration: Gabriele Stautner, ARTIFOX © Max-Planck-Institut für Biochemie
Die Huntington-Krankheit beginnt häufig mit Störungen des Gefühlslebens und ist durch unwillkürliche Muskelbewegungen und dem Verlust geistiger Fähigkeiten charakterisiert. Die neurologische Erkrankung zählt zu den bis heute unheilbaren und zum Tode führenden Erbkrankheiten.
Das Protein HTT, auch Huntingtin genannt, spielt die zentrale Rolle bei der Huntington-Krankheit. Das Huntingtin Gen ist die Bauanleitung für das gleichnamige Protein. Seit 25 Jahren ist bekannt, dass Mutationen in diesem Gen die Ursache für die Huntington-Krankheit sind.
Obwohl seit vielen Jahren an der Erkrankung geforscht wird, gibt es immer noch viele Hürden zu überwinden. Jetzt ist es in der Zusammenarbeit von Rubén Fernández-Busnadiego aus der Abteilung „Molekulare Strukturbiologie“ am MPI für Biochemie und Stefan Kochanek, Leiter der Abteilung „Gentherapie“ am Universitätsklinikum Ulm, gelungen, die molekulare, dreidimensionale Struktur des Huntingtin Proteins zu entschlüsseln.
Überwundene Hürde
Schon viele Jahre haben Wissenschaftler wie Stefan Kochanek von der Ulmer Universitätsmedizin an der Produktion und Aufreinigung von Huntingtin gearbeitet. Doch was hat eine detaillierte Analyse des Proteins in den letzten Jahrzehnten verhindert? Fernández-Busnadiego, Experte für Kryo-Elektronenmikroskopie, nennt zwei Hauptgründe: „Die Kryo-Elektronenmikroskopie wurde erst in den letzten Jahren soweit optimiert, um Proteinstrukturen mit fast molekularer Auflösung anzuschauen. Der zweite Grund ist, dass das Huntingtin-Protein in seiner Struktur sehr beweglich ist. Auch dafür haben wir erst jetzt eine Lösung gefunden.“
Bei der Analyse wird das Protein aus unterschiedlichen Perspektiven unter dem Mikroskop aufgenommen. Aus der Vielzahl der entstandenen Bilder kann die dreidimensionale, molekulare Struktur errechnet werden. Dafür muss das Protein immer in der gleichen Form vorliegen. Fernández-Busnadiego erklärt: „Vergleichbar wäre dies mit einer Person, die im Dunkeln fotografiert wird. Bleibt die Person nicht für eine Weile ruhig stehen, wird die Aufnahme verschwommen.“
Um ein scharfes Bild zu erhalten, haben die Forscher um Kochanek nach weiteren Proteinen gesucht, die mit Huntingtin in Verbindung stehen und es stabilisieren. „Ein Protein, dass Huntingtin für die Kryo-Elektronenmikroskopie stabilisiert ist HAP40. So konnten wir, gemittelt über viele Bilder, die dreidimensionale Struktur ableiten“, so Kochanek. „Bleiben wir in der Analogie vom Foto im Dunkeln, dann wirkt das Protein wie ein Stuhl für die fotografierte Person. Darauf sitzend, bewegt sich die Person viel weniger und das Bild wird bei gleicher Belichtungszeit viel schärfer“, ergänzt Fernández-Busnadiego.
Wozu wird die dreidimensionale Struktur von Huntingtin benötigt?
„Wir wissen zwar seit einer Weile, dass die Mutation des Huntingtin-Gens schlimme Folgen hat, doch ist bis heute nur relativ wenig über die Funktion und die Aufgaben des gesunden Proteins bekannt“, erklärt Kochanek. Proteine sind die molekularen Maschinen der Zelle. Um ihre vielseitigen Aufgaben zu erfüllen, haben diese eine bestimmte dreidimensionale Struktur, ähnlich wie ein bestimmtes Bauteil in einer Maschine.
„Da wir jetzt den exakten Aufbau des Bauteils Huntingtin kennen, können wir in weiteren Studien untersuchen, welche Bereiche von Huntingtin besonders wichtig sind und wie andere Protein mit Huntingtin funktionell zusammenarbeiten. Auf diese Weise könnten Strukturen entschlüsselt werden, an denen bestimmte Wirkstoffe therapeutisch angreifen.“
In der Erforschung der Huntington-Krankheit gibt es derzeit viel Bewegung. Große Hoffnung richtet sich derzeit auf eine ‚Stummschaltung' des Huntingtin Gens mit sogenannten Antisense-Oligonukleotiden (ASO) zur Behandlung der Huntington-Krankheit. Diese kleinen Moleküle vermindern die Bildung des Huntingtin Proteins in den Zellen.
Dabei kann das Medikament nicht zwischen dem normalen und dem krankhaft veränderten Huntingtin-Protein unterscheiden. Auch aus diesem Grund ist es wichtig, mehr über die Funktion des gesunden Huntingtin Proteins zu lernen. „Die entschlüsselte Struktur wird uns einen großen Schritt voran bringen“, schaut Kochanek in die Zukunft.
[CM]
Kommentar vom Kliniker
Bernhard Landwehrmeyer ist Leiter der Huntington Ambulanz der Abteilung Neurologie am Universitätsklinikum Ulm (Rehabilitations- und Universitätskliniken Ulm/RKU) und Leiter der weltgrößten internationalen Kohortenstudie zur Huntington-Krankheit (mit mehr als 16.000 Teilnehmern):
„Die Aufklärung der Struktur von Huntingtin ist ein gewaltiger Schritt voran für die vielen Familien, die auf eine wirksame Behandlung der Huntington Krankheit hoffen. Die Krankheit ist zum Teil Folge neuer Eigenschaften, die die krankhaft veränderten Huntingtin-Genprodukte durch die Huntington-Mutation erwerben, zum Teil aber auch eine Folge einer Beeinträchtigung der normalen Funktion von Huntingtin. Jetzt – mit der Kenntnis der Struktur von Huntingtin – können viel rascher und gezielter Fragen zur normalen Funktion von Huntingtin geklärt werden und passgenaue Wirkstoffe entwickelt werden, die die normale Funktion fördern.“
„Die Antisense-Oligonukeotid (ASO)-Behandlungsversuche werden bisher erst an wenigen Kliniken durchgeführt; die Neurologische Universitätsklinik Ulm leitet die Medikamentenprüfung für Deutschland. Einige der zur Zeit geprüften ASOs senken sowohl die Bildung des normalen als auch die des krankhaft veränderten Huntingtin Proteins, andere ASOs streben an, in erster Linie das veränderte Huntingtin zu senken. Zurzeit ist ungeklärt, ob eine teilweise Hemmung der Bildung des normalen Huntingtin Eiweißes Nachteile mit sich bringt und ohne unerwünschte Wirkungen vertragen wird. Auch aus diesem Grund ist es wichtig, mehr über die normale Funktion des Huntingtin Proteins zu lernen. Hierzu wird die jetzt im Fachjournal Nature veröffentlichte Untersuchung einen wichtigen Beitrag leisten.“
Originalpublikation:
Q. Guo, B. Huang, J. Cheng, M. Seefelder, T. Engler, G. Pfeifer, P. Oeckl, M. Otto, F. Moser, M. Maurer, A. Pautsch, W. Baumeister, & R. Fernández-Busnadiego and S. Kochanek: The cryo-EM structure of huntingtin, Nature, Februar 2018
DOI: 10.1038/nature25502
Kontakt:
Dr. Rubén Fernández-Busnadiego
Molekulare Strukturbiologie
Max-Planck-Institut für Biochemie
Am Klopferspitz 18
82152 Martinsried
E-Mail: ruben@biochem.mpg.de
http://www.biochem.mpg.de/en/rd/baumeister
Dr. Christiane Menzfeld
Öffentlichkeitsarbeit
Max-Planck-Institut für Biochemie
Am Klopferspitz 18
82152 Martinsried
Tel. +49 89 8578-2824
E-Mail: pr@biochem.mpg.de
http://www.biochem.mpg.de
Prof. Dr. Stefan Kochanek
Abteilung Gentherapie
Universitätsklinikum Ulm
Helmholtzstr. 8/1
89081 Ulm
E-Mail: stefan.kochanek@uni-ulm.de
https://www.uniklinik-ulm.de/abteilung-gentherapie.html
Annika Bingmann
Presse- und Öffentlichkeitsarbeit
Universität Ulm
Helmholtzstraße 16
89081 Ulm
Tel.: 0731-50 22121
Fax.: 0731-50 22048
E-Mail: annika.bingmann@uni-ulm.de
http://www.uni-ulm.de/universitaet/hochschulkommunikation/presse-und-oeffentlich…
http://www.biochem.mpg.de/news/pressroom – Pressemitteilungen des MPIs für Biochemie
http://www.biochem.mpg.de/en/rd/baumeister – Webseite der Abteilung „Molekulare Strukturbiologie“
https://twitter.com/MPI_Biochem – Twitter @MPI_Biochem
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















