Wie das Schlucken gesteuert wird
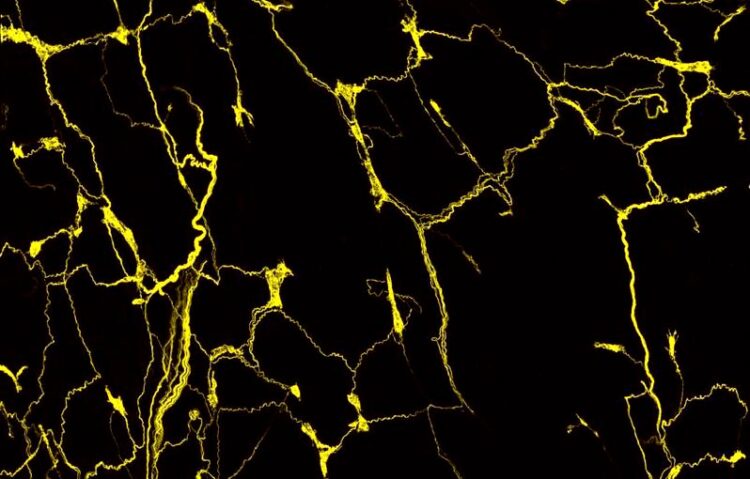
Konfokale Mikroskop-Aufnahme: Die Axone der sensorischen Nervenzellen bilden ein feines Netzwerk in der Speiseröhre der Maus. Die Fortsätze der sensorischen Neuronen, die zu einem Zellknoten des Vagusnervs (vagales Ganglion) gehören, sind gelb angefärbt.
(c) Elijah D. Lowenstein / AG C. Birchmeier, Max Delbrück Center
Sensorische Zellen des zehnten Hirnnervs erkennen, ob und wo sich in der Speiseröhre Nahrung befindet. Ihre Signale bewirken den Weitertransport zum Magen. Fallen sie aus, führe dies zu Schluckstörungen, schreibt ein Team um Carmen Birchmeier vom Max Delbrück Center jetzt im Fachblatt „Neuron“.

(c) Elijah D. Lowenstein / AG C. Birchmeier, Max Delbrück Center
Schluckbeschwerden können viele Ursachen haben. Ältere Menschen zum Beispiel leiden vermehrt daran. Aber auch neurologische Erkrankungen wie Multiple Sklerose und Parkinson oder bestimmte Medikamente führen mitunter dazu, dass die Nahrung nicht mehr ohne Weiteres vom Mund in den Magen gelangt. Die möglichen Folgen sind Mangelernährung, Gewichtsverlust und Austrocknung.
Ein Team um Professorin Carmen Birchmeier, die am Berliner Max Delbrück Center die Arbeitsgruppe „Entwicklungsbiologie / Signaltransduktion in Nerven und Muskelzellen“ leitet, hat den Schluckvorgang jetzt genauer analysiert. Im Fachblatt „Neuron“ beschreiben die Forschenden sensorische Zellen des zehnten Hirnnervs, Nervus vagus genannt, die auf mechanische Reize in der Speiseröhre reagieren und deren unbewusste Bewegung anregen. Insgesamt gibt es zwölf Hirnnerven, die direkt im Gehirn entspringen und den Kopf, den Hals und Organe im Rumpf ansteuern. Die Ergebnisse der Studie könnten in Zukunft dabei helfen, Schluckstörungen besser zu behandeln.
Videos vom Schluckvorgang
„Die modernen Methoden der Einzelzellsequenzierung haben unsere Arbeit möglich gemacht“, erläutert Birchmeier. „Mithilfe der dabei gewonnenen Daten konnten wir genetische Modelle herstellen, die es uns erlaubt haben, die Funktionen der sensorischen Nervenzellen in den vagalen Ganglien im Halsbereich genauer zu untersuchen.“ Ganglien sind eine Ansammlung von Nervenzellkörpern im peripheren Nervensystem und werden daher auch als Nervenknoten bezeichnet.
Die Wissenschaftler*innen färbten die Nervenzellen zunächst an, um zu prüfen, welche Organe sie ansteuern. Anschließend ermittelten sie, ob und wie sie auf mechanische Reize in der Speiseröhre reagieren. In einem letzten Schritt schalteten sie die Zellen aus, um die Konsequenzen für den Schluckvorgang zu analysieren. Dr. Teresa Lever von der University of Missouri School of Medicine in Columbia hat dafür ein Verfahren entwickelt, mit dem die Forschenden den Schluckvorgang in frei agierenden, nicht betäubten Mäusen per Video-Fluoroskopie in Echtzeit beobachten konnten.
Nicht nur ein hohler Schlauch
„Der Verlust der Nervenzellen, die mechanische Reize aus der Speiseröhre reflexartig in Muskelbewegungen umwandeln, welche die Nahrung Richtung Magen befördern, führte bei den Mäusen nach kurzer Zeit zu einer Gewichtsabnahme“, erläutert der Erstautor Dr. Elijah Lowenstein, der mit dieser Arbeit im Team von Birchmeier promoviert hat. Mittlerweile forscht er an der Harvard Medical School in Boston. Der Gewichtsverlust zeige, dass diese Neuronen eine Schlüsselrolle bei der körperlichen Homöostase spielen.
„Die Speiseröhre ist also nicht nur ein hohler Schlauch, der den Mund mit dem Magen verbindet“, sagt Lowenstein. „Sondern sie ist auf eine mechanosensorische Rückkopplung angewiesen, um ihre Funktion zu erfüllen.“ Ohne diese Zellen des Vagusnervs bleibe die Nahrung buchstäblich in der Speiseröhre stecken, ergänzt Birchmeier. Teilweise sei sie bei den Mäusen sogar in den Rachen zurückgeflossen.
Ein molekularer Atlas für alle
„Unsere Arbeit kann jetzt dazu beitragen, Schluckbeschwerden künftig besser zu behandeln – etwa indem man die von uns entdeckten Mechanorezeptoren pharmakologisch aktiviert“, sagt die Forscherin. Zudem möchte Birchmeier die genetischen Modelle nutzen, um die Funktionen anderer vagaler sensorischer Nervenzellen zu ermitteln – etwa jener, die die Lunge oder die Aorta ansteuern.
„Womöglich spielen diese Neuronen eine entscheidende, aber noch unbekannte Rolle bei der Entstehung bestimmter Atemwegserkrankungen oder Herz-Kreislauf-Leiden wie Bluthochdruck“, sagt sie. Auch andere Forschende können sich an diesen Projekten beteiligen: Birchmeier und ihr Team haben für alle vagalen Neurone der Maus einen molekularen Atlas erstellt, der im Internet frei zugänglich ist.
Max Delbrück Center
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (Max Delbrück Center) gehört zu den international führenden biomedizinischen Forschungszentren. Nobelpreisträger Max Delbrück, geboren in Berlin, war ein Begründer der Molekularbiologie. An den Standorten in Berlin-Buch und Mitte analysieren Forscher*innen aus rund 70 Ländern das System Mensch – die Grundlagen des Lebens von seinen kleinsten Bausteinen bis zu organ-übergreifenden Mechanismen. Wenn man versteht, was das dynamische Gleichgewicht in der Zelle, einem Organ oder im ganzen Körper steuert oder stört, kann man Krankheiten vorbeugen, sie früh diagnostizieren und mit passgenauen Therapien stoppen. Die Erkenntnisse der Grundlagenforschung sollen rasch Patient*innen zugutekommen. Das Max Delbrück Center fördert daher Ausgründungen und kooperiert in Netzwerken. Besonders eng sind die Partnerschaften mit der Charité – Universitätsmedizin Berlin im gemeinsamen Experimental and Clinical Research Center (ECRC) und dem Berlin Institute of Health (BIH) in der Charité sowie dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK). Am Max Delbrück Center arbeiten 1800 Menschen. Finanziert wird das 1992 gegründete Max Delbrück Center zu 90 Prozent vom Bund und zu 10 Prozent vom Land Berlin.
Wissenschaftliche Ansprechpartner:
Prof. Dr. Carmen Birchmeier
AG Entwicklungsbiologie / Signaltransduktion in Nerven und Muskelzellen
Max Delbrück Center
+49 (0) 30 9406-2403
cbirch@mdc-berlin.de
Originalpublikation:
Elijah D. Lowenstein et al. (2023): „Prox2 and Runx3 vagal sensory neurons regulate esophageal motility“. Neuron, DOI: 10.1016/j.neuron.2023.04.025
Weitere Informationen:
https://www.sciencedirect.com/science/article/pii/S089662732300332X?via%3Dihub – Paper
https://www.mdc-berlin.de/birchmeier-kohler AG Birchmeier
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Neues Wirkprinzip gegen Tuberkulose
Gemeinsam ist es Forschenden der Heinrich-Heine-Universität Düsseldorf (HHU) und der Universität Duisburg-Essen (UDE) gelungen, eine Gruppe von Molekülen zu identifizieren und zu synthetisieren, die auf neue Art und Weise gegen…

Gefahr durch Weltraumschrott
Neue Ausgabe von „Physikkonkret“ beleuchtet Herausforderungen und Lösungen für eine nachhaltige Nutzung des Weltraums. Die Deutsche Physikalische Gesellschaft (DPG) veröffentlicht eine neue Ausgabe ihrer Publikationsreihe „Physikkonkret“ mit dem Titel „Weltraumschrott:…

Wasserstoff: Versuchsanlage macht Elektrolyseur und Wärmepumpe gemeinsam effizient
Die nachhaltige Energiewirtschaft wartet auf den grünen Wasserstoff. Neben Importen braucht es auch effiziente, also kostengünstige heimische Elektrolyseure, die aus grünem Strom Wasserstoff erzeugen und die Nebenprodukte Sauerstoff und Wärme…





















