Schutzfunktion von regulatorischen T-Zellen nur mit T-Zell-Rezeptor möglich

Deshalb existieren zum Schutz regulatorische T-Zellen, so genannte Tregs, die überschießende Immunreaktionen und Reaktionen gegen uns selbst unterdrücken. Bisher waren zwei molekulare Eigenschaften von Tregs bekannt, die diese schützenden Funktionen steuern.
Forscher der Technischen Universität München (TUM) zeigten jetzt, dass zusätzlich Signale durch den T-Zell Rezeptor auf ihrer Oberfläche für die Identität und ihre unterdrückende Wirkung absolut essentiell sind.
T-Zellen sind wichtige Zellen des Immunsystems, die Erreger bekämpfen und die Immunantworten des Körpers steuern. Jede T-Zelle trägt ihren eigenen speziellen T-Zell Rezeptor (TZR) auf der Zelloberfläche, der jeweils nur ganz bestimmte Substanzen erkennt.
Manche T-Zellen würden aufgrund ihrer genetischen Ausstattung durch ihren TZR körpereigene Zellen erkennen und bekämpfen. Zum Schutz des Körpers werden die meisten dieser so genannten autoreaktiven Zellen im Laufe ihrer Entwicklung aussortiert und zerstört.
Eine Minderheit der autoreaktiven T-Zellen entwickeln sich zu regulatorischen T-Zellen – den Aufpassern des Immunsystems. Sie unterdrücken Immunantworten des Körpers und erfüllen somit eine wichtige Kontrollfunktion gegen zu starke Immunreaktionen. Es ist bekannt, dass sie ihren Rezeptor, der körpereigene Stoffe erkennt, für ihre Entwicklung brauchen – doch wofür brauchen sie ihn danach?
Prof. Marc Schmidt-Supprian, seit März 2014 Tenure Track Professor an der TUM, hat mit seinem Team der III. Medizinischen Klinik des TUM Klinikums rechts der Isar diese Frage untersucht. Gemeinsam mit weiteren Forschungsgruppen aus München, Freiburg, Dresden, Rijeka (Kroatien) und Osaka (Japan) inaktivierten sie hierfür zu einem bestimmten Zeitpunkt den T-Zell Rezeptor auf reifen Tregs in genetisch veränderten Mäusen. Dann verfolgten sie das weitere Schicksal der TZR-losen Zellen.
T-Zell-Rezeptor Signale sind ein essentieller Bestandteil von Tregs
Ihre Experimente zeigten deutlich: Ohne den T-Zell Rezeptor konnten die defekten Tregs ihr Aufgaben als Aufpasser des Immunsystems nicht mehr erfüllen. Darüber hinaus schrumpfte die Zellpopulation der Tregs stark, weil sich die Zellen nicht mehr vermehrten. Die Wissenschaftler fanden aber heraus, dass die zwei bekannten zentralen molekularen Eigenschaften der Tregs, die Herstellung des Proteins Foxp3 und spezifische chemische Veränderungen der DNA, in den defekten T-Zellen noch vorhanden waren.
„Ohne ihren Rezeptor sind die Tregs zwar noch eindeutig als solche identifizierbar, büßen aber einen großen Teil ihrer zellulären Identität ein. Außerdem verlieren sie ihre besondere Fähigkeit, überschießende Immunreaktionen zu unterdrücken.“, erklärt Christoph Vahl, Erstautor der Studie. „Die Tregs brauchen offensichtlich ständig Kontakt zu ihrer Umgebung, um korrekt zu funktionieren. Vermutlich besitzen sie deshalb einen Rezeptor, der körpereigene Stoffe erkennt und somit permanent Signale liefert.“
„Mit unseren Ergebnissen konnten wir einen sehr wichtigen Mechanismus für die Unterdrückung von Immunreaktionen aufklären, die gegen den Körper gerichtet oder überschießend sind. Unsere Erkenntnisse könnten auch für Situationen relevant sein, in denen man die Unterdrückung von Immunreaktionen durch Tregs schwächen möchte, wie zum Beispiel in der Krebsbekämpfung.“, meint Schmidt-Supprian.
Originalpublikation
Vahl J. C., Drees C., Heger K., Heink S., Fischer J.C., Nedjic J., Ohkura N., Morikawa H., Poeck H., Schallenberg S., Rieß D., Hein M. Y., Buch T., Polic B., Schönle A., Zeiser R., Schmitt-Gräff A., Kretschmer K., Klein L., Korn T., Sakaguchi S. and M. Schmidt-Supprian, Continuous T Cell Receptor Signals Maintain a Functional Regulatory T Cell Pool, Immunity, 2014.
DOI: 10.1016/j.immuni.2014.10.012
Kontakt
Prof. Dr. Marc Schmidt-Supprian
Lehrstuhl für Experimentelle Hämatologie
III. Medizinische Klinik
Klinikum rechts der Isar der Technischen Universität München
Tel: +49 (0)89 4140 – 4104
Email: supprian@lrz.tum.de
http://www.tum.de/die-tum/aktuelles/pressemitteilungen/kurz/article/32053/ – Dieser Text im Web
http://www.professoren.tum.de/schmidt-supprian-marc/ – Professorenprofil von Marc Schmidt-Supprian
http://www.med3.med.tum.de/forschung/Grundlagenforschung/MolecularImmunopath/ind… – Lehrstuhl für Experimentelle Hämatologie
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Wie die Galvanotechnik durch Digitalisierung effizient wird
SurfaceTechnology GERMANY… Digitalisierung und Hartverchromung aus Chrom(III)-Elektrolyten: Das sind die beiden großen Themen, mit denen sich Forscherinnen und Forscher von der Abteilung Galvanotechnik am Fraunhofer IPA derzeit beschäftigen. Ihre Erkenntnisse…

Ersatz für Tierversuche – jetzt ganz ohne Tierleid
Erstes Gewebe-Modell der Leber völlig ohne Materialien tierischer Herkunft hergestellt. Wissenschaftler*innen der TU Berlin haben mit Hilfe von 3D-Biodruck erstmals ein Modell der Leber aus menschlichen Zellen hergestellt, ohne dabei…
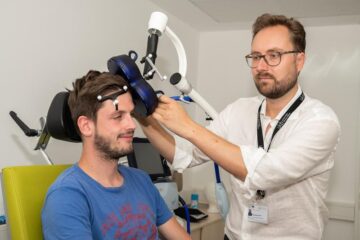
Neue Wege zur mentalen Gesundheit
Magnetspule am Kopf sorgt für antidepressive Effekte… In der Klinik und Poliklinik für Psychiatrie und Psychotherapie am Universitätsklinikum Bonn (UKB) wird derzeit eine Studie zur Erforschung der antidepressiven Wirkung einer…