Revolutionären Regulationsmechanismus der Blutgerinnung entdeckt
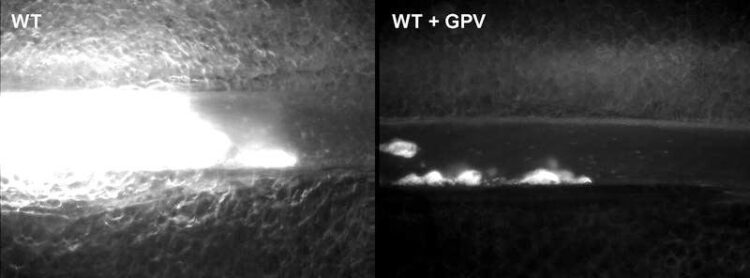
Behandlung einer Maus mit löslichem GPV verhindert die Bildung eines gefäßverschließenden Thrombus im experimentellen Modell zur Thrombosebildung (rechts). Im Vergleich dazu ist ein gefäßverschließender Thrombus einer unbehandelten Maus gezeigt (links)
(c) Sarah Beck / RVZ
Würzburger Arbeitsgruppe rund um Studienleiter Bernhard Nieswandt entschlüsselt einen von Blutplättchen vermittelten Regulationsmechanismus der Fibrinbildung bei der Blutgerinnung und leitet daraus neue Therapieansätze ab.
Die Blutstillung ist lebenswichtig, um übermäßigen Blutverlust zu vermeiden. Bei einer überschießenden Reaktion und einer unkontrollierten Bildung von Fibrin besteht jedoch ein Thrombose-Risiko. In der in Nature Cardiovascular Research publizierten Studie decken die Forschenden das Glykoprotein GPV als Schaltstelle für die Blutstillung und Thrombusbildung auf.

(c) RVZ
Wenn unsere Blutgefäße durch Schnitt- oder Schürfwunden oder Quetschungen verletzt werden, ist es lebenswichtig, dass die Blutung gestillt und die Wunde verschlossen wird. In der Fachsprache heißt dieser Prozess Hämostase. Diese besteht aus zwei Vorgängen: Der Blutstillung, bei der sich Blutplättchen (Thrombozyten) an die Wundränder heften, einen Pfropf bilden und die Verletzung provisorisch abdichten. Und der Blutgerinnung beziehungsweise Gerinnungskaskade, bei der am Ende lange Fasern aus Fibrin gebildet werden, welche gemeinsam mit den Blutplättchen die Wunde fest abdichten. Wird Fibrin jedoch im Übermaß gebildet, zum Beispiel bei chronischen Wunden, kann es zu Gefäßverschlüssen, so genannten Thrombosen, kommen. Deshalb ist eine strenge Regulierung der Fibrinbildung wichtig. Doch wie die Gerinnung begrenzt wird, war bislang nicht vollständig verstanden. In einem von der Würzburger Universitätsmedizin koordinierten, internationalen Projekt haben Forschende jetzt einen zentralen Regulationsmechanismus der Fibrinbildung entschlüsselt und daraus neue Therapieansätze abgeleitet. Die Ergebnisse wurden im renommierten Magazin Nature Cardiovascular Research veröffentlicht.
GPV kontrolliert die Aktivität von Thrombin und Bildung von Fibrin
In der Studie gelangt die Arbeitsgruppe rund um Studienleiter Prof. Dr. Bernhard Nieswandt zu grundlegend neuen Erkenntnissen: „Wir konnten erstmals eine neue Schaltstelle aufdecken, die sowohl die Blutstillung als auch die Bildung von Thrombosen reguliert. Diese Schaltstelle ist das Glykoprotein V, kurz GPV, das sich auf der Oberfläche von Blutplättchen befindet. GPV kontrolliert die Aktivität des Enzyms Thrombin, das für die Bildung von Fibrin verantwortlich ist“, erläutert Bernhard Nieswandt, Leiter des Lehrstuhls für Experimentelle Biomedizin I und Vorstand des Rudolf-Virchow-Zentrum – Center for Integrative and Translational Bioimaging (RVZ) der Universität Würzburg.
Thrombin ist ein entscheidendes Enzym in der Blutgerinnung und seine Aktivität muss daher zeitlich-räumlich sehr genau kontrolliert sein. Bisher war bekannt, dass der Oberflächenrezeptor GPV während der Aktivierung der Blutplättchen durch Thrombin geschnitten wird. Dadurch wird GPV als lösliche Rezeptorform freigesetzt. Die physiologische Funktion dieses Rezeptors war jedoch weitestgehend unbekannt. Mit genetischen und pharmakologischen Ansätzen haben die Forschenden gezeigt, dass eine Thrombin-vermittelte Abspaltung von GPV die Bildung von Fibrin begrenzt. Indem das lösliche GPV an Thrombin gebunden bleibt, verändert es die Aktivität von Thrombin, sodass dieses weniger Fibrin bilden kann.
„Erkenntnisse werden Lehrbuchwissen verändern“
In einer Reihe von Versuchen an experimentellen Thrombosemodellen konnte gezeigt werden, dass lösliches GPV unter anderem die Bildung von gefäßverschließenden Thromben verhindert und einen deutlichen Schutz vor experimentellem Schlaganfall und damit verbundener Hirnschädigung vermittelt. Bernhard Nieswandt ist davon überzeugt, dass diese neuen Erkenntnisse das Lehrbuchwissen erweitern werden, und dankt den beteiligten Wissenschaftlerinnen und Wissenschaftler des RVZ und des Universitätsklinikums Würzburg (UKW), die von Kolleginnen und Kollegen aus Mainz, Maastricht und den USA unterstützt wurden.
Antikörper gegen GPV bieten großes klinisches Potential bei Behandlung einer gestörten Hämostase
In einem weiteren Ansatz hat die Forschungsgruppe Antikörper gegen GPV generiert, die das Thrombin-vermittelte Abschneiden von GPV verhindern. „In unseren Studien konnten wir zeigen, dass diese Antikörper die Thrombin-Aktivität erhöhen und es dadurch zu einer vermehrten Fibrinbildung kommt. Unsere Idee war es deshalb, diese Antikörper im Zusammenhang mit einer gestörten Hämostase zu nutzen, um die Fibrinbildung zu erhöhen“, führt Prof. Dr. David Stegner, Leiter der Arbeitsgruppe Vaskuläre Bildgebung am RVZ und einer der Letztautoren der Studie, weiter aus. Neben genetischen Ursachen kann eine gestörte Hämostase auch auf pharmakologisch-bedingte Beeinträchtigungen der Thrombozytenanzahl oder -funktion zurückgeführt werden. Dies ist zum Beispiel nach Einnahme von Thrombozytenaggregationshemmern wie etwa Clopidogrel der Fall, die zur Vorbeugung eines Herzinfarkts oder eines Schlaganfalls und zur Behandlung von Durchblutungsstörungen eingesetzt werden.
„In einem experimentellen Modell zur Blutstillung konnte unser neuer Antikörper tatsächlich die Hämostase unter Bedingungen wiederherstellen, unter denen ansonsten keine Blutstillung möglich ist. Dies weist auf eine Unterstützung der Hämostase durch Verbesserung der Thrombin-abhängigen Fibrinbildung hin.“ ergänzt Dr. Sarah Beck, Wissenschaftlerin am Würzburger Institut für Experimentelle Biomedizin und Erstautorin der Studie. „Eine Anti-GPV-Behandlung könnte großes klinisches Potential haben und ist ein Ansatzpunkt, den wir in Zukunft näher verfolgen werden.“
Wissenschaftliche Ansprechpartner:
Prof. Dr. Bernhard Nieswandt (Rudolf-Virchow-Zentrum, Universität Würzburg)
Tel.: + 49 931 31-80405, bernhard.nieswandt(at)virchow.uni-wuerzburg.de
Originalpublikation:
Sarah Beck, Patricia Öftering, Renhao Li, Katherina Hemmen, Magdolna Nagy, Yingchun Wang, Alessandro Zarpellon, Michael K. Schuhmann, Guido Stoll, Zaverio M. Ruggeri, Katrin G. Heinze, Johan W.M. Heemskerk, Wolfram Ruf, David Stegner, Bernhard Nieswandt: Platelet glycoprotein V spatio-temporally controls fibrin formation. Nature Cardiovascular Research (April 2023) DOI: 10.1038/s44161-023-00254-6; URL: https://www.nature.com/articles/s44161-023-00254-6
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Neues Wirkprinzip gegen Tuberkulose
Gemeinsam ist es Forschenden der Heinrich-Heine-Universität Düsseldorf (HHU) und der Universität Duisburg-Essen (UDE) gelungen, eine Gruppe von Molekülen zu identifizieren und zu synthetisieren, die auf neue Art und Weise gegen…

Gefahr durch Weltraumschrott
Neue Ausgabe von „Physikkonkret“ beleuchtet Herausforderungen und Lösungen für eine nachhaltige Nutzung des Weltraums. Die Deutsche Physikalische Gesellschaft (DPG) veröffentlicht eine neue Ausgabe ihrer Publikationsreihe „Physikkonkret“ mit dem Titel „Weltraumschrott:…

Wasserstoff: Versuchsanlage macht Elektrolyseur und Wärmepumpe gemeinsam effizient
Die nachhaltige Energiewirtschaft wartet auf den grünen Wasserstoff. Neben Importen braucht es auch effiziente, also kostengünstige heimische Elektrolyseure, die aus grünem Strom Wasserstoff erzeugen und die Nebenprodukte Sauerstoff und Wärme…





















