Proteinfunktionen – Ein Lichtblitz genügt
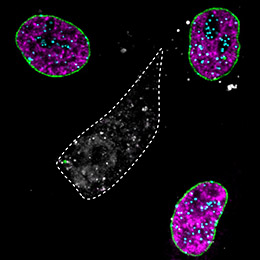
Bei der mittleren Zelle (grau) wurden gezielt gleich drei verschiedene Protein entfernt, ein Protein der Zellkernhülle (Lamin A, grün), ein Chromatinprotein (CENPA, türkis) und das Replikationsprotein (PCNA, magenta). Bild: Dr. Wen Deng, LMU
Proteine sind zentrale Bestandteile jeder Zelle. Alle grundlegenden Prozesse des Lebens, etwa Zellteilung, Wachstum und Stoffwechsel, aber auch die Entstehung von Krankheiten, werden durch zelluläre Proteine kontrolliert.
Um diese Prozesse umfassend zu verstehen, sind Untersuchungen zur Funktion der beteiligten Proteine unerlässlich. Um die Rolle eines Proteins zu analysieren, beobachten Forscher, was sein Verlust bewirkt. Dazu wird im Experiment häufig das entsprechende Gen mutiert oder ganz ausgeschaltet.
Bei lebenswichtigen Proteinen ist dieser Ansatz jedoch nicht möglich, da die Zellen dann absterben, bevor sich funktionelle Studien durchführen lassen. LMU-Wissenschaftler um Professor Heinrich Leonhardt vom Biozentrum der LMU haben nun ein Werkzeug entwickelt, das dieses Hindernis umgeht:
Ihre neue Methode setzt direkt an den Proteinen an, indem sie deren gezielten und kurzfristigen Abbau ermöglicht – steuerbar mit Licht oder Chemikalien. Über ihre Ergebnisse berichten die Wissenschaftler im Fachmagazin Nature Communications.
„Für die Entwicklung dieser Technologie haben wir die zelluläre Müllabfuhr für unsere Zwecke umprogrammiert“, sagt Leonhardt. Defekte oder nicht mehr benötigte Proteine werden in der Zelle mit dem Molekül Ubiquitin verknüpft. Die zelluläre Abbaumaschinerie für Proteine, das Proteasom, erkennt diese Markierung und zerlegt die ausgemusterten Proteine in ihre Einzelteile.
Diesen Mechanismus nutzen die Wissenschaftler, indem sie Ubiquitin mithilfe spezifischer Antikörperfragmente, sogenannter Nanobodies, an die Zielproteine heften – diese also dem zellulären Schredder ausliefern.
Um steuern zu können, ob und wann ein Zielmolekül markiert und abgebaut wird, haben die Wissenschaftler einen zusätzlichen Schalter eingebaut. Erst wenn die Wissenschaftler diesen Schalter durch Licht oder kleine chemische Moleküle aktivieren, wird das Zielmolekül markiert.
„Auf diese Weise können wir gezielt einzelne Proteine zeitlich und räumlich wie mit einem Dimmer stufenlos regulieren, das heißt jede gewünschte Konzentration einstellen und die Auswirkung auf zelluläre Prozesse beobachten“, sagt Leonhardt.
Als eine erste Anwendung untersuchten die Wissenschaftler ein Protein, das bei der DNA-Replikation eine zentrale Rolle spielt und deshalb nicht genetisch ausgeschaltet werden kann. „Wir haben dieses Protein mit unseren Werkzeugen vorübergehend entfernt und konnten so dessen Rolle bei der DNA-Reparatur untersuchen“, sagt Wen Deng, der Erstautor der Studie.
Dabei zeigte sich, dass das Protein eine zentrale Andockstation für andere an der Reparatur beteiligte Proteine darstellt und damit sicherstellt, dass DNA-Schäden in der Zelle effizient repariert werden.
Ein weiterer Vorteil des neuen Werkzeugs ist, dass es auch in ganzen Organismen angewendet werden kann. Im Fadenwurm C. elegans beispielsweise, einem Modellorganismus der Biologie, gelang es den Wissenschaftlern in Kooperation mit der Arbeitsgruppe von Professor Barbara Conradt (University College London), einen wichtigen Schritt des programmierten Zelltods zu untersuchen.
Während der Entwicklung dieses Wurms stirbt bei bestimmten Zellteilungen jeweils eine der zwei Tochterzellen. „Durch den gezielten Abbau des dafür verantwortlichen Exekutionsproteins konnten wir den Tod der Tochterzelle verhindern und so neue Einsichten in diesen Prozess gewinnen“, sagt Leonhardt.
Da das Ubiquitin-Proteasom-System sowohl in allen höheren Organismen als auch in Archaeen und einigen Bakterien existiert, gehen die Wissenschaftler davon aus, dass ihr Instrumentarium zum künstlich gesteuerten Proteinabbau breit einsetzbar sein wird und einen wichtigen Beitrag dazu liefern kann, insbesondere die Funktion von lebenswichtigen Proteinen zu untersuchen.
Prof. Dr. Heinrich Leonhardt
BioSysM
Tel. +49 (0)89 2180-74232
h. leonhardt@lmu.de
Tunable light and drug induced depletion of target proteins
Wen Deng, Jack A. Bates, Hai Wei, Michael D. Bartoschek, Barbara Conradt & Heinrich Leonhardt
Nature Communications 2020
https://www.nature.com/articles/s41467-019-14160-8
Media Contact
Weitere Informationen:
https://www.uni-muenchen.de/forschung/news/2020/leonhardt_werkzeug.htmlAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Neues Wirkprinzip gegen Tuberkulose
Gemeinsam ist es Forschenden der Heinrich-Heine-Universität Düsseldorf (HHU) und der Universität Duisburg-Essen (UDE) gelungen, eine Gruppe von Molekülen zu identifizieren und zu synthetisieren, die auf neue Art und Weise gegen…

Gefahr durch Weltraumschrott
Neue Ausgabe von „Physikkonkret“ beleuchtet Herausforderungen und Lösungen für eine nachhaltige Nutzung des Weltraums. Die Deutsche Physikalische Gesellschaft (DPG) veröffentlicht eine neue Ausgabe ihrer Publikationsreihe „Physikkonkret“ mit dem Titel „Weltraumschrott:…

Wasserstoff: Versuchsanlage macht Elektrolyseur und Wärmepumpe gemeinsam effizient
Die nachhaltige Energiewirtschaft wartet auf den grünen Wasserstoff. Neben Importen braucht es auch effiziente, also kostengünstige heimische Elektrolyseure, die aus grünem Strom Wasserstoff erzeugen und die Nebenprodukte Sauerstoff und Wärme…





















