Genexpression in Mitochondrien gezielt verändern
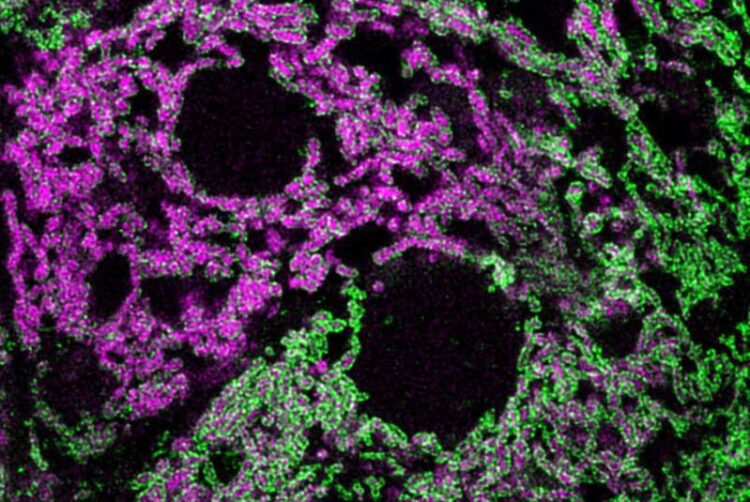
Die Abbildung zeigt Hepatozyten der Maus, in denen der Prozess der mitochondrialen Translation innerhalb der von der Mitochondrienmembran (grün) umschlossenen Mitochondrienmatrix sichtbar ist (magenta).
R. Yousefi, Institut für Zellbiochemie, UMG
Göttinger Wissenschaftler*innen des Exzellenzclusters Multiscale Bioimaging (MBExC) und des Sonderforschungsbereichs 1190 entwickeln neue Strategie zur Untersuchung der Genexpression in Mitochondrien. Veröffentlicht im Wissenschaftsjournal „Cell“.
Mitochondrien gelten als die Kraftwerke der Zellen, da sie mit Hilfe von Sauerstoff Energie aus unserer Nahrung erzeugen. Die dafür notwendige Maschinerie wird als Atmungskette bezeichnet. Deren zentralen Bausteine werden von Mitochondrien selbst durch die Expression von Genen des ihnen eigenen Erbguts gebildet. Störfälle bei der Genexpression können die Energieproduktion aus dem Gleichgewicht bringen und schwere Erkrankungen des Nervensystems und des Herzens verursachen, die häufig tödlich verlaufen. Wie genau die Genexpression in den Mitochondrien abläuft, ist weitgehend nicht verstanden.
Göttinger Grundlagenforscher um Prof. Dr. Peter Rehling, Direktor des Instituts für Zellbiochemie an der Universitätsmedizin Göttingen (UMG), Sprecher des Sonderforschungsbereichs SFB 1190 „Transportmaschinen und Kontaktstellen zellulärer Kompartimente“ und Mitglied des Göttinger Exzellenzclusters „Multiscale Bioimaging: Von Molekularen Maschinen zu Netzwerken erregbarer Zellen“ (MBExC) sind nun einen Schritt weiter. Sie haben eine neue Methode entwickelt, die es zum ersten Mal erlaubt, die Proteinbildung in den Kraftwerken experimentell zu verändern. Die dadurch gewonnenen Erkenntnisse ermöglichen auch Rückschlüsse auf die Entstehung „Mitochondrialer Erkrankungen“. Die Technik wurde kürzlich in der renommierten Fachzeitschrift „Cell“ veröffentlicht.
Originalveröffentlichung: An in vitro system to silence mitochondrial gene expression. Cruz-Zaragoza LD, Dennerlein S, Linden A,Yousefi R, Lavdovskaia E, Aich A Falk RR, Gomkale R, Schöndorf T, Bohnsack MT, Richter-Dennerlein R, Urlaub H, Rehling P (2021) Cell, 184, 1-14. doi: 10.16/j.cell.2021.09.033.
Forschung im Detail
Im Prozess der mitochondrialen Genexpression regulieren vielfältige Faktoren die Bildung von Proteinen (Translation) für die Atmungskette. Störungen in diesem Prozess werden mit einer Vielzahl von Krankheiten in Verbindung gebracht, darunter Herz-Kreislauf-Erkrankungen und Erkrankungen des Nervensystems. „Um Ansätze entwickeln zu können, mit denen sich krankheitsrelevante Störungen verhindern lassen, müssen wir zunächst die molekularen Mechanismen der Genexpression in Mitochondrien verstehen. Dafür sind reduktionistische Ansätze unverzichtbare Werkzeuge“, sagt Prof. Rehling, Seniorautor der Publikation. „Sie ermöglichen es uns, biologische Prozesse auf verschiedenen Ebenen zu zerlegen und auf diese Weise die Funktion einzelner beteiligter Komponenten zu untersuchen.“ Solche experimentellen Strategien fehlten bisher. Ein Haupthindernis für ihre Entwicklung liegt in der Tatsache, dass Mitochondrien nicht ohne Weiteres genetisch zugänglich sind. Um dieses Problem zu lösen, haben die Göttinger Wissenschaftler*innen eine völlig neue Technik entwickelt: Sie erlaubt es ihnen, die Translation in gereinigten Mitochondrien gezielt zu verändern. Durch die Verwendung kleinster Mengen eines modifizierten mitochondrialen Vorläuferproteins, das sie effizient in gereinigte menschliche Mitochondrien einschleusen, gelingt es ihnen, die Bildung einzelner Proteine in den Mitochondrien zu verhindern. „Mit Hilfe dieses in vitro Systems können wir nun untersuchen, wie sich der Verlust der Expression einer einzelnen mRNA auf die Physiologie und Organisation von Mitochondrien auswirkt, und das mit minimalem indirekten Einfluss auf andere Prozesse“, sagt Dr. Luis Daniel Cruz-Zaragoza, Wissenschaftler am Institut für Zellbiochemie, UMG, und Erstautor der Studie. Mehr noch: Die Wissenschaftler*innen konnten die Technik auch leicht auf gereinigte Mitochondrien von Mäusen übertragen, ein Hinweis darauf, dass sie auch im Kontext von Krankheitsmodellen anwendbar ist. Diese neue experimentelle Strategie ist also auch für die klinische Forschung bedeutsam. Störungen in der mitochondrialen Genexpression können schwere Erkrankungen des Nervensystems und des Herzens zur Folge haben, die häufig tödlich verlaufen.
Das Göttinger Exzellenzcluster 2067 Multiscale Bioimaging: Von molekularen Maschinen zu Netzwerken erregbarer Zellen (MBExC)
Das Göttinger Exzellenzcluster 2067 Multiscale Bioimaging: Von molekularen Maschinen zu Netzwerken erregbarer Zellen (MBExC) wird seit Januar 2019 im Rahmen der Exzellenzstrategie des Bundes und der Länder gefördert. Mit einem einzigartigen interdisziplinären Forschungsansatz untersucht MBExC die krankheitsrelevanten Funktionseinheiten elektrisch aktiver Herz- und Nervenzellen, von der molekularen bis hin zur Organebene. Hierfür vereint MBExC zahlreiche universitäre und außeruniversitäre Partner*innen am Göttingen Campus. Das übergeordnete Ziel: den Zusammenhang von Herz- und Hirnerkrankungen zu verstehen, Grundlagen- und klinische Forschung zu verknüpfen und damit neue Therapie- und Diagnostikansätze mit gesellschaftlicher Tragweite zu entwickeln.
Weitere Informationen
über Rehling Lab: https://biochemie.uni-goettingen.de
über MBExC: https://mbexc.de/
Weitere Informationen / Ansprechpartner:
Universitätsmedizin Göttingen, Georg-August-Universität Göttingen
Institut für Zellbiochemie
Prof. Dr. Peter Rehling
Humboldtallee 23, 37073 Göttingen
Telefon 0551 / 39-5947
E-Mail: peter.rehling@medizin.uni-goettingen.de
Exzellenzcluster Multiscale Bioimaging (MBExC)
Dr. Heike Conrad (Kontakt – Pressemitteilung)
Telefon 0551 / 39-61305
E-Mail: heike.conrad@med.uni-goettingen.de
Wissenschaftliche Ansprechpartner:
Universitätsmedizin Göttingen, Georg-August-Universität Göttingen
Institut für Zellbiochemie
Prof. Dr. Peter Rehling
Humboldtallee 23, 37073 Göttingen
Telefon 0551 / 39-5947
E-Mail: peter.rehling@medizin.uni-goettingen.de
Originalpublikation:
Originalveröffentlichung: An in vitro system to silence mitochondrial gene expression. Cruz-Zaragoza LD, Dennerlein S, Linden A,Yousefi R, Lavdovskaia E, Aich A Falk RR, Gomkale R, Schöndorf T, Bohnsack MT, Richter-Dennerlein R, Urlaub H, Rehling P (2021) Cell, 184, 1-14. doi: 10.16/j.cell.2021.09.033.
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















