Erstes künstliches Gewebemodell entwickelt, in dem Blutgefäße wachsen
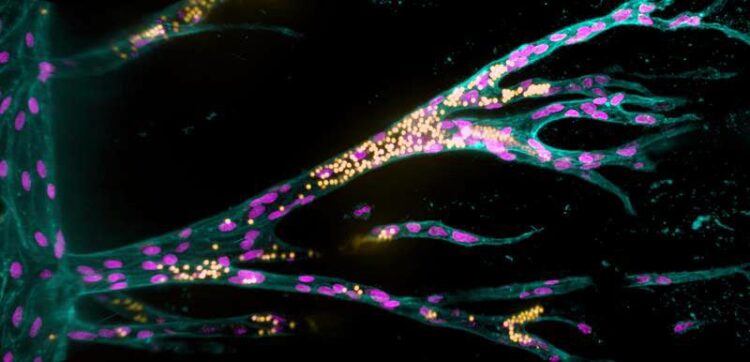
Growing from a parent blood vessel (upright on the left), endothelial cells (pink nuclei) form new blood vessels in a synthetic hydrogel. The fluorescent beads (yellow) simulate blood flow.
(c) Jifeng Liu, MPI Münster / Liu et al./Nat Comm 2021
Forscher um die Biomedizin-Ingenieurin Dr. Britta Trappmann vom Max-Planck-Institut für molekulare Biomedizin in Münster haben ein Zellkultursystem entwickelt, in dem sich erstmals in einem Gerüst aus künstlichen Materialien ein funktionsfähiges Blutgefäßsystem bildet. Das Team untersucht, welche Materialeigenschaften einzelne Parameter der Gefäßbildung fördern – ein Schritt auf dem Weg zur Zukunftsvision implantierbarer künstlicher Gewebe. Die Studie ist in der Fachzeitschrift „Nature Communications“ erschienen.
Im Labor Gewebe herzustellen, mit denen sich geschädigte Organe heilen oder ersetzen lassen, ist eine der großen Zukunftsvisionen der Medizin. Künstliche Materialien könnten sich als Gewebegerüste eignen, denn anders als natürliches Gewebe bleiben sie im Organismus lange genug stabil, so dass der Körper neue natürliche Strukturen ausbilden kann. Eine grundlegende Voraussetzung für funktionsfähige Gewebe ist, dass in ihnen Blutgefäße wachsen und sich mit dem Gefäßsystem des Organismus verbinden können, so dass das Gewebe durchblutet und mit Sauerstoff und Nährstoffen versorgt wird. Bisher ist allerdings fast nichts darüber bekannt, welche Materialeigenschaften das Wachstum von Blutgefäßen fördern.
Ein Team um die Biomedizin-Ingenieurin Dr. Britta Trappmann vom Max-Planck-Institut für molekulare Biomedizin in Münster hat jetzt ein Zellkultursystem entwickelt, in dem sich zum ersten Mal in einem Gerüst aus künstlichen Materialien ein funktionsfähiges Blutgefäßsystem bildet. Die Wissenschaftlerinnen und Wissenschaftler arbeiteten mit einem speziellen Hydrogel, dessen Eigenschaften sie kontrolliert verändern können, und ließen darin ein Ursprungsblutgefäß aus menschlichen Blutgefäßzellen wachsen. Sie untersuchten, wie die Materialeigenschaften der künstlichen Zellumgebung die Bildung weiterer Blutgefäße beeinflussten, und stimmten diese fein aufeinander ab. Ihre wichtigsten Erkenntnisse: „Das künstliche Gewebematerial muss bestimmte Adhäsionsmoleküle in der Membran von Blutgefäßzellen aktivieren, damit die Zellen in Gruppen aus dem Ursprungsgefäß auswandern und röhrenförmige Strukturen bilden – gleichzeitig muss das Material für die Blutgefäßzellen schnell genug abbaubar sein, damit sie Gefäße in ausreichender Größe formen können“, erklärt Britta Trappmann. Um sich an die natürliche Umgebung von Zellen anzunähern, müssten in weiteren Schritten zahlreiche weitere Biomoleküle und Zellen in das Modellsystem integriert werden, beispielsweise Signalproteine, Immunzellen oder die Blutgefäße stabilisierende Zellen. „Die Wirkung all dieser Faktoren ist in natürlichem Gewebe zudem gekoppelt und von Organ zu Organ unterschiedlich“, ergänzt die Wissenschaftlerin. All das zu verstehen, sei ein Fernziel. Das Wissen könnte man dann nutzen, um implantierbare Gewebe zu entwickeln.
Britta Trappmann und ihr Team arbeiteten bei ihren Untersuchungen mit Kollegen an der Universität Münster sowie Arbeitsgruppen aus München und North Carolina zusammen. Die Studie ist in der Fachzeitschrift „Nature Communications“ erschienen.
Details zu Methoden und Ergebnissen:
Dreidimensionales Gewebegerüst aus Hydrogel
Für ihre Untersuchungen bauten die Forschenden auf einem Modellsystem auf, das Britta Trappmann während ihrer Zeit als Postdoktorandin in den USA an der Boston und Harvard University gemeinsam mit Kolleginnen und Kollegen entwickelt hatte. Es besteht aus einem dreidimensionalen Hydrogel auf Zuckerbasis, in das die Wissenschaftler mit einer Akkupunkturnadel zwei Kanäle stechen. Diese haben jeweils einen Durchmesser von 400 Mikrometern und verlaufen im Abstand von etwa einem Millimeter parallel zueinander. In dem einen Kanal säen die Wissenschaftler Endothelzellen aus, die auch in natürlichen Geweben die Blutgefäße auskleiden. „Die Endothelzellen bilden untereinander Kontakte, heften sich in dem Kanal an ihre künstliche Gewebeumgebung und formen so nach etwa einem Tag ein Ursprungsblutgefäß“, erklärt Britta Trappmann. Wenn es soweit ist, schicken die Wissenschaftler durch den zweiten Kanal einen Wachstumsfaktorcocktail – dies sind Moleküle, die auch in natürlichen Geweben das Blutgefäßwachstum vorantreiben – woraufhin die Endothelzellen in das Hydrogel einwandern.
Moleküle in der Zellmembran setzen die Blutgefäßbildung in Gang
Die Wissenschaftler wollten nun herausfinden, welche Eigenschaften des Hydrogels bestimmen, ob die wandernden Endothelzellen wirklich neue Blutgefäße bilden. Sie untersuchten, welche Rolle die Aktivierung von sogenannten Adhäsionsmolekülen in der Membran der Zellen spielt, durch die sich Zellen an die Umgebung anheften können. Die Forscher reicherten das Gewebegerüst aus Hydrogel zunächst mit unterschiedlichen Mengen von Peptiden an, die einen bestimmten Typ von Adhäsionsmolekülen in der Membran von Endothelzellen aktivieren – die Integrine.
Je höher die Konzentration der Peptide war, desto mehr Endothelzellen wanderten in Gruppen durch das Hydrogel. Blockierten die Wissenschaftler die Integrinfunktion, beobachteten sie hingegen, dass die Zellen nur einzeln migrierten. In einem weiteren Schritt untersuchte das Team dies für zwei Integrin-Subtypen. „Wir haben herausgefunden, dass Integrin αvβ3 das entscheidende Adhäsionsmolekül ist, das aktiviert werden muss, damit die Endothelzellen in Gruppen auswandern“, erzählt Britta Trappmann. Die Wissenschaftler zeigten auch, dass die kollektive Zellwanderung wiederum Voraussetzung dafür ist, dass die Endothelzellen im nächsten Schritt – nach einer Kulturzeit von etwa zwei Wochen – Hohlräume formen, die mit dem Ursprungsgefäß verbunden sind.
Zellen brauchen Bewegungsfreiheit, um ausreichend große Blutgefäße zu bilden
Zwar bildeten die Blutgefäßzellen nun röhrenförmige Strukturen, diese waren allerdings kleiner als bei natürlichem Gewebe, was sich – so die Hypothese der Wissenschaftler – möglicherweise dadurch erklären ließ, dass das künstliche Hydrogel im Vergleich zu natürlichem Gewebe weniger abbaubar ist und kleinere Poren hat, durch die Zellen hindurchschlüpfen können. Ihre Lösung: Das Hydrogel besteht aus Zuckermolekülketten, die durch bestimmte Moleküle miteinander vernetzt sind. Die Wissenschaftler tauschten diese Vernetzermoleküle aus, so dass die Zellen das Hydrogel durch von ihnen freigesetzte Enzyme schneller spalten und somit schneller migrieren konnten, wodurch sie größere Gefäßstrukturen bildeten.
Förderung
Die Studie erhielt finanzielle Unterstützung durch die Max-Planck-Gesellschaft sowie Forschungsverbünde der Westfälischen Wilhelms-Universität Münster – dazu gehören die von der Deutschen Forschungsgemeinschaft geförderten Sonderforschungsbereiche 1348 „Dynamische zelluläre Grenzflächen“ und 1009 „Breaking Barriers“ sowie das Forschungsnetzwerk „Cells in Motion“.
Links
Originalpublikation in „Nature Communications“
https://www.nature.com/articles/s41467-021-23644-5
Forschungsgruppe Dr. Britta Trappmann am Max-Planck-Institut für molekulare Biomedizin in Münster
https://www.mpi-muenster.mpg.de/229324/trappmann
Dr. Britta Trappmann am Cells in Motion Interfaculty Centre der Universität Münster
https://www.uni-muenster.de/Cells-in-Motion/de/people/all/trappmann-b.php
Forschungsschwerpunkt „Zelldynamik und Bildgebung“ an der WWU
https://www.uni-muenster.de/forschung/profil/schwerpunkt/zelldynamik.html
Wissenschaftliche Ansprechpartner:
Dr. Britta Trappmann, Max-Planck Forschungsgruppenleiterin
Max-Planck-Institut für molekulare Biomedizin
britta.trappmann@mpi-muenster.mpg.de
Weitere Kontaktperson:
Doris Niederhoff, Referentin für Wissenschaftskommunikation
Cells in Motion Interfaculty Centre, Münster
+49 251 83-49315
doris.niederhoff@uni-muenster.de
Originalpublikation:
Liu J, Long H, Zeuschner D, Räder AFB, Polacheck WJ, Kessler H, Sorokin L, Trappmann B. Synthetic extracellular matrices with tailored adhesiveness and degradability support lumen formation during angiogenic sprouting. Nat Commun 2021 Jun 7;12(1):3402. doi: 10.1038/s41467-021-23644-5.
Link: https://www.nature.com/articles/s41467-021-23644-5
Weitere Informationen:
https://www.mpi-muenster.mpg.de/643779/20210727-hydrogel-tissue-for-blood-vessel…
https://www.uni-muenster.de/Cells-in-Motion/de/newsviews/2021/07-27.html
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Neues Wirkprinzip gegen Tuberkulose
Gemeinsam ist es Forschenden der Heinrich-Heine-Universität Düsseldorf (HHU) und der Universität Duisburg-Essen (UDE) gelungen, eine Gruppe von Molekülen zu identifizieren und zu synthetisieren, die auf neue Art und Weise gegen…

Gefahr durch Weltraumschrott
Neue Ausgabe von „Physikkonkret“ beleuchtet Herausforderungen und Lösungen für eine nachhaltige Nutzung des Weltraums. Die Deutsche Physikalische Gesellschaft (DPG) veröffentlicht eine neue Ausgabe ihrer Publikationsreihe „Physikkonkret“ mit dem Titel „Weltraumschrott:…

Wasserstoff: Versuchsanlage macht Elektrolyseur und Wärmepumpe gemeinsam effizient
Die nachhaltige Energiewirtschaft wartet auf den grünen Wasserstoff. Neben Importen braucht es auch effiziente, also kostengünstige heimische Elektrolyseure, die aus grünem Strom Wasserstoff erzeugen und die Nebenprodukte Sauerstoff und Wärme…





















