Die Verpackung macht’s!
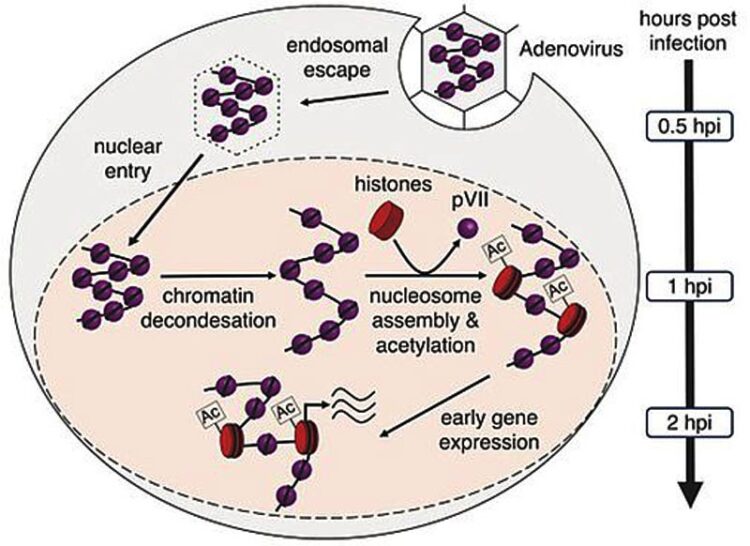
Das Genom des Adenovirus ist spezifisch verpackt mit dem viralen Protein pVII. Nach dem Eindringen des Virus in die Zelle wird das Genom aus der Virushülle freigesetzt und in den Zellkern transportiert. Bevor die virale Information abgelesen werden kann, wird Protein pVII gezielt an regulatorisch wichtigen Stellen des viralen Genoms, durch zelluläre Verpackungsproteine (Histone) ausgetauscht. Nach der chemischen Modifikation der Histone (Azetylierung), wird die zelluläre Maschinerie zum Auslesen der viralen Information gekapert und das Virus kann sich vermehren. Grafik © Dr. Uwe Schwartz
Wie ein Virus seine DNA-Verpackung verändert, um in der menschlichen Zelle aktiv zu werden.
Die DNA ist das Erbmolekül, das die genetische Information der Menschen trägt. Das Molekül mit einer Länge von etwa zwei Metern befindet sich im Zellkern jeder einzelnen Zelle — und das, obwohl Zellkerne einen Durchmesser von nur einem Millionstel Meter haben. Damit diese dünnen DNA-Fäden in den Zellkern passen, werden sie auf molekularen Spulen, bestehend aus Histonproteinen, aufgewickelt und kompaktiert. Die Histone und die Art der DNA-Verpackung sind für den Zugang zum DNA-Code und somit für die Funktion in der Zelle von entscheidender Bedeutung.
Die DNA der Adenoviren ist im Gegensatz zur DNA in humanen Zellen nicht auf Histonproteine aufgewickelt. Stattdessen wird die virale DNA durch das spezifische Virusprotein pVII gebunden. Dieses pVII-DNA System ist allerdings nicht kompatibel mit der menschlichen DNA-Verpackung. Lange war unklar, wie die Information der viralen DNA während der Infektion in der menschlichen Zelle zugänglich gemacht wird.
Dieses Wissen hat allerdings zentrale wissenschaftliche Bedeutung, um die Vermehrung von Viren in den Wirtszellen und die Auslösung von Krankheiten zu verstehen. Darüber hinaus spielt es auch in der angewandten Forschung eine große Rolle, da Adenoviren als Plattform für Gentherapien verwendet werden. Dies wird durch zwei Eigenschaften dieser Viren ermöglicht: Zum einen, dass Adenoviren humane Zellen infizieren, aber nur eine geringe Pathogenität, also geringe Fähigkeit zur Krankheitserregung, besitzen. Zum anderen, dass Adenoviren genetisch manipuliert werden können. Während der Corona Pandemie wurde dies erfolgreich genutzt — so wurden Adenoviren zur Vakzinierung gegen den SARS-CoV2 Virus eingesetzt.
Forscher*innen der Universität Regensburg und der Universität Bordeaux haben unter der Leitung von Prof. Dr. Gernot Längst, Biochemie Zentrum Regensburg, die frühe Infektion menschlicher Zellen mit Adenoviren mittels hochauflösender Mikroskopie und Genomstruktur-Analysen zeitlich verfolgt. Die Untersuchungen lieferten detaillierte Einblicke in die Verpackung des Virus mit dem pVII-Protein. Nach der Infektion wird die Organisation der Virenverpackung auf dem Weg von der Zelloberfläche in den Zellkern dynamisch verändert, um das Auslesen der viralen Information zu ermöglichen.
Im Virus ist die DNA eng um das pVII-Protein herumgewickelt, um in das kleine Viruskapsid zu passen. Nach dem Eindringen in die Zelle wird die verpackte DNA innerhalb von ca. 30 Minuten aus dem Kapsid freigesetzt und in den Zellkern importiert. Im Zellkern angekommen, wird die kompaktierte Virus-DNA aufgelockert. Dabei werden wenige pVII-Proteine gezielt an den regulatorischen Stellen der früh zu aktivierenden Gene entfernt und durch menschliche Histonproteine ersetzt.
Das Ersetzen der viralen Verpackungsproteine durch die humanen Histone ermöglicht erst das Auslesen der viralen DNA durch die menschliche Zelle — ein Prozess, der etwa eine Stunde nach Aufnahme der viralen DNA in die Zellen beginnt.
Das Verständnis der dynamischen Reorganisation ermöglicht einen grundlegenden Einblick in die Mechanismen der viralen Genaktivierung in infizierten Zellen. Dieses Wissen kann das Design und die Herstellung von optimierten Adenoviren ermöglichen: Viren, die als sichere und präzisere Vakzine oder Gentherapeutika angewendet werden können. Zwei medizinische Bereiche, die auch in der Zukunft eine zentrale Rolle spielen werden.
Diese Studie wurde kürzlich in der renommierten Fachzeitschrift European Molecular Biology Organization Journal (EMBO J) publiziert.
Wissenschaftliche Ansprechpartner:
Prof. Gernot Längst
Biochemie Zentrum Regensburg
Universität Regensburg
E-Mail: gernot.laengst@ur.de
Prof. Harald Wodrich
Microbiologie Fondamentale et Pathogénicité,
Universität Bordeaux, Frankreich
E-Mail: harald.wodrich@u-bordeaux.fr
Originalpublikation:
“Changes in adenoviral chromatin organization precede early gene activation upon infection”, Schwartz, U.; Komatsu, T.; Huber, C.; Lagadec, F.; Baumgartl, C.; Silberhorn E.; Nützel M.; Rayne, F.; Basyuk E.; Bertrand E.; Rehli M.; Wodrich H.; Längst, G.; The EMBO Journal (2023) e114162.
https://doi.org/10.15252/embj.2023114162
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Robotisch assistiertes Laserverfahren soll OP-Risiken minimieren
Eine Spinalkanalstenose – eine knöcherne Verengung des Wirbelkanals – kann für Betroffene zur Qual werden. Drückt sie auf das Rückenmark, drohen ihnen chronische Schmerzen und Lähmungserscheinungen. Häufig hilft dann nur…

Verbesserte Materialien für die Verbindungen von Mikrochips
Leistungsfähiger, stromsparender, komplexer – Hersteller von modernen Microchips sehen sich stetig neuen Herausforderungen gegenüber, auch in Bezug auf die dort notwendigen elektrischen Verbindungen. Das Fraunhofer IPMS und BASF widmen sich…

Inspiriert von der Natur: Biophysiker aus dem Projekt InCamS@BI entwickelt neuartige Mikroplastikfilter im Labor
Heutzutage ist es überall zu finden: Mikroplastik. Es wird insbesondere durch die Luft und durchs Wasser in die entlegensten Winkel der Erde transportiert. Eine der großen Fragen lautet: Wie können…



