Brückenantikörper mit Verstärker kann Brustkrebszellen zerstören

Fluroeszenzmikroskopie von Brustkrebs-Organoiden: Krebszellen fluoreszieren blau, T-Zellen grün: Nur wenn Brücken- und Verstärkerantikörper am Organoid zusammenwirken, ist eine erhebliche Aktivierung der T-Zellen zu beobachten. Die T-Zellen wandern in das Organoid ein und die Krebszellen sterben weitgehend ab (rot). | © Momburg/DKFZ
Wissenschaftler vom Deutschen Krebsforschungszentrum haben Antikörper entwickelt, die zwei Antigenbindestellen besitzen und Krebszellen mit Zellen der Immunabwehr koppeln können. In Laborversuchen waren diese Brückenantikörper zusammen mit einem Verstärker-Antikörper in der Lage, die körpereigene Immunabwehr gezielt zu mobilisieren und Brustkrebszellen zu zerstören.
Seit einigen Jahren bereichern bispezifische Antikörper (BiMAb: bispecific monoclonal antibodies) die Krebsimmuntherapie. Das sind Antikörper, die zwei verschiedene Antigenbindestellen besitzen. Mit der einen docken sie an ein tumorspezifisches Molekül auf Krebszellen an. Mit der anderen heften sie sich an ein Antigen, das auf der Oberfläche von Immunabwehrzellen lokalisiert ist. Durch die Brückenfunktion der bispezifischen Antikörper werden Krebs- und Abwehrzelle miteinander in physischen Kontakt gebracht, so dass das Immunsystem den Tumor gezielt angreifen kann und ihn im Idealfall schließlich zerstört.
Im Kampf gegen Blutkrebs haben sich BiMAb bereits in bestimmten Erkrankungssituationen als hochgradig wirksam erwiesen. Experimente zur Bekämpfung solider Tumoren wie Brustkrebs, schwarzer Hautkrebs oder Knochenkrebs waren dagegen bisher weniger erfolgreich.
Forschern des Deutschen Krebsforschungszentrums unter der Leitung von Frank Momburg ist es zusammen mit einer Arbeitsgruppe von Dirk Jäger, Nationales Centrum für Tumorerkrankungen (NCT) Heidelberg, gelungen, BiMAb zu entwickeln, die in der Zellkulturschale gezielt die Immunabwehr aktivieren. Selbst an millimetergroßen kugeligen Zellverbänden aus Brustkrebszellen, so genannten Organoiden, konnten die Wissenschaftler diesen Effekt erzielen.
Sie konstruierten dazu eine Reihe von Antikörpervarianten, die sich jeweils gegen ein für Brustkrebs charakteristisches Antigen richteten und außerdem gegen das T-Zell-Molekül CD3. Die Bindung der Antikörper regte die T-Zellen dazu an, Botenstoffe auszuschütten, und aktivierte zellabtötende Mechanismen. „Die Kunst dabei ist es, bispezifische Antikörper gegen Tumorantigene und CD3 herzustellen, die so selektiv sind, dass sie ausschließlich am Tumorgewebe wirken, nicht aber das umliegende gesunde Gewebe angreifen“, erklärt Momburg. „Das ist nicht trivial, da viele Tumorantigene in geringem Maße auch in gesundem Gewebe vorkommen.“
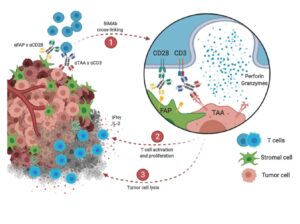
© Warwas/DKFZ
Eine weitere Schwierigkeit besteht darin, dass Zellen solider Tumoren anders als Blutkrebszellen für Antikörper physisch schwer zugänglich sind. Außerdem wirkt das Milieu, das die Tumoren umgibt, meist immunsuppressiv, was die Abwehrmechanismen zusätzlich ausbremst. Um diesen Herausforderungen zu begegnen und die T-Zellantwort am Tumor zu verstärken, verwendeten Karsten Warwas und Kollegen zusätzliche bispezifische Antikörper, die den Kontakt zwischen weiteren Molekülpaaren auf der Tumor- und der T-Zelle herstellen. Diese Verstärker-Antikörper aktivieren die T-Zellen nicht direkt, verstärken das Signal der aktivierenden BiMAbs jedoch durch „Ko-Stimulation“. Damit konnte die Dosis des T-Zell-aktivierenden BiMAb auf ein Minimum reduziert werden. Das kann in einer therapeutischen Situation helfen, toxische Nebenwirkungen von Antikörpern durch eine überschießende Ausschüttung von Botenstoffen zu vermeiden.
Die Laborexperimente mit Brustkrebs-Organoiden zeigten, dass die Kombination aus Brücken- und Verstärkerantikörper in der Lage war, T-Zellen gezielt zu mobilisieren, und zwar nur in Proben, in denen sich auch Krebszellen befanden, die das Tumorantigen trugen. „Die T-Zellaktivierung fand also nur dann statt, wenn beide Zelltypen – Tumorzellen und T-Zellen – in engem zeitlichen und räumlichen Abstand aufeinandertrafen. Das ist mit Blick auf eine spätere Anwendung am Menschen ein ganz entscheidender Sicherheitsaspekt“, so Momburg.
Die neue Methode kann möglicherweise einmal Anwendung in der Krebsimmuntherapie finden, muss jetzt aber zunächst noch weiter erprobt werden, bevor sie in klinische Studien Eingang findet. Frank Momburg erklärt: „In unserem Ansatz ergänzen sich stimulierende und kostimulierende BiMAb. Dieses Prinzip könnte für die Behandlung solider Tumoren mit spärlich ausgeprägten Tumorantigenen von Vorteil sein.“
Karsten M. Warwas, Marten Meyer, Márcia Goncalves, Gerhard Moldenhauer, Nasja Bulbuc, Susanne Knabe, Claudia Luckner-Minden; Claudia Ziegelmeier, Claus Peter Heussel, Inka Zörnig, Dirk Jäger und Frank Momburg: Co-Stimulatory Bispecific Antibodies Induce Enhanced T Cell Activation and Tumor Cell Killing in Breast Cancer Models.
Frontiers in Immunology 2021, https://doi.org/10.3389/fimmu.2021.719116.
Das Deutsche Krebsforschungszentrum (DKFZ) ist mit mehr als 3.000 Mitarbeiterinnen und Mitarbeitern die größte biomedizinische Forschungseinrichtung in Deutschland. Über 1.300 Wissenschaftlerinnen und Wissenschaftler erforschen im DKFZ, wie Krebs entsteht, erfassen Krebsrisikofaktoren und suchen nach neuen Strategien, die verhindern, dass Menschen an Krebs erkranken. Sie entwickeln neue Methoden, mit denen Tumoren präziser diagnostiziert und Krebspatienten erfolgreicher behandelt werden können. Beim Krebsinformationsdienst (KID) des DKFZ erhalten Betroffene, interessierte Bürger und Fachkreise individuelle Antworten auf alle Fragen zum Thema Krebs. Gemeinsam mit Partnern aus den Universitätskliniken betreibt das DKFZ das Nationale Centrum für Tumorerkrankungen (NCT) an den Standorten Heidelberg und Dresden, in Heidelberg außerdem das Hopp-Kindertumorzentrum KiTZ. Im Deutschen Konsortium für Translationale Krebsforschung (DKTK), einem der sechs Deutschen Zentren für Gesundheitsforschung, unterhält das DKFZ Translationszentren an sieben universitären Partnerstandorten. Die Verbindung von exzellenter Hochschulmedizin mit der hochkarätigen Forschung eines Helmholtz-Zentrums an den NCT- und den DKTK-Standorten ist ein wichtiger Beitrag, um vielversprechende Ansätze aus der Krebsforschung in die Klinik zu übertragen und so die Chancen von Krebspatienten zu verbessern. Das DKFZ wird zu 90 Prozent vom Bundesministerium für Bildung und Forschung und zu 10 Prozent vom Land Baden-Württemberg finanziert und ist Mitglied in der Helmholtz-Gemeinschaft Deutscher Forschungszentren.
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















