Netzwerkbildung im Gehirn trotz Sendepause
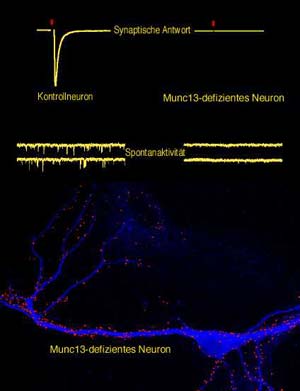
Abb.: Eine nicht mehr zur Transmitterfreisetzung fähige Nervenzelle in Kultur; Zellkörper und Fortsätze sind blau fluoreszierend dargestellt. Die elektrophysiologischen Messkurven im oberen Bildteil zeigen die totale Blockade der synaptischen Kommunikation in dieser Zellmutante (Munc13-defizientes Neuron) im Vergleich zu einem normalen Kontrollneuron. Die trotz dieser Blockade zahlreich angelegten Synapsen sind rot fluoreszierend dargestellt. <br> <br>Abb.: Max-Planck-Institut für biophysikalische Chemie <br>
Max-Planck-Wissenschaftler liefern neue Ergebnisse zur Gehirnentwicklung / Widerspruch zur bisherigen Lehrmeinung
Anhand aktueller Untersuchungen zur Gehirnentwicklung haben Wissenschaftler der Max-Planck-Institute für experimentelle Medizin sowie für biophysikalische Chemie in Göttingen den Nachweis erbringen können, dass sich auch bei kompletter Blockade der Nervenzellkommunikation normal strukturierte Netzwerke im Gehirn bilden. Mit ihrer jüngsten Publikation in der Ausgabe vom 25. Juni 2002 in den Proceedings of the National Academy of Sciences USA haben die Max-Planck-Forscher damit die bisher gängige Lehrmeinung, wonach genau gesteuerte Verschaltungsprozesse nur möglich sind, wenn Nervenzellen aktiv miteinander kommunizieren können, zu Fall gebracht.
Die Informationsverarbeitung im menschlichen Nervensystem erfolgt an spezialisierten Kontaktstellen zwischen sendenden und empfangenden Nervenzellen. Ein exakt organisiertes Netzwerk von etwa 100 Billionen dieser als Synapsen bezeichneten Kontaktstellen sorgt für die Verknüpfung der 100 Milliarden Nervenzellen in unserem Gehirn und ist für die Steuerung sowohl von einfachen Körperfunktionen und Bewegungen als auch von komplizierten Verstandes-, Gefühls- und Gedächtnisleistungen verantwortlich. Bis vor kurzem gingen Hirnforscher davon aus, dass ein normaler Ablauf der Gehirnentwicklung nur möglich ist, wenn Nervenzellen schon in den frühesten Phasen der Entwicklung aktiv miteinander kommunizieren können.
Die Kommunikation an den Synapsen beginnt, wenn eine sendende Nervenzelle durch einlaufende Signale erregt wird und ihrerseits Botenstoffe ausschüttet. Diese als Neurotransmitter bezeichneten Signalmoleküle gelangen dann zur jeweiligen Empfängerzelle und beeinflussen wiederum deren Aktivitätszustand. Um den Einfluss dieser synaptischen Kommunikation auf die Gehirnentwicklung zu untersuchen, haben die Forscherteams um Nils Brose und Christian Rosemund genetisch veränderte Mäuse, also Mutanten, erzeugt, deren Nervenzellen nicht mehr zur Freisetzung von Neurotransmittern fähig sind.
Die Untersuchungen an den Mausmutanten, die ein Modell für die menschliche Gehirnentwicklung darstellen, führten zu einem überraschenden Ergebnis: Zwar herrschte in Folge der eingeführten Mutationen in fast allen Teilen des Gehirns dieser Tiere quasi Sendepause, die komplizierten Verschaltungen zwischen den Nervenzellen entwickelten sich jedoch trotzdem weitgehend normal. “Besonders überraschend war, dass sogar die Struktur einzelner Synapsen und ihre Ausstattung mit den für die Synapsenfunktion wichtigen Proteinen in den Mausmutanten vollkommen normal war”, so Nils Brose, Direktor am Max-Planck-Institut für experimentelle Medizin. “Diese Befunde stehen”, wie Christian Rosenmund, Forschungsgruppenleiter am Max-Planck-Institut für biophysikalische Chemie ergänzt, “im Widerspruch zu einer großen Zahl von Arbeiten über die Mechanismen der Gehirnentwicklung.”
Die Forscher sind sich einig, dass ihr genetisches Modellsystem die bisher klarste Einschätzung der Bedeutung von Nervenzellaktivität für die frühe Entwicklung des Nervensystems von Säugetieren liefert: “Entstehung und Erhalt von Synapsen basieren zunächst auf automatisch ablaufenden zellulären Programmen und erfolgen offensichtlich unabhängig von neuronaler Kommunikation”, so Rosenmund. Außer Frage sei dabei allerdings, dass aktive Signalübertragung zwischen Nervenzellen für die exakte Organisation von synaptischen Netzwerken in späteren Phasen der Hirnentwicklung – etwa während der Reifung der für verschiedene Sinneswahrnehmungen verantwortlichen Hirnbereiche – sehr wichtig ist.
Weitere Informationen erhalten Sie von:
Dr. Nils Brose
Abteilung Molekulare Neurobiologie
Max-Planck-Institut für experimentelle Medizin
Tel.: 05 51 – 38 99 – 7 25 (Büro), 38 99 – 7 13 (Labor)
Fax: 05 51 – 38 99 – 7 07
E-Mail: brose@em.mpg.de
Dr. Christian Rosemund
Abteilung Membranbiophysik
Max-Planck-Institut für biophysikalische Chemie
Tel.: 0551 – 201 – 1672
Fax: 0551 – 201 – 1688
E-Mail: crosenm@gwdg.de
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Robotisch assistiertes Laserverfahren soll OP-Risiken minimieren
Eine Spinalkanalstenose – eine knöcherne Verengung des Wirbelkanals – kann für Betroffene zur Qual werden. Drückt sie auf das Rückenmark, drohen ihnen chronische Schmerzen und Lähmungserscheinungen. Häufig hilft dann nur…

Verbesserte Materialien für die Verbindungen von Mikrochips
Leistungsfähiger, stromsparender, komplexer – Hersteller von modernen Microchips sehen sich stetig neuen Herausforderungen gegenüber, auch in Bezug auf die dort notwendigen elektrischen Verbindungen. Das Fraunhofer IPMS und BASF widmen sich…

Inspiriert von der Natur: Biophysiker aus dem Projekt InCamS@BI entwickelt neuartige Mikroplastikfilter im Labor
Heutzutage ist es überall zu finden: Mikroplastik. Es wird insbesondere durch die Luft und durchs Wasser in die entlegensten Winkel der Erde transportiert. Eine der großen Fragen lautet: Wie können…



