Bauplan eines bakteriellen Kraftwerks entschlüsselt
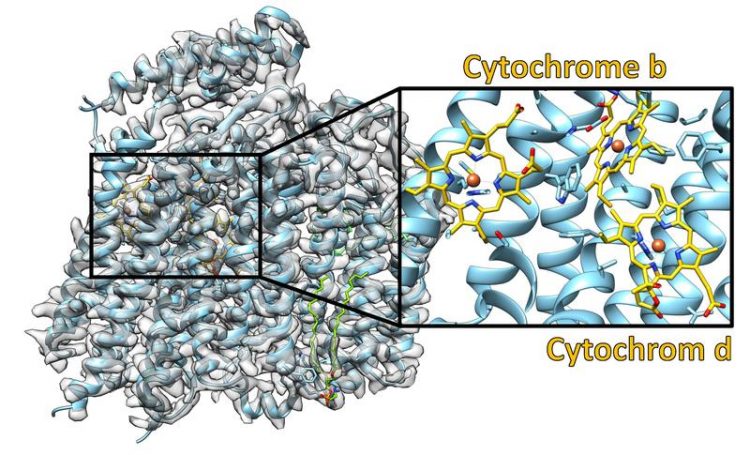
Struktur der Cytochrom-bd-Oxidase: Experimentellen Daten in grau und das daraus abgeleitete molekulare Modell farbig. Die Ausschnittvergrößerung zeigt wo die drei Cytochrome gebunden sind. Rudolf-Virchow-Zentrum, Universität Würzburg
Sowohl Menschen als auch viele andere Lebewesen brauchen Sauerstoff zum Überleben. Bei der Umsetzung von Nährstoffen in Energie wird der Sauerstoff zu Wasser umgewandelt, wofür das Enzym Oxidase verantwortlich ist. Es stellt den letzten Schritt der sogenannten Atmungskette dar.
Energiegewinnung mit Hilfe des Enzyms Oxidase
Während Menschen nur einen Typ dieser Oxidasen besitzen, hat der bakterielle Modellorganismus Escherichia coli (E. coli) drei alternative Enzyme zur Verfügung. Um besser zu verstehen, warum E. coli und andere Bakterien mehrere Oxidasen brauchen, haben Prof. Bettina Böttcher vom Rudolf-Virchow-Zentrum in Zusammenarbeit mit Prof. Thorsten Friedrich (Universität Freiburg) die molekulare Struktur der Cytochrom-bd-Oxidase aus E. coli aufgeklärt. Diesen Typ von Oxidasen findet man nur in Bakterien und den mikrobiellen Archaeen.
Bakterien besitzen andere Typen von Oxidasen
Die namengebenden Cytochrome, zwei vom Typ b und eines vom Typ d, sind die entscheidenden eisenhaltigen Gruppen, die der Oxidase ihre Funktion verleihen. Am Cytochrom d wird der Sauerstoff gebunden und zu Wasser umgesetzt. Bei der Strukturaufklärung stellte sich heraus, dass die Architektur der Cytochrom-bd-Oxidase aus E. coli sehr ähnlich der Struktur aus einem anderen Bakterium ist, Geobacillus thermodenitrificans.
„Zu unserer großen Überraschung zeigte sich jedoch, dass ein Cytochrom b und das Cytochrom d die Positionen gewechselt haben und damit den Ort der Sauerstoffumsetzung innerhalb des Enzyms“, berichtet Prof. Thorsten Friedrich.
Die Ursache für diesen Wechsel könnte sein, dass die Cytochrom-bd-Oxidase eine zweite Funktion erfüllen kann: Neben der Energiegewinnung kann es zum Schutz gegen oxidativen Stress und Stress durch Nitroxide dienen. Besonders pathogene Bakterienstämme zeigen eine hohe Aktivität der Cytochrom-bd-Oxidase.
Da Menschen diesen Typ der Oxidase nicht besitzen, könnten diese Ergebnisse einen wichtigen Hinweis auf die Entwicklung neuer antimikrobieller Wirkstoffe liefern, die auf die Cytochrom-bd-Oxidase von Krankheitserregern wie Mykobakterien abzielen.
Maßgeblich für den Erfolg war das neue Hochleistungselektronenmikroskop, das seit 2018 unter der Leitung von Prof. Böttcher am Rudolf-Virchow-Zentrum betrieben wird. „Die Cytochrom-bd-Oxidase stellte eine anspruchsvolle Probe für die Kryo-Elektronenmikroskopie dar, weil es eines der kleinsten Membranproteine ist, dessen Struktur mit dieser Technik bisher aufgeklärt wurde“, erklärt Prof. Bettina Böttcher.
Besonderheiten dieser Technik sind extrem tiefe Temperaturen bis zu minus 180 Grad Celsius und eine Auflösung, die sich in der Größenordnung von Atomen bewegt. Sie ermöglicht es, biologische Moleküle und Komplexe in Lösung zu untersuchen, die zuvor schockgefroren wurden, und deren dreidimensionale Struktur zu rekonstruieren. Mit einer Spannung von 300.000 Volt beschleunigt das Mikroskop die Elektronen, mit denen es die Proben „abtastet“.
Die Studie wurde im November 2019 im Fachjournal Nature Communications veröffentlicht.
Personen:
Prof. Dr. Bettina Böttcher ist Professorin für Biochemie und leitet seit 2016 eine Forschungsgruppe am Lehrstuhl für Biochemie und am Rudolf-Virchow-Zentrum für Experimentelle Biomedizin der Julius-Maximilians-Universität (JMU) Würzburg.
Prof. Dr. Thorsten Friedrich ist seit 2001 Professor für Biochemie in der Fakultät für Chemie und Pharmazie der Albert-Ludwigs-Universität Freiburg und leitet seit 2016 das von der DFG geförderte Graduiertenkolleg 2202 „Transport über und in Membranen“.
Pressekontakt:
Dr. Daniela Diefenbacher (Pressestelle, Rudolf-Virchow-Zentrum)
Tel. 0931 31 88631, daniela.diefenbacher@uni-wuerzburg.de
Dr. Tim Rasmussen (AG Böttcher, Rudolf-Virchow-Zentrum)
Tel. 0931 31 89659, tim.rasmussen@uni-wuerzburg.de
Prof. Dr. Bettina Böttcher (Rudolf-Virchow-Zentrum, Julius-Maximilians-Universität Würzburg)
Tel. 0931 31 84193, bettina.boettcher@uni-wuerzburg.de
Prof. Dr. Thorsten Friedrich (Universität Freiburg)
Tel. 0761 203 6060, friedrich@bio.chemie.uni-freiburg.de
Alexander Theßeling#, Tim Rasmussen#, Sabrina Burschel, Daniel Wohlwend, Jan
Kägi, Rolf Müller, Bettina Böttcher* and Thorsten Friedrich*: Homologous bd oxidases share the same architecture but differ in mechanism. Nature Communications, Nov 2019, DOI:10.1038/s41467-019-13122-4
Media Contact
Weitere Informationen:
https://www.uni-wuerzburg.deAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















