Von Schnürsenkeln und Eieröffnern – Max-Planck-Forscher entdecken Photosynthese-Helferprotein

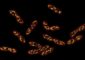
Das Helferprotein (blau) zieht an einem Ende von Rubisco (bunt) und setzt so den Zucker frei. Die Blockade ist aufgehoben. Graphic: Manajit Hayer-Hartl / Copyright: Max Planck Institute of Biochemistry<br>
Rotalgen dagegen nutzen einen leicht veränderten Mechanismus und sind daher produktiver. Forscher vom Max-Planck-Institut für Biochemie (MPIB) haben jetzt ein bisher unbekanntes Helferprotein der Photosynthese in Rotalgen entdeckt. „Wir konnten seine Struktur und seinen faszinierenden Mechanismus entschlüsseln“, erläutert Manajit Hayer-Hartl, Gruppenleiterin am MPIB. „Der Vergleich seines Mechanismus mit dem in grünen Pflanzen könnte helfen, effizientere Pflanzen zu entwickeln.“ Die Arbeit wurde in Nature und Nature Structural & Molecular Biology veröffentlicht.
Pflanzen, Algen und Plankton wandeln Kohlenstoffdioxid (CO2) und Wasser in Sauerstoff und Zucker um. Ohne diesen Prozess (Photosynthese) wäre das heutige Leben undenkbar. Somit ist das Schlüsselprotein der Photosynthese, das Forscher kurz Rubisco nennen, eines der wichtigsten Proteine überhaupt. Es bindet CO2 und leitet die Umwandlung in Zucker und Sauerstoff ein.
“Obwohl es so wichtig ist, steckt Rubisco voller Fehler”, sagt Manajit Hayer-Hartl, Leiterin der Forschungsgruppe “Chaperonin-vermittelte Proteinfaltung“ am MPIB. Ein Problem ist, dass Rubisco falsche Zuckermoleküle bindet, die dann seine Aktivität hemmen. Damit Rubisco seine Arbeit wieder aufnehmen kann, müssen die Zuckermoleküle von einem speziellen Helferprotein (Rubisco Aktivase) entfernt werden. Die Max-Planck-Wissenschaftler haben jetzt entdeckt, dass sich im Laufe der Evolution zwei verschiedene Rubisco Aktivasen in Pflanzen und Rotalgen entwickelt haben. Sie unterscheiden sich in ihrem dreidimensionalen Aufbau und in ihren Arbeitsmechanismen.
Zwei Wege führen zur Wiederherstellung der Rubisco-Aktivität
Die neu entdeckte Rubisco Aktivase in Rotalgen repariert blockierte Rubisco-Proteine, in dem sie an einem Ende des Proteins zieht – wie jemand, der an einem Schnürsenkel zieht. Dadurch öffnet das Helferprotein das aktive Zentrum von Rubisco und setzt so den Zucker frei. Die entsprechende Rubisco Aktivase in Grünpflanzen funktioniert dagegen eher wie ein Eieröffner: Sie quetscht das inaktive Rubisco-Protein und zwingt es so, die Zuckermoleküle frei zu lassen. „Das Verständnis der Struktur und Funktion der beiden Helferproteine könnte helfen Pflanzen und Mikroorganismen herzustellen, die effektiver arbeiten und somit mehr CO2 in Biomasse umwandeln“, hofft Manajit Hayer-Hartl.
Originalveröffentlichungen:
O. Mueller-Cajar, M. Stotz, P. Wendler, F. U. Hartl, A. Bracher & M. Hayer-Hartl: Structure and function of the AAA1protein CbbX, a red-type Rubisco activase. Nature, November 2, 2011
M. Stotz, O. Mueller-Cajar, S. Ciniawsky, P. Wendler, F. U. Hartl, A. Bracher & M. Hayer-Hartl: Structure of green-type Rubisco activase from tobacco. Nature Structural & Molecular Biology, November 6, 2011
Kontakt:
Dr. Manajit Hayer-Hartl
Chaperonin-vermittelte Proteinfaltung
Max-Planck-Institut für Biochemie
Am Klopferspitz 18
82152 Martinsried
mhartl@biochem.mpg.de
Anja Konschak
Öffentlichkeitsarbeit
Max-Planck-Institut für Biochemie
Am Klopferspitz 18
82152 Martinsried
Tel: ++49 (0) 89 8578 2824
E-mail: konschak@biochem.mpg.de
Media Contact
Weitere Informationen:
http://www.biochem.mpg.deAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge
Experiment öffnet Tür für Millionen von Qubits auf einem Chip
Forschenden der Universität Basel und des NCCR SPIN ist es erstmals gelungen, eine kontrollierbare Wechselwirkung zwischen zwei Lochspin-Qubits in einem herkömmlichen Silizium-Transistor zu realisieren. Diese Entwicklung eröffnet die Möglichkeit, Millionen…

Stofftrennung trifft auf Energiewende
Trennkolonnen dienen der Separation von unterschiedlichsten Stoffgemischen in der chemischen Industrie. Die steigende Nutzung erneuerbarer Energiequellen bringt nun jedoch neue Anforderungen für einen flexibleren Betrieb mit sich. Im Projekt ColTray…

Kreuzfahrtschiff als Datensammler
Helmholtz-Innovationsplattform und HX Hurtigruten Expeditions erproben neue Wege in der Ozeanbeobachtung. Wissenschaftliche Forschung nicht nur von speziellen Forschungsschiffen aus zu betreiben, sondern auch von nicht-wissenschaftlichen Schiffen und marinen Infrastrukturen –…