Jedem Krebspatienten seine individuelle Therapie

Die Deutsche Forschungsgemeinschaft (DFG) fördert sieben Teilprojekte mit 2,3 Millionen Euro für die kommenden drei Jahre, die Universität steuert dieselbe Summe bei.
In naher Zukunft wird Krebs vermutlich die Herz-Kreislauf-Erkrankungen als Todesursache Nummer eins ablösen, wie es sich aktuell bereits in den Vereinigten Staaten und in China abzeichnet. „Eines der größten Probleme bei Krebs sind Resistenzen gegenüber Chemotherapeutika“, erläutert Professor Dr. Andreas Neubauer, der Sprecher der Forschergruppe KFO 210 „Genetics of drug resistance in cancer“.
Die beteiligten Wissenschaftler von den Universitäten Marburg und Würzburg wollen nun herausfinden, welche molekularen Signalwege dafür verantwortlich sind, dass Tumorzellen nicht auf Krebsmedikamente ansprechen. Dazu schalten die Forscher einzelne Gene aus, um Rückschlüsse auf deren Funktion ziehen zu können. In Hochdurchsatz-Experimenten können Tausende von Genen pro Durchgang getestet werden, indem man jeweils ein Gen pro Zelle inaktiviert. Die technologische Grundlage für diese Vorgehensweise liefern moderne RNAi-Screening-Verfahren, die Professor Dr. Martin Eilers mit seiner Würzburger Arbeitsgruppe weiterentwickelt, damit die Marburger Kollegen ihre Forschungen mit den neuartigen Instrumenten vorantreiben können.
Die Teilprojekte an der Philipps-Universität unterscheiden sich voneinander hinsichtlich der untersuchten Krebsarten sowie der Signalwege, die erforscht werden sollen. „Wir träumen davon, dass jeder Patient seine individuell zugeschnittene Therapie bekommt“, fasst Neubauer das Fernziel der Forschergruppe zusammen.
Die Universitätsleitung begrüßte die Einrichtung der neuen Forschergruppe. „Die Förderung durch die DFG belegt, welch hohen Stellenwert die Marburger Krebsforschung im nationalen Vergleich hat“, sagte Dr. Friedhelm Nonne, der Kanzler der Philipps-Universität. „Deshalb unterstützt die Universität das Vorhaben auch finanziell.“ Auch Professor Dr. Werner Seeger, der ärztliche Geschäftsführer des Universitätsklinikums Gießen und Marburg zeigte sich erfreut über die Anerkennung der Marburger Universitätsmedizin durch die DFG: „Die bewilligten Projekte stärken das wissenschaftliche Profil unseres Klinikums. Die Förderzusage macht erneut deutlich, wie gut exzellente Forschung in einem privatisierten Umfeld gedeihen kann.“
Die Vorhaben im Einzelnen:
Das Team von Professor Dr. Andreas Neubauer beschäftigt sich mit der Wechselwirkung zwischen einem bekannten Krebsgen und dem Wirkstoff Cytarabin. „Das Projekt geht von klinischen Beobachtungen aus, die ich vor 20 Jahren als junger Wissenschaftler gemacht habe“, erläutert der Onkologe: Leukämie-Patienten, die eine krebsfördernde Mutation im so genannten Ras-Gen tragen, sprechen überdurchschnittlich gut auf das hochdosierte Medikament Cytarabin an. In aktuellen Untersuchungen konnte Neubauer diesen Befund auch in Zellkultur bestätigen. Die DFG-Förderung ermöglicht es nun, nach weiteren Zielgenen im Ras-Signalweg zu fahnden, die anschließend molekular charakterisiert und in Zellkultur getestet werden sollen.
Dr. Andreas Burchert sucht nach Genen, die dafür verantwortlich sind, dass Tumorzellen eine Behandlung mit dem Wirkstoff Cisplatin oder Imatinib überdauern. Als Modell hierfür dienen das Lungenkarzinom und die chronische myeloische Leukämie. Burchert ist zugleich Leiter der Forschergruppe.
Die Bedeutung des Proteins WNT5A für das Überleben von Tumorzellen ist das Thema von Dr. Patrick Michl. Er möchte am Beispiel von Bauchspeicheldrüsen-Krebs die Rolle von Molekülen aufklären, die das WNT5A-Signal weiterleiten oder modifizieren.
Dr. Volker Ellenrieder widmet sich in seiner Forschungsarbeit ebenfalls dem Bauchspeicheldrüsen-Krebs. Das Teilprojekt gilt der Frage, wie der Transkriptionsfaktor NFAT zur Chemoresistenz beiträgt, indem er mit dem Ras-Signalweg interagiert.
Die Arbeitsgruppe von Professor Dr. Thomas Stiewe befasst sich mit einem zellulären Reparatursystem, das Fehler bei der Vervielfältigung der Erbsubstanz DNA aufdeckt und korrigiert. Wenn das Reparatursystem nicht funktionsfähig ist, kommt es vermehrt zur Tumorbildung.
Die Voraussetzungen für die verschiedenen Vorhaben liefert das Plattform-Projekt von Professor Dr. Martin Eilers in Würzburg. Das Ziel seiner Arbeitsgruppe ist es, Fremd-DNA mittels Viren in Zellen einzuschleusen, so dass dort zelleigene Gene ausgeschaltet werden.
Dr. Cornelia Brendel wird in ihrem Teilprojekt aufwendige Zellsortierungs-Verfahren verwenden, um Zelltypen zu finden, die dafür verantwortlich sind, dass Patienten nicht auf Therapien ansprechen oder einen Rückfall erleiden.
Weitere Informationen:
Ansprechpartnerin zum Pressegespräch:
Dr. Sabine Eber,
Fachbereich Medizin
Tel.: 06421 58-66370
E-Mail: eber@med.uni-marburg.de
Ansprechpartner für Fragen zur Forschergruppe:
Professor Dr. Andreas Neubauer,
Klinik für Hämatologie, Onkologie und Immunologie
Tel.: 06421 58-66272
E-Mail: neubauer@staff.uni-marburg.de
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Wie die Galvanotechnik durch Digitalisierung effizient wird
SurfaceTechnology GERMANY… Digitalisierung und Hartverchromung aus Chrom(III)-Elektrolyten: Das sind die beiden großen Themen, mit denen sich Forscherinnen und Forscher von der Abteilung Galvanotechnik am Fraunhofer IPA derzeit beschäftigen. Ihre Erkenntnisse…

Ersatz für Tierversuche – jetzt ganz ohne Tierleid
Erstes Gewebe-Modell der Leber völlig ohne Materialien tierischer Herkunft hergestellt. Wissenschaftler*innen der TU Berlin haben mit Hilfe von 3D-Biodruck erstmals ein Modell der Leber aus menschlichen Zellen hergestellt, ohne dabei…
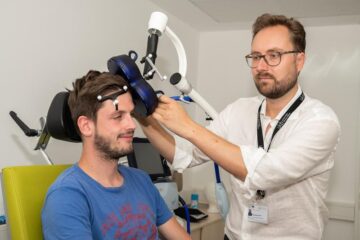
Neue Wege zur mentalen Gesundheit
Magnetspule am Kopf sorgt für antidepressive Effekte… In der Klinik und Poliklinik für Psychiatrie und Psychotherapie am Universitätsklinikum Bonn (UKB) wird derzeit eine Studie zur Erforschung der antidepressiven Wirkung einer…