Ein negatives Enzym liefert positive Resultate
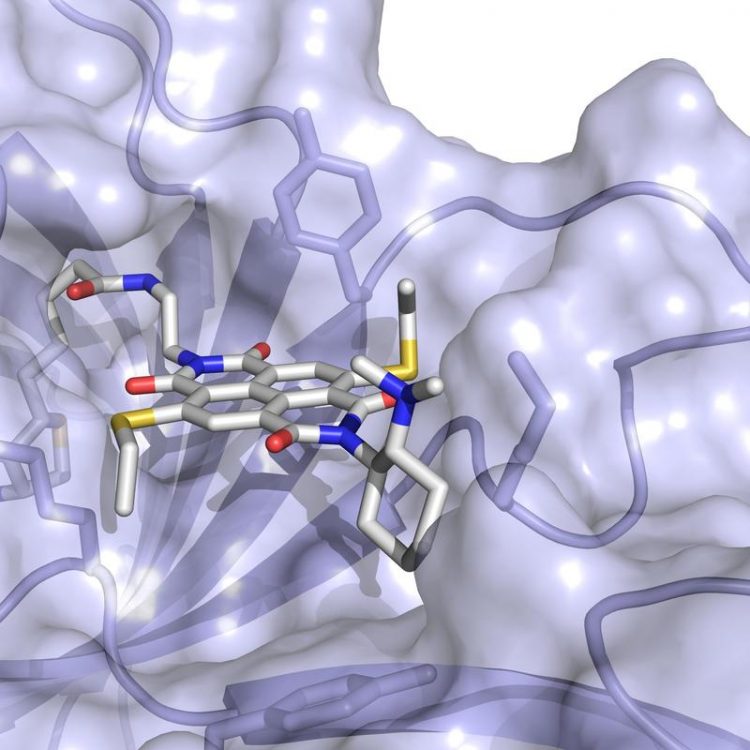
Das Anion-π-Enzym besteht aus einem elektronenarmen Aren-Kofaktor (graue Stäbchenrepresentation), eingebettet in ein Protein (als Oberfläche dargestellt). Universität Basel, Departement Chemie
Proteine sind die Arbeitspferde jeder Zelle. Sie bestehen aus Aminosäurebausteinen, die als Kette verbunden sind, welche sich zu funktionalen Maschinen zusammenfalten, um anschliessend alle wesentlichen zellulären Prozesse anzutreiben.
Für diese Aufgaben benötigt die Natur zwanzig solcher Aminosäurebausteine zusammen mit ein paar spezialisierten Kofaktoren, die häufig zu der Gruppe der Vitamine zählen. Chemiker haben intelligente Wege gefunden, wie man das natürliche Proteinrepertoire beispielsweise durch das Hinzufügen zusätzlicher nicht-natürlicher Aminosäuren oder Kofaktoren erweitern kann.
Die Forscher um Stefan Matile und Thomas Ward haben jetzt einen neuartigen Kofaktor geschaffen, welcher eine der klassischen Wechselwirkungen in Proteinen umkehrt: die Kationen-π-Bindung, also die Stabilisierung einer positiven Ladung durch Anlagerung an eine elektronenreiche Molekülebene. Die Natur verwendet diese Kationen-π-Bindungen bei der Herstellung von so wichtigen Molekülen wie Steroiden, Hormonen, Vitaminen, Sehpigmenten oder Duftstoffen, um Signale in das Gehirn zu vermitteln, Antigene zu erkennen und Ähnlichem.
Nun haben die Forschungsgruppen von Matile und Ward ihren neuen Kofaktor und das daraus resultierende künstlichen Protein verwendet, um zusammen das erste «Anionen-π-Enzym» der Natur zu bauen.
Darin ist die elektronenreiche durch eine elektronenarme Moleküleben ersetzt, wodurch eine negative Ladung während der Reaktion stabilisiert wird. Die Forscher konnten zeigen, dass Proteine mit dieser in der Natur nicht vorkommenden Funktionalität traditionelle organisch-chemische Katalysatoren in einer wichtigen, aber energetisch ungünstigen Reaktion bezüglich ihrer hohen Spezifität und Selektivität übertreffen.
Die Forscher sind optimistisch, dass dieser Ansatz in Zukunft in Zellen verwendet werden kann, um bisher unmögliche chemische Transformationen zu ermöglichen.
Die Autoren bedanken sich für die finanzielle Unterstützung durch den Nationalen Forschungsschwerpunkt (NFS) Molecular Systems Engineering und Chemische Biologie, bei der Universität Genf und der Universität Basel sowie dem Europäischen Forschungsrat.
https://www.unibas.ch/de/Aktuell/News/Uni-Research/Ein-negatives-Enzym-liefert-p…
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge
Forschende enthüllen neue Funktion von Onkoproteinen
Forschende der Uni Würzburg haben herausgefunden: Das Onkoprotein MYCN lässt Krebszellen nicht nur stärker wachsen, sondern macht sie auch resistenter gegen Medikamente. Für die Entwicklung neuer Therapien ist das ein…

Mit Kleinsatelliten den Asteroiden Apophis erforschen
In fünf Jahren fliegt ein größerer Asteroid sehr nah an der Erde vorbei – eine einmalige Chance, ihn zu erforschen. An der Uni Würzburg werden Konzepte für eine nationale Kleinsatellitenmission…

Zellskelett-Gene regulieren Vernetzung im Säugerhirn
Marburger Forschungsteam beleuchtet, wie Nervenzellen Netzwerke bilden. Ein Molekülpaar zu trennen, hat Auswirkungen auf das Networking im Hirn: So lässt sich zusammenfassen, was eine Marburger Forschungsgruppe jetzt über die Vernetzung…