Neuer Signalweg für das mTor-abhängige Zellwachstum entdeckt
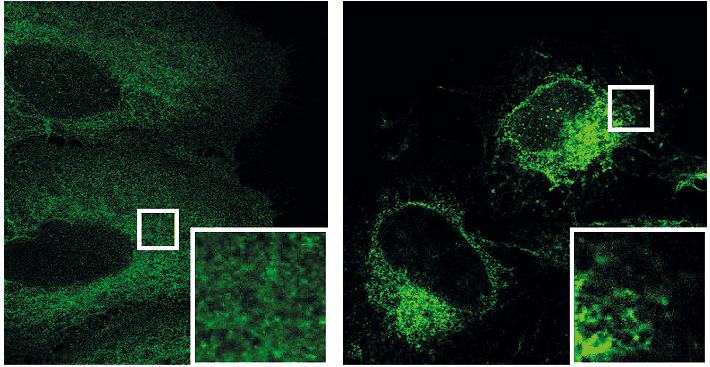
Links: Protein-Kinase N (PKN) ist aktiv und inhibitiert PI3KC2ß (grün eingefärbt). Rechts: PKN fehlt. Das führt dazu, dass PI3KC2ß die Lokalisation in der Zelle ändert und aktiv ist. Bild: Alexander Wallroth, FMP
Signalwege in Körperzellen sind enorm komplex: Damit ein bestimmter Mechanismus ausgelöst wird, müssen mehrere „Schalter“ in einer festgelegten Reihenfolge „umgelegt“ werden. Diese „Schalter“ zu finden, kann jedoch knifflig sein, weil an der zellulären Signalübermittlung zahlreiche Substanzen und Stoffkomplexe beteiligt sind, deren Rolle nicht immer einfach zu identifizieren ist.
So war lange unbekannt, wie der mTor-Komplex 1 in der Zelle deaktiviert werden kann. Diesen „Schalter“ hatten Forschende des FMP bereits 2017 identifizieren können: Eine bestimmte Lipid-Kinase (PI3KC2ß) fungiert als natürliche Bremse für das Protein mTor und sorgt dafür, dass der mTor-Komplex 1 abgeschaltet wird, etwa wenn bestimmte hormonelle Signale wie Insulin ausbleiben.
Alexander Wallroth aus der Arbeitsgruppe von Volker Haucke hat nun genauer untersucht, wie diese Lipid-Kinase reguliert wird. „Wir haben die Lipidkinase auf verschiedene Weise manipuliert und uns angeschaut, welche Effekte das auf die Aktivität von mTOR und auf das Zellwachstum hat“, so der Biologe.
Dabei fanden die Forschenden einen Mechanismus, wie die Lipid-Kinase PI3KC2ß inaktiviert wird. Eine wichtige Rolle spielt dabei eine weitere Kinase, die Protein-Kinase N (PKN). Sie hemmt die Lipid-Kinase PI3KC2ß und sorgt dadurch indirekt für die Aktivierung von mTOR. Die Proteinkinase N wird über Wachstumsfaktoren reguliert:
Wachstumsfaktoren stimulieren an der Zellmembran den mTor-Komplex 2, den zweiten Protein-Komplex, in dem mTor in der Zelle vorliegt. Dieser wiederum aktiviert die PKN, die ihrerseits die Lipid-Kinase deaktiviert.
„Damit haben wir zwei weitere Komponenten gefunden, die pharmaklogisch angegriffen werden könnten“, erklärt Alexander Wallroth. Schafft man es nämlich, PKN zu hemmen, wird die Lipid-Kinase PI3KC2ß aktiviert und schlussendlich mTOR-abhängiges Zellwachstum unterbunden. Wird der Signalweg über Wachstumsfaktoren, den mTor-Komplex 2 und, schließlich, PKN hingegen aktiviert, bleibt die Lipid-Kinase inaktiv und der mTOR-Komplex 1 kann das Zellwachstum befördern.
Inhibitoren, die PKN hemmen könnten, kennt man bereits. Diese sind allerdings nicht sehr spezifisch und blockieren auch viele andere lebenswichtige Vorgänge in der Zelle, so dass sie im lebenden Gewebe derzeit noch nicht eingesetzt werden können.„Interessant an unseren Ergebnissen ist insbesondere, dass wir einen zellbiologischen Signalweg gefunden haben, der die mTor-Komplexe 1 und 2 miteinander verbindet. Schaltet man z.B. 2 aus, wirkt sich das auch auf 1 aus“, sagt Alexander Wallroth.
So konnten die Forschenden in der vorangegangenen Arbeit zeigen, dass die Lipid-Kinase PI3KC2ß direkt auf den mTor-Komplex 1 einwirkt, wenn sie aktiviert ist. Wird nun durch mTor-Komplex 2 die PKN aktiviert und damit die Lipid-Kinase deaktiviert, wirkt sich das auch auf den mTor-Komplex 1 aus. Über den mTor-Komplex 2 war im Verhältnis zu Komplex 1 bisher weniger bekannt. Die vorliegenden Ergebnisse zeigen nun, dass mTOR Komplex 2 die Aktivität des wichtigen Komplex 1 mitsteuert.
„Das gibt weiteren Forschungen zu medizinischen Eingriffsmöglichkeiten bei verschiedenen Krankheiten wie Insulinresistenz oder Krebs neuen Spielraum“, betont Alexander Wallroth.
Bildunterschrift: Links: Protein-Kinase N (PKN) ist aktiv und inhibitiert PI3KC2ß (grün eingefärbt). Rechts: PKN fehlt. Das führt dazu, dass PI3KC2ß die Lokalisation in der Zelle ändert und aktiv ist. Bild: Alexander Wallroth, FMP
Professor Dr. Volker Haucke
Professor für Molekulare Pharmakologie an der Freien Universität Berlin
Mitglied im Exzellenzcluster NeuroCure
Direktor am Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP)
Robert-Rössle-Str.1013125 Berlin,
Campus Berlin-Buch
E-Mail: haucke@fmp-berlin.de
www.leibniz-fmp.de/haucke
Marat, A.L., Wallroth, A., Lo, W., Müller, R., Norata, G.D., Falsaca, M., Schultz, C., Haucke, V. (2017) mTORC1 activity repression by late endosomal phosphatidylinositol 3,4 bisphosphate. Science, Ausgabe vom 2. Juni 2017
Wallroth, A., Koch, P. A., Marat, A. L., Krause, E., Haucke, V. (2019). Protein kinase N controls a lysosomal lipid switch to facilitate nutrient signalling via mTORC1. Nature Cell Biology, Ausgabe September 2019
http://www.leibniz-fmp.de/de/press-media/filmportraits-2017/filmportraits-2017-v…
http://www.leibniz-fmp.de/haucke
https://www.leibniz-fmp.de/de/press-media/press-releases/press-releases-single-v…
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















