Innsbrucker Team entschlüsselt neuen Mechanismus zur gezielten Aktivierung des Tumorsuppressors p53
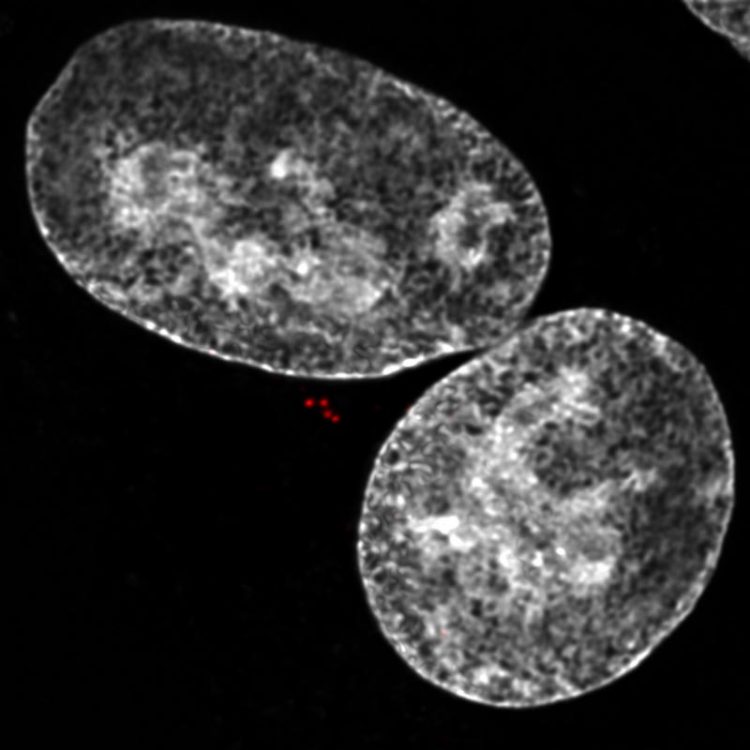
Die Abbildung (Fluoreszenzmikroskop) zeigt das Innere einer Krebszelle nach fehlerhafter Zytokinese: Man sieht zwei Zellkerne (weiss) und vier rote Punkte, die zwei Zentrosomen markieren, die jeweils aus zwei Zentriolen aufgebaut sind. Zentrosomen sind wichtige Organelle, die das Zytoskelett in der Zelle organisieren und die nach einem Zytokinesefehler doppelt vorkommen. (c) MUI
Fehler im Prozess der Zellteilung (Zytokinese) können zur Verdopplung des Genoms und damit zur Entstehung von Zellen mit vierfachem Chromosomensatz führen. Dieser „tetraploide“ kann zu einem „aneuploiden“ Zustand (ungleiche Chromosomen-Verteilung) führen – ein Merkmal vieler Tumorzellen, verbunden mit oft schlechter Prognose und für das Team um Andreas Villunger vom Biozentrum Innsbruck zugleich potentielle Angriffsfläche für neue Krebstherapien. In einer aktuellen Forschungsarbeit beleuchten die ForscherInnen einen neuen Aktivierungsmechanismus des Tumorsuppressors p53 nach fehlerhafter Zytokinese.
Bereits seit vielen Jahren ist bekannt, dass der Transkriptionsfaktor p53 bei mehr als der Hälfte aller TumorpatientInnen durch Mutation inaktiviert ist, was seine kritische Rolle bei der Vermeidung von Krebs untermauert. In gesunden Zellen fungiert p53 als eine Art Bremse, die Zellen vor unkontrolliertem Wachstum nach defekter Zellteilung oder nach DNA Schädigung schützt. Im Visier des Forschungsteams um Andreas Villunger, Leiter der Sektion für Entwicklungsimmunologie am Innsbrucker Biozentrum, stehen deshalb auch jene Mechanismen, die zur Aktivierung des wichtigsten Tumorsuppressors nach fehlerhafter Zytokinese führen.
Unvollständige Zellteilung im Blickwinkel
Die Zellteilung ist ein eng regulierter Prozess. In der Regel erfolgt die Abschnürung und Teilung einer Mutter- in zwei Tochterzellen nach erfolgreicher Verdoppelung des Genoms mit höchster Präzision. Läuft dies nicht korrekt oder ungenau ab, wird dieser Prozess abgerochen und es entsteht eine Zelle mit vier Chromosomensätzen (Tetraploidie).
Um solche Zellen vor unkontrolliertem Wachstum und chromosomaler Instabilität zu schützen, wird die Kontrollfunktion des Proteins p53 benötigt. „Dieses frühe Stadium der potentiellen Tumorentstehung, dessen Beitrag zur Tumorevolution und jene Mechanismen, die zur Aktivierung von p53 führen, bilden momentan das Zentrum für unsere Suche nach neuen Ansätzen für die Krebstherapie“, berichtet Andreas Villunger, der mit seinem Team erst kürzlich nachweisen konnte, dass das Enzym Caspase-2, eine Protease mit sehr diversen Eigenschaften, die p53-Aktivierung stimulieren kann.
p53-Aktivierung durch Multiproteinkomplex
In der aktuellen, soeben im renommierten Journal Genes & Development veröffentlichten Forschungsarbeit nahm das Team mit Erstautor Luca Fava den Prozess der p53 Aktivierung in tetraploiden Zellen unter die Lupe und beleuchtete die bislang unerforschten Mechanismen, die nach DNA-Verdoppelung und fehlerhafter Zytokinese zur p53-Aktivierung führen.
Im Fokus stand ein als PIDDosom bekannter Multiproteinkomplex, bestehend aus den Proteasen PIDD1, RAIDD und Caspase-2. Mittels biochemischer als auch zellbiologischer Verfahren und mit Unterstützung weiterer Forschungsgruppen am Standort wie auch des Biozentrums in Basel gelang es erstmals nachzuweisen, dass das eiweißspaltende Enzym Caspase-2 das onkogene Substrat MDM2 spaltet und somit dessen Funktion als Negativregulator von p53 aushebelt.
„Das Protein p53 wird auf diese Weise stabilisiert und kann dadurch selektiv seine wachstumshemmende Wirkung entfalten“, erklärt Erstautor Luca Fava, der nach fünfjähriger Forschungsarbeit im Labor von Andreas Villunger nun mit einem 1-Million-$-Grant der Armenise Harvard Foundation nach Italien zurückkehrt, um in Trient am Zentrum für Integrative Biologie (CIBIO) sein eigenes Labor aufzubauen.
Mit der erstmaligen Beschreibung dieses Mechanismus der p53-Aktivierung erhellen die Innsbrucker ForscherInnen einen weiteren Baustein im zentralen Prozess der Zellzykluskontrolle und liefern vor dem Hintergrund des bevorstehenden Weltkrebstages einen neuen potentiellen Ansatz für die Entwicklung innovativer Krebstherapien. Letztendlich soll es gelingen, den Transkriptionsfaktor p53 gezielt pharmakologisch in Tumorzellen, die diesen noch nicht verloren haben, aktivieren zu können.
Die Forschung des Teams um Andreas Villunger wird durch den FWF und das Sonderprogramm Partnership in Research (PiR) der Christian Doppler Forschungsgesellschaft unterstützt.
Für Rückfragen:
Univ.Prof. Mag.Dr Andreas Villunger
Sektion für Entwicklungsimmunologie
Mobile: +43 676 871672380 E-Mail: Andreas.Villunger@i-med.ac.at
Mag.Dr. Luca Fava
Sektion für Entwicklungsimmunologie
Tel.: +43 512 9003 70369
E-Mail: Luca.Fava@i-med.ac.at
Medienkontakt:
Mag.a Doris Heidegger
Medizinische Universität Innsbruck
Abteilung für Öffentlichkeitsarbeit
Innrain 52, 6020 Innsbruck, Austria
Telefon: +43 512 9003 70083, Mobil: +43 676 8716 72083
public-relations@i-med.ac.at, www.i-med.ac.at
Details zur Medizinischen Universität Innsbruck
Die Medizinische Universität Innsbruck mit ihren rund 1.400* MitarbeiterInnen und ca. 3.000 Studierenden ist gemeinsam mit der Universität Innsbruck die größte Bildungs- und Forschungseinrichtung in Westösterreich und versteht sich als Landesuniversität für Tirol, Vorarlberg, Südtirol und Liechtenstein. An der Medizinischen Universität Innsbruck werden folgende Studienrichtungen angeboten: Humanmedizin und Zahnmedizin als Grundlage einer akademischen medizinischen Ausbildung und das PhD-Studium (Doktorat) als postgraduale Vertiefung des wissenschaftlichen Arbeitens. An das Studium der Human- oder Zahnmedizin kann außerdem der berufsbegleitende Clinical PhD angeschlossen werden.
Seit Herbst 2011 bietet die Medizinische Universität Innsbruck exklusiv in Österreich das Bachelorstudium „Molekulare Medizin“ an. Ab dem Wintersemester 2014/15 kann als weiterführende Ausbildung das Masterstudium „Molekulare Medizin“ absolviert werden.
Die Medizinische Universität Innsbruck ist in zahlreiche internationale Bildungs- und Forschungsprogramme sowie Netzwerke eingebunden. Schwerpunkte der Forschung liegen in den Bereichen Onkologie, Neurowissenschaften, Genetik, Epigenetik und Genomik sowie Infektiologie, Immunologie & Organ- und Gewebeersatz. Die wissenschaftliche Forschung an der Medizinischen Universität Innsbruck ist im hochkompetitiven Bereich der Forschungsförderung sowohl national auch international sehr erfolgreich.
*vollzeitäquivalent
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















