Wenn der Durchschnitt einfach nicht gut genug ist
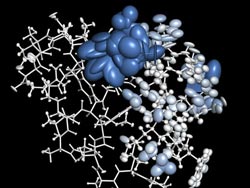
Atommodell des Proteins Villin Kopfstück. Farbe und Größe der Ellipsoide stellen die lokale Dynamik der einzelnen Atome dar.<br><br>Copyright: Bojan Zagrovic<br>
Am Beispiel der Analyse von Proteinkristallstrukturen demonstrieren Computerbiologen der Max F. Perutz Laboratories der Universität Wien und der Medizinischen Universität Wien nun, dass das nicht immer der beste Weg ist.
Die Studie des Teams um Bojan Zagrovic, erschienen im Fachjournal Nature Communications, zeigt, dass Proteinstrukturen wahrscheinlich sehr viel dynamischer und heterogener sind, als gängige Methoden zur Röntgenstrukturanalyse nahelegen.
Wann die Ermittlung des Durchschnitts gut ist und wann nicht
Generell ist der Durchschnitt eine gute Sache, denn er kann helfen, einen Überblick über verschiedenste Gegebenheiten zu bekommen und das Leben ein ganzes Stück einfacher machen. Zum Beispiel wenn es beim Essen mit einer Gruppe von FreundInnen ans Bezahlen geht. Nimmt man die Gesamtrechnung und teilt sie durch die Anzahl der anwesenden Personen, bezahlt jederR in etwa soviel, wie er auch individuell bezahlt hätte, vorausgesetzt jedeR hatte ein Getränk und ein Essen.
Haben jedoch einige eine Vorspeise, Steak, Dessert und Sekt bestellt, während man selbst nur Spaghetti und ein Glas Wasser hatte, wird man sich ziemlich abgezockt vorkommen, wenn man plötzlich den Durchschnitt von 45€ für das Essen zahlt. Auch bei der Analyse wissenschaftlicher Daten wird der Durchschnitt ermittelt und das ist gut so: WissenschaftlerInnen wiederholen ihre Experimente zumeist viele Male und bilden den Durchschnitt aus all ihren Messergebnissen. Nur wenn diese lediglich in geringem Maße voneinander abweichen, werden die ForscherInnen ihren Laborergebnisse Glauben schenken.
Röntgenkristallographie – oder wie die Struktur von Proteinen ermittelt wird
Eine der wichtigsten Methoden der modernen Biologie ist die Röntgenkristallographie. Hinter diesem komplizierten Namen steckt eine Methode, die es erlaubt, die Struktur von Proteinen zu ermitteln. Kennen WissenschaftlerInnen die Struktur eines Proteins, können sie nicht nur Rückschlüsse ziehen, was seine Funktion ist und wie es diese ausübt, sondern auch Medikamente entwickeln, die diese Funktion hemmen oder aktivieren. Zur Röntgenkristallographie wird ein Protein aufgereinigt und getrocknet – dabei entsteht ein Kristall aus Abermillionen Kopien des gleichen Proteins.
Bestrahlt man diesen nun mit Röntgenstrahlen, erhält man ein Bild von der Anordnung der kleinsten Baueinheiten eines Proteins – den Atomen – und wie dynamisch jedes Einzelne davon ist, d.h. wie stark es in seiner Position herumwackeln kann. Die Analyse eines Kristalls liefert also den Durchschnitt des Verhaltens von Abermillionen der jeweils gleichen Atome. Man würde annehmen, dass das genug ist um mit ziemlicher Sicherheit Aussagen über die tatsächliche Struktur des Proteins in der Natur machen zu können. Das dem nicht so ist und dass der Durchschnitt einen manchmal täuschen kann, erklärt der Leiter der Studie, Bojan Zagrovic: „Würde man zum Beispiel den durchschnittlichen Aufenthaltsort eines Torhüters während eine Fußballspiels bestimmen, bei dem nach der Halbzeit die Teams die Seiten wechseln, würde dieser ziemlich genau in der Mitte des Feldes liegen. Ich denke, wir alle sind uns einig, dass das weit von der Realität entfernt ist.“
Die Atome von Proteinen wackeln bis zu sechsmal stärker als bisher angenommen
Wie genau können also die derzeit verwendeten Programme zur Analyse von röntgenkristallographischen Daten die Struktur und Dynamik eines Proteins bestimmen? Dieser Frage ging Antonija Kuzmanic, im Rahmen ihrer Doktorarbeit im Labor von Zagrovic und unterstützt durch dessen Starting Grant des Europäischen Forschungsrates (ERC) nach. In Zusammenarbeit mit Kollege Navraj S. Pannu an der Universität von Leiden, Niederlande, nutze sie Computersimulationen um einen Proteinkristall zu „bauen“ und diesen röntgenkristallographisch zu untersuchen. Die dabei gewonnen Daten wurden schließlich mit den derzeit gängigen Softwareprogrammen ausgewertet und die Struktur des Proteins bestimmt. Dieser experimentelle Aufbau erlaubte es Antonija Kuzmanic Rückschlüsse darauf zu ziehen, ob und wie genau die momentanen Analysemethoden wirklich das „sehen“ was da ist. „Wir waren total überrascht, als wir festgestellt haben, dass die gängigen Programme zur Analyse röntgenkristallographischer Daten zur Strukturbestimmung von Proteinen die Dynamik innerhalb des Proteins – also wie stark jedes einzelne Atom in seiner Position herumwackeln kann – völlig unterschätzen. Unsere Daten zeigen, dass die Beweglichkeit der Atome bis zu sechsmal höher ist. Das ist, als ob man seinen Kopf plötzlich um 180 Grad drehen könnte, statt nur nach links oder rechts“, wie Antonija Kuzmanic erklärt.
Inspirierende Arbeit
Garib Murshudov von der Universität Cambridge in England, Strukturbiologe und einer der Gutachter der Doktorarbeit von Antonija Kuzmanic, schrieb: „Das ist mein Lieblingskapitel, es ist inspirierend … es zeigt ganz eindeutig, dass wir neue Methoden brauchen um die Dynamik von Proteinen in Kristallen zu beschreiben.“
Solche Programme zur genaueren Analyse röntgenkristallographischer Daten und zur Bestimmung der Dynamik eines Proteins werden nicht nur ein realistischeres Bild von der Struktur eines Proteins in der Natur geben – also davon, wo der Torhüter sich tatsächlich aufhält und wie er sich bewegt – sondern auch helfen neue Medikamente zu entwickeln, die die Funktion eines Proteins gezielter und effizienter regulieren können.
Publikation in Nature Communications:
Antonija Kuzmanic, Navraj S. Pannu and Bojan Zagrovic: X-ray refinement significantly underestimates the level of microscopic heterogeneity in biomolecular crystals. In: Nature Communications (January 2014).
DOI: http://dx.doi.org/10.1038/ncomms4220
Max F. Perutz Laboratories
Die Max F. Perutz Laboratories (MFPL) sind ein gemeinsames Forschungs- und Ausbildungszentrum der Universität Wien und der Medizinischen Universität Wien am Campus Vienna Biocenter. An den MFPL sind rund 500 WissenschaftlerInnen in über 60 Forschungsgruppen mit Grundlagenforschung im Bereich der Molekularbiologie beschäftigt.
Rückfragehinweis:
Dr. Lilly Sommer
Max F. Perutz Laboratories
Communications
T +43-1-4277-240 14
lilly.sommer@mfpl.ac.at
Media Contact
Weitere Informationen:
http://www.univie.ac.at/Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















