Ungewöhnliche Proteinstrukturen machen Bakterien hitzebeständig
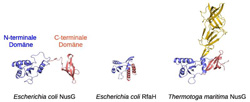
Links: Das Protein NusG zeigt in Bakterien wie Escherichia coli keine Wechselwirkung zwischen der N-terminalen Domäne (blau) und der C-terminalen Domäne (rot). Die Domänen sind relativ zueinander frei beweglich und können so an weitere Proteine binden. // Mitte: Das Bakterium Escherichia coli besitzt auch ein dem NusG ähnliches Protein, RfaH. Hier liegen die Domänen eng beieinander, sie werden erst durch die Bindung eines spezifischen DNA Stücks geöffnet, wobei die C-terminale Domäne komplett ihre Struktur ändert. // Rechts: Im Bakterium Thermotoga maritima trägt die Wechselwirkung zwischen der N-terminalen Domäne (blau) und der C-terminalen Domäne (rot) erheblich zur Stabilität des Proteins bei. Zusätzlich existiert eine weitere strukturelle Einheit (gelb), deren Funktion bisher unbekannt ist.<br><br>Grafik: Dr. Kristian Schweimer, Lehrstuhl Biopolymere, Universität Bayreuth; mit Quellenangabe zur Veröffentlichung frei.<br>
Thermotoga maritima jedoch ist ein Bakterium, das sich dem Wachstum in heißen Quellen und in vulkanischem Gestein sehr gut angepasst hat. Damit Bakterien unter diesen Bedingungen leben können, müssen ihre Proteine sehr temperaturstabil sein.
Die erhöhte Stabilität des Proteins NusG aus Thermotoga maritima zum Beispiel kann durch das ungewöhnliche Wechselspiel einzelner Strukturelemente erklärt werden. Darüber berichtet ein Forschungsteam unter der Leitung von Prof. Dr. Paul Rösch, Lehrstuhl Biopolymere der Universität Bayreuth, in der Zeitschrift „Structure“.
Funktionsuntüchtig, aber stabil:
NusG-Moleküle im geschlossenen Zustand
Proteine vom Typ des bakteriellen NusG übernehmen, soweit bekannt, in vielen Organismen lebenswichtige Steuerungsfunktionen. NusG-Proteine sind entscheidend an der Genexpression beteiligt, insbesondere am Vorgang der Transkription, bei dem die in der DNA enthaltene Erbinformation in RNA umgeschrieben wird. Hier hat NusG die Aufgabe, verschiedene weitere Proteine mit dem Enzym RNA-Polymerase zu verknüpfen. Oft besteht NusG aus zwei klar unterscheidbaren räumlich strukturierten Einheiten, der amino- und der carboxyterminalen Domäne. Wie bei früheren Forschungsarbeiten beobachtet werden konnte, treten in vielen Bakterienarten diese Domänen nicht miteinander in Kontakt. Dadurch ist gewährleistet, dass sie sich bei der Erfüllung ihrer spezifischen Funktionen nicht behindern.
Anders verhält es sich jedoch bei der Bakterienart Thermotoga maritima. Wie die Bayreuther Wissenschaftler zusammen mit Kollegen an der Freien Universität Berlin und der Columbia University, New York, festgestellt haben, hat das Protein NusG in diesen Bakterien zumeist eine geschlossene Struktur, das heißt, die zwei Domänen liegen fast immer eng beieinander. Dies hat zur Folge, dass ausgerechnet diejenigen Bereiche, die mit anderen Proteinen wechselwirken können, sich gegenseitig verdecken. In dieser Struktur ist keine der beiden Domänen imstande, an lebenswichtigen Prozessen der Genexpression teilzunehmen. Das Protein NusG macht sich mithin selbst funktionsuntüchtig, ein Zustand, den die Forschung als Autoinhibition bezeichnet. Und doch hat diese Struktur für das Bakterium einen wesentlichen Vorteil: Sie erhöht die Stabilität des Proteins und bewirkt, dass es hohen Temperaturen standhalten kann.
Blitzschnelle Strukturwechsel:
Oszillierende NusG-Moleküle
NusG verharrt aber nicht in dieser geschützten Struktur. Um wenigstens kurzfristig aktiv werden zu können, öffnet sich das Protein. Jetzt haben die beiden Domänen die Bewegungsfreiheit, die sie brauchen, um mit anderen Proteinen in Wechselwirkung zu treten. Mit NMR-spektroskopischen Analysen an der Universität Bayreuth ist es den Forschern gelungen, diesen Strukturwechsel zu beobachten. Ihre Untersuchungen haben zu dem Ergebnis geführt, dass sich jedes NusG-Molekül für den winzigen Zeitraum von 2 Hunderttausendstel Sekunden öffnet. Danach fällt es sofort in den geschlossenen Zustand zurück, in dem es etwa 1 Tausendstel Sekunde lang verbleibt. Da sich dieser Rückfall in die Inaktivität schneller vollzieht als die Öffnung, befinden sich zu jedem beliebigen Zeitpunkt rund 98 Prozent der im Bakterium enthaltenen NusG-Moleküle im geschlossenen Zustand. Nur die restlichen 2 Prozent sind geöffnet.
„Das ständige Oszillieren zwischen zwei verschiedenen Strukturen ist ein äußerst ungewöhnlicher Kunstgriff der Natur, durch den gewährleistet ist, dass die NusG-Moleküle einerseits sehr hohen Temperaturen standhalten, andererseits aber an der Genexpression und an weiteren zellulären Prozessen mitwirken können“, erklärt Dr. Kristian Schweimer vom Lehrstuhl Biopolymere der Universität Bayreuth. „Ein solcher blitzschneller Strukturwechsel ist bei ähnlichen Proteinen der bei Raumtemperatur lebenden Bakterien bisher nicht beobachtet worden.“
NusG-Proteine aus hitzebeständigen Bakterien:
Untätig in normalen Bakterien
Was geschieht, wenn man E.coli-Bakterien, die am besten bei Körpertemperatur leben, diese zwischen einer offenen und einer geschlossenen Struktur oszillierenden NusG-Proteine unterschiebt? Wie die Bayreuther Wissenschaftler herausgefunden haben, verhalten sich die eingepflanzten Proteine völlig passiv. „Die Neigung zur Autoinhibition ist offenbar die Ursache dafür, dass die NusG-Proteine in gewöhnlichen Bakterien wie E.coli nicht durch NusG-Proteine aus den hitzebeständigen Bakterien ersetzt werden können“, meint Johanna Drögemüller M.Sc., die Erstautorin des Beitrags in Structure.
Eine weitere strukturelle Besonderheit
Die kristallographischen Analysen in Berlin haben gezeigt, dass das Protein NusG in den hitzebeständigen Bakterien der Spezies Thermotoga maritima noch eine andere strukturelle Besonderheit aufweist: Die aminoterminale Domäne enthält ihrerseits eine strukturelle Untereinheit. Welche Funktionen dieses Strukturelement hat, ist bisher allerdings noch ungeklärt.
Veröffentlichung:
Drögemüller et al.
An Autoinhibited State in the Structure of Thermotoga maritima NusG.
Structure 2013, DOI: 10.1016/j.str.2012.12.015
Ansprechpartner:
Dr. Kristian Schweimer
Universität Bayreuth
Lehrstuhl für Biopolymere
D-95440 Bayreuth
Telefon: +49 (0) 921 55 3543
E-Mail: kristian.schweimer@uni-bayreuth.de
Media Contact
Weitere Informationen:
http://www.uni-bayreuth.deAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Diamantstaub leuchtet hell in Magnetresonanztomographie
Mögliche Alternative zum weit verbreiteten Kontrastmittel Gadolinium. Eine unerwartete Entdeckung machte eine Wissenschaftlerin des Max-Planck-Instituts für Intelligente Systeme in Stuttgart: Nanometerkleine Diamantpartikel, die eigentlich für einen ganz anderen Zweck bestimmt…

Neue Spule für 7-Tesla MRT | Kopf und Hals gleichzeitig darstellen
Die Magnetresonanztomographie (MRT) ermöglicht detaillierte Einblicke in den Körper. Vor allem die Ultrahochfeld-Bildgebung mit Magnetfeldstärken von 7 Tesla und höher macht feinste anatomische Strukturen und funktionelle Prozesse sichtbar. Doch alleine…

Hybrid-Energiespeichersystem für moderne Energienetze
Projekt HyFlow: Leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem für moderne Energienetze. In drei Jahren Forschungsarbeit hat das Konsortium des EU-Projekts HyFlow ein extrem leistungsfähiges, nachhaltiges und kostengünstiges Hybrid-Energiespeichersystem entwickelt, das einen…





















