Überlebensstrategie des Tuberkuloseerregers aufgedeckt

Der Tuberkuloseerreger M. tuberculosis besitzt die aussergewöhnliche Fähigkeit, sich innerhalb von Fresszellen (so genannten Makrophagen) zu verstecken, ohne vernichtet zu werden. Dort kann sich das Bakterium über lange Zeit unbehelligt verbergen, und die Krankheit bricht erst aus, wenn der Gesundheitszustand des Wirts beeinträchtigt ist. Diese Persistenz ist mit ein Grund, weshalb durch Tuberkulose mehr Menschen sterben als durch jeden anderen bakteriellen Krankheitserreger.
Normalerweise werden Bakterien im Inneren der Makrophagen von so genannten Phagosomen aufgenommen und an bestimmte Zellorganellen (Lysosomen) weitergereicht, die die Erreger verdauen. M. tuberculosis hat indes eine sehr effektive Strategie entwickelt, um gegen diese Immunabwehr zu bestehen, indem es seine Auslieferung an die Lysosomen verhindert und in den einigermassen komfortablen Phagosomen überlebt.
Bereits 1999 hatten Prof. Dr. Jean Pieters und sein damaliger Forschungsassistent Giorgio Ferrari ein Protein namens TACO identifiziert (heute als coronin 1 bezeichnet), von dem sie vermuteten, dass es die Auslieferung der Krankheitserreger an die Lysosomen verhindert. „Nun ging es um den Nachweis, dass TACO/coronin 1 der entscheidende Faktor für das Überleben von M. tuberculosis war“, erläutert Pieters. Denn andere Forschungsergebnisse legten nahe, dass dieses Protein vielmehr die Regulierung der Zellstruktur beeinflusst.
Der Doktorand Jan Massner entwickelte deshalb zusammen mit der Transgenic Mouse Core Facility am Biozentrum ein Mausmodell ohne das coronin 1-Protein. Und gleich, welchen Aspekt der Zellstruktur die Basler Wissenschaftler analysierten, zeigte sich kein Unterschied zwischen Tieren mit und ohne coronin 1.
Also fuhr das Forscherteam – verstärkt durch die beiden Postdocs Rajesh Jayachandran und Varadha Sundaramurthy – fort, die Rolle des Proteins beim Überleben von M. tuberculosis im Labor zu untersuchen. Mit ausgefeilten Experimentanlagen gelang schliesslich der Nachweis: Wenn coronin 1 fehlt, hat M. tuberculosis keine Chance. Die Bakterien werden unverzüglich zu den Lysosomen transportiert und zerstört.
Doch damit war noch nicht erklärt, wie die Anwesenheit von coronin 1 den Abbau von M. tuberculosis blockiert. Eine wichtige Idee lieferte schliesslich Rajesh Jayachandran, der vorschlug, bei der Infektion der Zellen mit den Mykobakterien die beiden Substanzen Cyclosporin A und FK506 (Tacrolimus) hinzuzufügen. Diese zwei Wirkstoffe sind gebräuchlich, um das Signalmolekül Calcineurin zu blockieren. Die Resultate waren erstaunlich: Der Zusatz der Calcineurinhemmer imitierte die Beseitigung von coronin 1 perfekt. Das wies darauf hin, dass coronin 1 das Signalmolekül Calcineurin aktiviert, um den Transport der Erreger zu den Lysosomen zu unterbinden.
Nun galt es zu zeigen, ob die Behandlung infizierter Mäuse mit Calcineurinhemmern das Verhalten von M. tuberculosis beeinflusst. Diese Experimente wurden in einem speziellen Biosicherheitslabor am Institut Pasteur in Brüssel durchgeführt. Und tatsächlich: Während die Tuberkelbakterien bei den unbehandelten Mäusen fern der Lysosomen verharrten, wurden sie bei den Tieren, die Calcineurinhemmer erhalten hatten, unverzüglich an die Lysosomen weitergereicht. Damit war der Nachweis erbracht, dass sich M. tuberculosis den Signalweg von Calcineurin für sein Überleben im Zellinnern zunutze macht.
Die Forschungsergebnisse eröffnen neue Perspektiven zur Bekämpfung von Tuberkulose, auch wenn es bis zu Präparaten für eine Behandlung der Krankheit noch ein weiter Weg ist. „Was wir jetzt in der Hand haben, ist ein komplett neuer und unerwarteter Pfad, von dem wir wissen, dass wir über ihn kleine Moleküle zu den Zielzellen hin schleusen können. Eine unserer künftigen Herausforderungen wird es sein, die einzelnen Prozesse besser zu verstehen und zu begreifen, welche Elemente sie in Gang setzen und stoppen“, so Pieters.
Die Forschungsarbeit wurde unterstützt durch Beiträge des Schweizerischen Nationalfonds zur Förderung der wissenschaftlichen Forschung, der Weltgesundheitsorganisation WHO, der Roche Research Foundation, der Olga-Mayenfisch-Stiftung und der Jubiläumsstiftung für Volksgesundheit und medizinische Forschung der Schweizerische Lebensversicherungs- und Rentenanstalt (Swiss Life).
Weitere Auskünfte
Prof. Dr. Jean Pieters, Biozentrum der Universität Basel, Klingelbergstrasse 50, 4056 Basel, Tel. +41 61 267 14 94, mobil: +41 79 749 01 15, E-Mail: jean.pieters@unibas.ch
Originalbeitrag
Rajesh Jayachandran et al.
Survival of Mycobacteria in Macrophages is Mediated by Coronin 1 Dependent Activation of Calcineurin
„Cell“ published July 13, 2007
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge
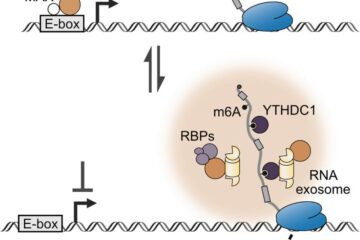
Forschende enthüllen neue Funktion von Onkoproteinen
Forschende der Uni Würzburg haben herausgefunden: Das Onkoprotein MYCN lässt Krebszellen nicht nur stärker wachsen, sondern macht sie auch resistenter gegen Medikamente. Für die Entwicklung neuer Therapien ist das ein…

Mit Kleinsatelliten den Asteroiden Apophis erforschen
In fünf Jahren fliegt ein größerer Asteroid sehr nah an der Erde vorbei – eine einmalige Chance, ihn zu erforschen. An der Uni Würzburg werden Konzepte für eine nationale Kleinsatellitenmission…

Zellskelett-Gene regulieren Vernetzung im Säugerhirn
Marburger Forschungsteam beleuchtet, wie Nervenzellen Netzwerke bilden. Ein Molekülpaar zu trennen, hat Auswirkungen auf das Networking im Hirn: So lässt sich zusammenfassen, was eine Marburger Forschungsgruppe jetzt über die Vernetzung…