Licht steuert Nervenzellen
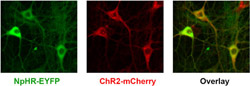
Hippocampus-Neuronen mit Halorhodopsin (NpHR) gekoppelt an einen gelb fluoreszierenden Farbstoff (eYFP) bzw. mit Channelrhodopsin-2 (ChR2) gekoppelt an einen rot fluoreszierenden Farbstoff (mCherry). Bild: Zhang et al., 2007
Als Schalter fungieren dabei ein aus einer Alge stammender lichtaktivierbarer Ionenkanal sowie eine ebenso durch Licht gesteuerte Ionenpumpe aus einem Archaebakterium. Beide gehören zur Klasse der mikrobiellen Rhodopsine, in die – wie beim Sehpurpur im menschlichen Auge – der Chromophor Retinal eingebunden ist. Die entsprechenden Gene wurden in Nervenzellen eingeschleust und führten dort zur Bildung funktioneller Proteine. Durch gezielte Aktivierung der Rhodopsine mit Licht unterschiedlicher Wellenlänge (d.h. Farbe) konnten die Forscher die Zellen unabhängig voneinander an- und abschalten. Durch diese elegante Manipulation der neuronalen Botschaften wird es nun möglich, die Rolle bestimmter Zellen in neuronalen Netzen zu erforschen. Die Wissenschaftler konnten ihr neues Werkzeug bereits am lebenden Tier testen: dem kleinen Fadenwurm C. elegans (Nature, 5. April 2007).
Das menschliche Gehirn ist das wohl faszinierendste Organ – die Frage, wie Informationen im Gehirn niedergelegt sein könnten und wie das Gehirn auf die Daten in diesem riesigen Informationsspeicher zugreift, beschäftigt die Menschheit schon seit langem. Erkenntnisfortschritte wurden oft mit neuen Techniken gewonnen, zu denen neben den verfeinerten elektrophysiologischen Methoden vor allem bildgebende, sogenannte Imaging-Verfahren gehören. Dennoch fehlte es bisher an geeigneten Werkzeugen, mit denen man Nervenzellen im intakten Hirngewebe nicht-invasiv präzise an- und abschalten kann, um ihren Beitrag im neuronalen Netzwerk nachzuweisen.
Zwei unscheinbare Mikroben haben den Wissenschaftlern vom Max-Planck-Institut für Biophysik in Frankfurt/Main und ihren Kollegen von der Univ. Frankfurt und der Stanford University in USA nun weitergeholfen: Dabei handelt es sich um das Archaebakterium Natronomonas pharaonis sowie die kleine Grünalge Chlamydomonas reinhardtii. Chlamydomonas besitzt einen als Channelrhodopsin-2 bezeichneten Ionenkanal (ChR2), der ursprünglich 2003 am Max-Planck-Institut für Biophysik charakterisiert wurde. Überträgt man das entsprechende Gen per Virus-Shuttle in Nervenzellen, so lässt sich der Kanal dort durch Licht in einem bestimmten Wellenlängenbereich (blau) aktivieren. Der daraus resultierende Einwärtsstrom von Kationen führt zu einer Depolarisation der Zellen und damit zur Auslösung von Aktionspotenzialen (Spikes) – die Nervenzellen werden quasi angeschaltet. Sobald der Lichtpuls aussetzt, schließt sich der Kanal wieder. Die elektrischen Botschaften der Nervenzellen – kodiert in der Spike-Frequenz – können also durch einen einfachen Lichtpuls gesteuert werden. Bereits 2005 hatten Alexander Gottschalk von der Universität Frankfurt, Georg Nagel – damals noch in der Abteilung Biophysikalische Chemie des Max-Planck-Instituts für Biophysik – und Ernst Bamberg (Direktor am MPI für Biophysik) mit ihren jeweiligen Mitarbeitern gezeigt, dass sich auf diese Weise in dem kleinen Fadenwurm Caenorhabditis elegans sogar Verhaltensantworten auslösen lassen.
Diese Vorgehensweise erlaubte jedoch nur eine Aktivierung der Zellen. Auf der Wunschliste der Forscher ganz oben stand daher ein Werkzeug, das es ermöglicht, Nervenzellen mit der gleichen zeitlichen Präzision, nämlich innerhalb von Millisekunden, abzuschalten – und zwar über einen Lichtpuls anderer Farbe. Im Fokus der Forscher: die Chloridpumpe Halorhodopsin. Ernst Bamberg hatte dieses Protein bereits früher mit Hilfe elektrischer Methoden detailliert auf seine Transporteigenschaften untersucht, und Georg Nagel war es in der Folge gelungen, Halorhodopsin aus Natronomonas pharaonis (NpHR) erstmals in tierischen Zellen zu exprimieren. Wurden die Zellen mit gelbem Licht beleuchtet, so kam es zu einem Einwärtsstrom von Chloridionen und infolgedessen zu einer Hyperpolarisation, die Aktionspotenziale hemmt.
Damit war der Grundstein für die vorliegende Nature-Veröffentlichung gelegt. Die Kollegen in Stanford fusionierten das NpHR-Gen mit einem fluoreszierenden Protein (eYFP) und schleusten es wiederum per Virus-Shuttle in kultivierte Hippocampus-Nervenzellen ein. Sie konnten nun mit gelbem Licht einzelne Aktionspotenziale ebenso wie eine ganze Salve von Spikes unterbinden. In einem nächsten Schritt verknüpften sie Channelrhodopsin-2 mit einer rot fluoreszierenden Protein-Variante (mCherry) und koexprimierten den Kanal aus der Alge und die Pumpe aus dem Archaebakterium in Hippocampus-Neuronen. Tatsächlich war es nun möglich, das Membranpotenzial in ein und demselben Neuron in beide Richtungen zu verändern: Blaue Lichtpulse lösten durch Aktivierung von ChR2 Aktionspotenziale aus, während gelbe Lichtpulse durch Aktivierung von NpHR die Aktionspotenziale löschten. „Dabei werden die grundlegenden elektrischen Eigenschaften der Zelle nicht beeinträchtigt“, betont Georg Nagel, der heute eine Professur an der Universität Würzburg innehat.
Eine wichtige, noch zu beantwortende Frage war, ob mit diesem System auch das Verhalten eines Tieres in vivo kontrolliert werden kann. Für Channelrhodopsin-2 war das ja bereits für die Taufliege Drosophila und den Fadenwurm C. elegans gezeigt worden. Wieder arbeiteten die Max-Planck-Wissenschaftler mit dem Team des C. elegans-Experten Alexander Gottschalk zusammen. Wurde die Chloridpumpe NpHR in Nerven- oder Muskelzellen von C. elegans exprimiert, so führte Lichtaktivierung zum unmittelbaren Stopp (innerhalb von 150 Millisekunden) der Schwimmbewegungen (siehe Movie 1). Nach Beendigung des Lichtreizes kehrte der kleine Fadenwurm zu seinem natürlichen Schwimmverhalten zurück. „Auch die gemeinsame Expression des Kationenkanals mit der Chloridpumpe in C. elegans war erfolgreich“, sagt Gottschalk.
„Das NpHR/ChR2-System erlaubt uns erstmals, Neuronen allein durch Licht auf einer Zeitskala von Millisekunden und mit extrem hoher räumlicher Auflösung, also im Mikrometerbereich, nicht-invasiv an- und abzuschalten. Damit kann durch die geeignete Wahl der Lichtpulssequenz der neuronale Code nachgeahmt oder verändert werden“, erklärt Ernst Bamberg. „Wir haben mit den beiden lichtschaltbaren Proteinen den Neurobiologen ein sehr vielseitig anwendbares Werkzeug in die Hand gegeben, mit dem sowohl in neuronalen Zellkulturen als auch in transgenen Tieren völlig neuartige Untersuchungen durchgeführt werden können.“
[CB]
Originalveröffentlichung:
Feng Zhang, Li-Ping Wang, Martin Brauner, Jana F. Liewald, Kenneth Kay, Natalie Watzke, Phillip G. Wood, Ernst Bamberg, Georg Nagel, Alexander Gottschalk & Karl Deisseroth; Multimodal fast optical interrogation of neural circuitry
Nature, 5. April 2007
Media Contact
Weitere Informationen:
http://www.mpg.deAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Neue universelle lichtbasierte Technik zur Kontrolle der Talpolarisation
Ein internationales Forscherteam berichtet in Nature über eine neue Methode, mit der zum ersten Mal die Talpolarisation in zentrosymmetrischen Bulk-Materialien auf eine nicht materialspezifische Weise erreicht wird. Diese „universelle Technik“…

Tumorzellen hebeln das Immunsystem früh aus
Neu entdeckter Mechanismus könnte Krebs-Immuntherapien deutlich verbessern. Tumore verhindern aktiv, dass sich Immunantworten durch sogenannte zytotoxische T-Zellen bilden, die den Krebs bekämpfen könnten. Wie das genau geschieht, beschreiben jetzt erstmals…

Immunzellen in den Startlöchern: „Allzeit bereit“ ist harte Arbeit
Wenn Krankheitserreger in den Körper eindringen, muss das Immunsystem sofort reagieren und eine Infektion verhindern oder eindämmen. Doch wie halten sich unsere Abwehrzellen bereit, wenn kein Angreifer in Sicht ist?…





















