Vom Speisepilz zum maßgeschneiderten Biokatalysator
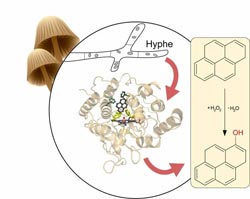
Struktur und Wirkungsweise von AaeAPO<br>Quelle: Eric Strittmatter<br>
Aromaten sind Kohlenwasserstoffe, die in der chemischen und pharmazeutischen Industrie jedes Jahr im Megatonnenmaßstab eingesetzt werden. Prof. Dr. Dietmar A. Plattner, Dr. Klaus Piontek und Eric Strittmatter vom Institut für Organische Chemie der Universität Freiburg ist es nun gelungen, die Struktur eines Enzyms aufzuklären, das Aromaten selektiv nur mithilfe von Wasserstoffperoxid aktivieren kann.
Die Struktur dient als Basis, um die Funktionsweise des Enzyms auf molekularer Ebene im Detail zu verstehen. In Zusammenarbeit mit Wissenschaftlerinnen und Wissenschaftlern vom Internationalen Hochschulinstitut der Universität Dresden in Zittau und von der Hochschule Lausitz in Senftenberg hat das Team die Ergebnisse dieser Arbeiten jetzt in der Fachzeitschrift „Journal of Biological Chemistry“ veröffentlicht. Die Forscher um Plattner hoffen, mit diesem Katalysatorsystem zukünftig eine Alternative zu den oft energie- und abfallintensiven Methoden der Industrie bereitzustellen.
Das Enzym mit dem Namen AaeAPO gehört zur Gruppe der so genannten aromatischen Peroxygenasen, kurz APOs. Es wird aus dem bekannten Speise- und Kulturpilz Agrocybe aegerita, dem Südlichen Ackerling – auch Pioppino genannt – gewonnen. Die biologische Rolle des Enzyms ist noch nicht geklärt: Es dient vermutlich als eine Art „extrazelluläre Leber“ des Pilzes und ist für den Abbau schädlicher Substanzen verantwortlich. AaeAPO kann beispielsweise krebserregende Aromaten wie Methylimidazol umsetzen und deren Giftigkeit und Löslichkeitseigenschaften nachhaltig verändern.
APOs wirken als Katalysatoren bei der chemischen Modifikation von Aromaten durch Wasserstoffperoxid, das heißt, sie machen diese chemische Reaktion möglich. Wasserstoffperoxid, ein aus Alltagsanwendungen bekanntes Bleichmittel, ist günstig herstellbar. Das ist einer der Gründe dafür, dass APOs attraktive Katalysatoren für schwierige chemische Synthesen sind. Zu ihren weiteren positiven Eigenschaften gehören hohe Löslichkeit sowie die Stabilität bei verschiedenen pH- und Temperaturwerten. Zusätzlich weisen APOs einen hohen Grad an Selektivität auf, was bedeutet, dass sie Sauerstoffatome aus Wasserstoffperoxid an genau definierten Stellen im Molekül einbauen. Dabei sind sie den industriell eingesetzten Cytochrom-P450-Monooxygenasen deutlich überlegen. Diese verlieren außerdem als Katalysatoren schneller ihre Enzymaktivität als APOs und funktionieren nur in zellulärer Umgebung, was ihre industrielle Anwendung erschwert.
Die Arbeitsweise von AaeAPO hängt unmittelbar mit seiner Struktur zusammen: Das Enzym besitzt eine für aromatische Substrate, also von AaeAPO umsetzbare Verbindungen, passende Bindungstasche, die nach dem Prinzip eines Spannrings die Substratmoleküle fixiert. Dadurch kann ein in das Enzym eingebettetes Häm-Molekül, bekannt aus dem roten Blutfarbstoff, ein Sauerstoffatom auf den Aromaten übertragen. Dieser Vorgang läuft in wässriger Umgebung und bereits bei Raumtemperatur effizient ab, also unter Bedingungen, bei denen die enzymfreie Reaktion niemals stattfindet. Durch gezielte Modifikation der Bindungstasche können zukünftig die katalytischen Eigenschaften des Enzyms verändert werden, um zum Beispiel das Substratspektrum zu variieren. AaeAPO wird so zum Prototyp einer ganzen Familie maßgeschneiderter Biokatalysatoren, die auf verschiedenen Gebieten eingesetzt werden können.
Weitere Informationen:
http://bioindustrie2021.eu
Originalveröffentlichung:
Klaus Piontek, Eric Strittmatter, René Ullrich, Glenn Gröbe, Marek J. Pecyna, Martin Kluge, Katrin Scheibner, Martin Hofrichter und Dietmar A. Plattner (2013). Structural Basis of Substrate Conversion in a New Aromatic Peroxygenase: P450 Functionality with Benefits. Journal of Biological Chemistry 288 (48). www.jbc.org/content/early/2013/10/14/jbc.M113.514521
Kontakt:
Prof. Dr. Dietmar A. Plattner
Institut für Organische Chemie
Albert-Ludwigs-Universität Freiburg
Tel.: 0761/203- 6013
Fax: 0761/203- 8714
E-Mail: dietmar.plattner@chemie.uni-freiburg.de
Dr. Klaus Piontek
Institut für Organische Chemie
Albert-Ludwigs-Universität Freiburg
Tel.: 0761/203- 6036
E-Mail: klaus.piontek@ocbc.uni-freiburg.de
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Merkmale des Untergrunds unter dem Thwaites-Gletscher enthüllt
Ein Forschungsteam hat felsige Berge und glattes Terrain unter dem Thwaites-Gletscher in der Westantarktis entdeckt – dem breiteste Gletscher der Erde, der halb so groß wie Deutschland und über 1000…

Wasserabweisende Fasern ohne PFAS
Endlich umweltfreundlich… Regenjacken, Badehosen oder Polsterstoffe: Textilien mit wasserabweisenden Eigenschaften benötigen eine chemische Imprägnierung. Fluor-haltige PFAS-Chemikalien sind zwar wirkungsvoll, schaden aber der Gesundheit und reichern sich in der Umwelt an….

Das massereichste stellare schwarze Loch unserer Galaxie entdeckt
Astronominnen und Astronomen haben das massereichste stellare schwarze Loch identifiziert, das bisher in der Milchstraßengalaxie entdeckt wurde. Entdeckt wurde das schwarze Loch in den Daten der Gaia-Mission der Europäischen Weltraumorganisation,…