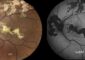
Reprogrammierung von Fruchtwasser-Stammzellen in Richtung Pluripotenz

Humane mesenchymale Fruchtwasser-Stammzellen kultiviert unter pluripotenten Bedingungen Hawkins et al.
Fruchtwasser-Stammzellen können bei der Geburt leicht isoliert werden, ohne das Baby oder die Mutter in Gefahr zu bringen. Obwohl diese Zellen primitiv sind und die Möglichkeit besitzen, zu verschiedenen Zelltypen zu werden, haben sie nicht die Möglichkeit zu jedem Zelltyp des Körpers zu werden (was als „Pluripotenz“ bezeichnet wird).
Embryonale Stammzellen sind pluripotent, weil Schlüssel-Gene wie OCT4, SOX2 und NANOG, exprimiert sind. Diese Gene werden fortschreitend während der frühen Entwicklung „ausgeschaltet“. Obwohl es unbekannt bleibt, wie diese ausgeschalteten Gene reaktiviert werden, demonstrierte die Pionier-Arbeit des Nobelpreis-Gewinners Shinya Yamanaka im Jahr 2007, dass das Einsetzen neuer Pluripotenz-Gene in das Genom der differenzierten Zellen die Zellen zurück zur Pluripotenz verjüngen konnte.
Eine Studie aus dem Jahr 2012 unter der Leitung von Dr. Pascale Guillot, einer Dozentin an dem University College London (UCL), Institut für Frauenheilkunde (UK), in Zusammenarbeit mit Professor Paolo De Coppi von dem UCL Great Ormond Street Institut für Kinderheilkunde, und Professor James Adjaye von dem Institut für Stammzellforschung und Regenerative Medizin, Medizinische Fakultät der Heinrich-Heine Universität, Düsseldorf, war die erste, die zeigte, dass humane Fruchtwasser-Stammzellen zu embryonalen Stammzellen verjüngt werden konnten, indem mit Chemikalien einige endogene Pluripotenz-Gene reaktiviert wurden. Aber die Autoren fanden auch heraus, dass die chemisch verjüngten Zellen genetisch unterschiedlich von den embryonalen Stammzellen blieben (Mol Ther. 2012;20(10):1953-67).
In einem zweiten mit Professor Paolo De Coppi und Professor James Adjaye in Molecular Therapy veröffentlichten aktuellen Artikel untersucht das Team von Dr. Pascale Guillot, was eine Zelle braucht, um ohne jegliche genetische Manipulation die Fähigkeit zurückzugewinnen, als embryonale Stammzelle zu funktionieren.
Die Autoren machten einen großen Schritt vorwärts, indem sie mit Einzel-Zell-Analyse zeigten, dass allein das reaktivierende endogene OCT4-Gen mit Chemikalien ausreicht, um spezifische Signalwege zu aktivieren, die die embryonale Funktion hervorbringen. Pascale Guillot kommentierte: „Die Zellen brauchen nicht die gleichen Gene wie embryonale Stammzellen zu exprimieren, um wie sie zu funktionieren.
Aber wir konnten zeigen, dass sie immer noch das spezifische Gen OCT4 exprimieren müssen und wir konzentrierten uns darauf, dieses Gen, das in den Zellen ausgeschaltet war, durch kleine Moleküle aufzuwecken. OCT4 funktioniert wie ein Starter, der andere in Pluripotenz involvierte Gene aufweckt, so dass die Zellen beginnen, sich zu verhalten, als wären sie jünger. Sie sehen anders als embryonale Stammzellen aus, sie exprimieren andere Gene, aber sie erlangen Pluripotenz als eine Funktion.“
Diese bahnbrechende Entdeckung zeigt, dass die Bemühungen, andere Zelltypen chemisch zur Pluripotenz zurückzubringen sich auf das Screening und Testen von OCT4-Modulatoren konzentrieren müssen.
Insbesondere zeigten die Autoren auch, dass einige der in diesen Signalweg involvierten Gene schon mit dem Pluripotenz-Phenotyp assoziiert worden sind, aber die molekulare Signatur der chemisch reprogrammierten Zellen unterstreicht auch, dass sie Zellen nicht wie embryonale Stammzellen „aussehen“ müssen, um wie sie zu funktionieren, denn die meisten Zellen in der Kultur revertierten in 2 Wochen zur Pluripotenz.
Prof. de Coppi kommentierte, dass “diese wichtige Arbeit helfen sollte, das einmalige Potenzial der Fruchtwasser-Stammzellen zu verstehen und uns bei Zellersatztherapien für Babys mit angeborenen Fehlbildungen einen Schritt weiterzubringen „ und Prof. Adjaye kam zu dem Schluss, dass „unsere Studie die Bedeutung des Aufbaus einer HLA homozygoten Fruchtwasser-iPSC-Stammzellbank für künftige Anwendungen in regenerativer Medizin und Drug-Screening unterstreicht.“ (HLA: Human Leukocyte Antigen; iPSC: induzierte pluripotente Stammzellen)
Artikel: Hawkins,K, Moschidou, D, Faccenda, Wruck, W, Martin-Trujillo, A, Kwan-Leong, H, Maria Ranzoni, A,Sanchez-Freire, V, Tommasini,F, Eaton, S, De Coppi, P, Monk, D, Campanella, M, Thrasher,AJ, Adjaye, J, and Guillot, PV. (2017). Human amniocytes are receptive to chemically-induced reprogramming to pluripotency. Molecular Therapy. DOI 10.1016/j.ymthe.2016.11.014
Media Contact
Weitere Informationen:
http://www.hhu.de/Alle Nachrichten aus der Kategorie: Medizin Gesundheit
Dieser Fachbereich fasst die Vielzahl der medizinischen Fachrichtungen aus dem Bereich der Humanmedizin zusammen.
Unter anderem finden Sie hier Berichte aus den Teilbereichen: Anästhesiologie, Anatomie, Chirurgie, Humangenetik, Hygiene und Umweltmedizin, Innere Medizin, Neurologie, Pharmakologie, Physiologie, Urologie oder Zahnmedizin.
Neueste Beiträge

Neue universelle lichtbasierte Technik zur Kontrolle der Talpolarisation
Ein internationales Forscherteam berichtet in Nature über eine neue Methode, mit der zum ersten Mal die Talpolarisation in zentrosymmetrischen Bulk-Materialien auf eine nicht materialspezifische Weise erreicht wird. Diese „universelle Technik“…

Tumorzellen hebeln das Immunsystem früh aus
Neu entdeckter Mechanismus könnte Krebs-Immuntherapien deutlich verbessern. Tumore verhindern aktiv, dass sich Immunantworten durch sogenannte zytotoxische T-Zellen bilden, die den Krebs bekämpfen könnten. Wie das genau geschieht, beschreiben jetzt erstmals…

Immunzellen in den Startlöchern: „Allzeit bereit“ ist harte Arbeit
Wenn Krankheitserreger in den Körper eindringen, muss das Immunsystem sofort reagieren und eine Infektion verhindern oder eindämmen. Doch wie halten sich unsere Abwehrzellen bereit, wenn kein Angreifer in Sicht ist?…