Von Hefe für Demenzerkrankungen lernen
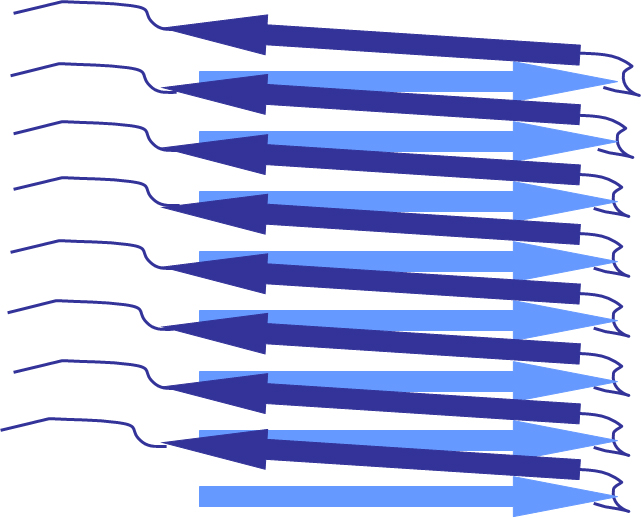
Schematische Darstellung von Amyloid-Fibrillen mit parallel verlaufenden beta-Faltblättern, wie sie auch in dem untersuchten Prion vorliegen. HHU / Henrike Heise
Biophysiker der Heinrich-Heine-Universität Düsseldorf (HHU) und des Forschungszentrums Jülich (FZJ) untersuchten zusammen mit japanischen Kollegen die Faltung bestimmter Proteine bei Hefepilzen. Sie fanden ähnliche Mechanismen wie bei sogenannten Prionen, also solchen Eiweißen, die fehlgefaltet sind und die neurodegenerative Erkrankungen auslösen. Mit den Prionen in Hefen gewannen die Forscher neue Erkenntnisse über die Entstehung der schädlichen Eiweiße. Sie veröffentlichten ihre Ergebnisse in der Fachzeitschrift Proceedings of the National Academy of Sciences (PNAS).
Proteine sind zentrale Bausteine jedes lebenden Organismus, sie dienen sowohl als Strukturmaterial als auch als Botenstoffe im Körper. Diese Proteine setzen sich ihrerseits aus einzelnen Aminosäurebausteinen zusammen. Der Bauplan, nach dem der Körper sie herstellt, ist im genetischen Code hinterlegt.
Die Proteine, die zum Teil aus hunderten bis tausenden Aminosäuren bestehen, sind komplex gefaltete dreidimensionale Gebilde. Ihre Struktur ist von entscheidender Bedeutung für ihre Funktion. Kommt es zu Faltungsfehlern, verlieren die Proteine nicht nur ihre biologische Funktion; sie können unter anderem auch neurodegenerative Erkrankungen verursachen.
Für die Rinderkrankheit BSE beziehungsweise die Creutzfeld-Jakob-Erkrankung beim Menschen sind Prionen verantwortlich, Aggregate aus fehlgefalteten körpereigenen Proteinen. Diese sind in der Lage, ihre falsche Struktur auf andere Proteine zu übertragen und sind damit ansteckend. Prionen können Nervengewebe zerstören.
Auch in Hefen gibt es Proteine, die – wie bei den Krankheitserregern beim Tier und Menschen – infektiöse Zusammenlagerungen, Prionen, bilden können. Hefen eignen sich deshalb gut als Studienobjekt, um zentrale Mechanismen bei den humanen Krankheiten zu untersuchen. Die Arbeitsgruppe um Prof. Dr. Henrike Heise vom Institut für Physikalische Biologie der HHU und vom Institute for Complex Systems – Strukturbiochemie des FZJ untersuchte zusammen mit Kollegen des japanischen RIKEN-Forschungsinstituts mit Hilfe der Kernspinresonanztomografie die Strukturen verschiedener Stämme der Prionen, die vom N-terminalen Fragment Sup35NM des Hefeprions Sup35p gebildet werden. Vor allem wollten die Wissenschaftler klären, welchen Einfluss Umweltbedingungen oder genetische Faktoren auf die Struktur der Prionen und damit auf ihre spezifischen Eigenschaften wie Infektiosität haben.
Nachdem bereits in früheren Versuchen gezeigt worden war, dass thermodynamische Faktoren wie die Umgebungstemperatur zu verschiedenen Prionenstämmen mit unterschiedlichen Strukturen und Eigenschaften führen können, untersuchten die Forscherinnen und Forscher in der aktuellen Studie eine Punktmutation, in der eine einzige Aminosäure im Zentrum des fehlgefalteten Bereiches – des Amyloid-Kernbereiches – durch eine andere ersetzt ist.
Dieser einzelne Aminosäureaustausch führt dazu, dass das mutierte Protein zwar auch Prionen bilden kann, die sich in ihren Eigenschaften allerdings deutlich von den Prionen des ursprünglichen „Wildtyp“-Proteins unterscheiden. Unabhängige Untersuchungen durch Proteinverdau-Experimente – Protein-abbauende Enzyme „verdauen“ dabei alle nicht zum Amyloidkern gehörenden Bereiche, so dass nur der Kernbereich zurückbleibt – sowie durch Festkörper-Kernspinresonanzspektroskopie zeigten, dass der Amyloid-Kernbereich der Prionen, die vom mutierten Sup35NM-Protein gebildet werden, in einer Region liegt, die im Wildtyp-Prion nicht zum Amyloid-Kernbereich gehört. Weiterhin fand man, dass diese Proteinmutante bereits im ungefalteten Zustand weniger kompakt ist, was letztendlich Auswirkungen auf die Zusammenlagerung der Proteine hat.
Dies sind wichtige Erkenntnisse für das Verständnis der Bildung von fehlerhaften und krankmachenden Proteinstrukturen. Auf dieser Grundlage kann es auch möglich sein, neue Therapieansätze zu finden. Neben der Creutzfeld-Jakob-Krankheit ist dies auch für andere neurologische Erkrankungen wie die Alzheimer-Demenz oder Parkinson relevant, da auch diese von fehlerhaft aufgebauten Proteinen verursacht werden, die sich verklumpen und in der Folge Nervenzellen schädigen können.
Originalveröffentlichung
Yumiko Ohhashi, Yoshiki Yamaguchi, Hiroshi Kurahashi, Yuji Kamatari, Shinju Sugiyama, Boran Uluca, Timo Piechatzek, Yusuke Komi, Toshinobu Shida, Henrik Müller, Shinya Hanashima, Henrike Heise, Kazuo Kuwata, Motomasa Tanaka, Molecular basis for diversification of yeast prion strain conformation, PNAS, 21. Februar 2018
DOI: 10.1073/pnas.1715483115
Online: http://www.pnas.org/content/early/2018/02/20/1715483115
Media Contact
Weitere Informationen:
http://www.hhu.de/Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Merkmale des Untergrunds unter dem Thwaites-Gletscher enthüllt
Ein Forschungsteam hat felsige Berge und glattes Terrain unter dem Thwaites-Gletscher in der Westantarktis entdeckt – dem breiteste Gletscher der Erde, der halb so groß wie Deutschland und über 1000…

Wasserabweisende Fasern ohne PFAS
Endlich umweltfreundlich… Regenjacken, Badehosen oder Polsterstoffe: Textilien mit wasserabweisenden Eigenschaften benötigen eine chemische Imprägnierung. Fluor-haltige PFAS-Chemikalien sind zwar wirkungsvoll, schaden aber der Gesundheit und reichern sich in der Umwelt an….

Das massereichste stellare schwarze Loch unserer Galaxie entdeckt
Astronominnen und Astronomen haben das massereichste stellare schwarze Loch identifiziert, das bisher in der Milchstraßengalaxie entdeckt wurde. Entdeckt wurde das schwarze Loch in den Daten der Gaia-Mission der Europäischen Weltraumorganisation,…