Tumoren gezielt attackieren
Ein neuartiger Ansatz verspricht in der Tumortherapie zukünftig eine selektivere und damit verträglichere Behandlung von Krebspatienten.<br><br>(c) Wiley-VCH<br>
Eine der größten Herausforderungen der Chemotherapie liegt darin, dass Krebszellen zwar wirksam abgetötet werden sollen, gesundes Gewebe dabei aber geschont werden soll.
In der Zeitschrift Angewandte Chemie stellen französische Forscher nun ein neues Konzept vor. Dabei wird der Wirkstoff durch das Enzym ?-Galaktosidase aus einer inaktiven Vorstufe, einem so genannten Prodrug, freigesetzt, das nur von Tumorzellen aufgenommen werden kann.
Inzwischen ist eine ganze Reihe von tumorspezifischen Markern bekannt, Rezeptoren, die in der Zellmembran von Tumorzellen gehäuft auftreten, auf der Oberfläche gesunder Zellen aber gar nicht oder nur in deutlich geringerer Konzentration vorhanden sind. Bisher wurden meist gegen sie gerichtete Antikörper verwendet, um Wirkstoffe selektiv zu Tumorzellen zu lotsen. Nachteile sind nicht nur die hohen Kosten und die aufwändige Entwicklung und Herstellung, sondern auch das damit verbundene Risiko von unerwünschten Immunantworten.
Das Team um Sébastien Papot von der Universität Poitiers hat jetzt einen einfacheren Ansatz entwickelt, der ohne Antikörper auskommt. Er basiert auf einem Prodrug aus vier Teilen: dem eigentlichen zytotoxischen Wirkstoff, einem Liganden, der einen der tumorspezifischen Rezeptoren erkennt, einem „Auslöser“ für die Freisetzung und einem Verbindungsstück, das alle Teile zusammenhält.
Im ersten Schritt bindet der Ligand an den tumorspezifischen Rezeptor auf der Oberfläche einer Tumorzelle. Die Tumorzelle stülpt daraufhin die Zellmembran an dieser Stelle nach innen, bis ein Bläschen entsteht, in dem sich Rezeptor und Prodrug befinden, und holt dieses ins Zellinnere (Rezeptor-vermittelte Endozytose). Diese Bläschen fusionieren dann mit so genannten Lysosomen, Zellorganellen, die unter anderem das Enzym ?-Galaktosidase enthalten. Dieses Enzym spaltet Galaktose von Mehrfachzuckern (Polysacchariden) ab. Der Auslöser-Teil des Prodrug ist ein solcher Galaktose-Baustein. Sobald das Enzym ihn abspaltet, kommt es innerhalb des Verbindungsstücks zu einem spontanen Zerfall, bei dem der Wirkstoff freigesetzt und damit aktiviert wird. Der Wirkstoff inhibiert die Zellteilung der Tumorzelle und tötet sie auf diese Weise.
Außerdem gelangt der Wirkstoff aber auch aus der eigentlichen Tumorzelle heraus und wird von direkt benachbarten Zellen aufgenommen, auch wenn diese den tumorspezifischen Rezeptor gar nicht in ihrer Membran haben, und tötet sie ebenfalls ab. Das ist sinnvoll, denn Tumoren bestehen oft aus verschiedenen Zelltypen, die nicht alle den entsprechenden Rezeptor aufweisen müssen. Weiter entfernte gesunde Zellen werden dagegen nicht beeinträchtigt. Das Prodrug können sie ohne den speziellen Rezeptor nicht aufnehmen.
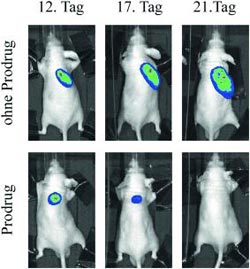
In ersten Tierversuchen zeigte sich ein Prodrug auf dieser Basis sehr wirksam. Die Tumoren schrumpften bei Behandlung mit dem Prodrug, während sich die Verabreichung des freien Zytostatikums als wenig wirksam erwies.
Angewandte Chemie: Presseinfo 39/2012
Autor: Sébastien Papot, Université de Poitiers (France), http://sfa.univ-poitiers.fr/m-papot-sebastien-172621.kjsp?RH=1268304565657
Angewandte Chemie, Permalink to the article: http://dx.doi.org/10.1002/ange.201204935
Angewandte Chemie, Postfach 101161, 69451 Weinheim, Germany.
Media Contact
Weitere Informationen:
http://presse.angewandte.de/Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Anlagenkonzepte für die Fertigung von Bipolarplatten, MEAs und Drucktanks
Grüner Wasserstoff zählt zu den Energieträgern der Zukunft. Um ihn in großen Mengen zu erzeugen, zu speichern und wieder in elektrische Energie zu wandeln, bedarf es effizienter und skalierbarer Fertigungsprozesse…

Ausfallsichere Dehnungssensoren ohne Stromverbrauch
Um die Sicherheit von Brücken, Kränen, Pipelines, Windrädern und vielem mehr zu überwachen, werden Dehnungssensoren benötigt. Eine grundlegend neue Technologie dafür haben Wissenschaftlerinnen und Wissenschaftler aus Bochum und Paderborn entwickelt….

Dauerlastfähige Wechselrichter
… ermöglichen deutliche Leistungssteigerung elektrischer Antriebe. Überhitzende Komponenten limitieren die Leistungsfähigkeit von Antriebssträngen bei Elektrofahrzeugen erheblich. Wechselrichtern fällt dabei eine große thermische Last zu, weshalb sie unter hohem Energieaufwand aktiv…





















