Mehr als nur ein Nervtöter: Atomare Struktur von Alzheimer-Protein APP aufgeklärt

Alzheimer ist die häufigste Form der Altersdemenz. Ausgelöst wird diese Krankheit durch unlösliche Eiweißbestandteile, die sich in der Umgebung von Nervenzellen ablagern und dort Plaques bilden.
Diese Proteinklumpen – auch Beta-Amyloide genannt – schädigen die Nervenzellen, bis diese schließlich absterben. Mittlerweile ist bekannt, dass diese neurotoxischen Eiweißablagerungen aus Spaltprodukten eines bestimmten Makromoleküls bestehen, das auf der Membran von Nervenzellen zu finden ist. Amyloid-Vorläufer-Protein (APP) wird dieses Membranmolekül genannt.
„Es ist unwahrscheinlich, dass der biologische Sinn dieses Membranmoleküls darin besteht, Plaques zu bilden, Nervenzellen zu töten und damit eine der schlimmsten Formen von Demenz auszulösen. Man vermutet, dass dies eher ein unerwünschter Nebeneffekt ist“, sagt Dr. Manuel Than. Der Forschungsgruppenleiter vom Leibniz-Institut für Altersforschung, Fritz-Lipmann-Institut in Jena – analysiert mit seinem Team die atomare Struktur des Amyloid-Vorläufer-Proteins, um dessen biologische Grundfunktionen ergründen zu können.
Den Jenaer Forschern ist es gelungen, einen wesentlichen Teil dieses Proteins – die so genannte E1-Domäne – zu kristallisieren und dessen atomare Struktur aufzuklären. Durch Bestrahlung von Proteinkristallen mit Röntgenstrahlung erzeugen die Wissenschaftler sogenannte „Beugungsdaten“. Durch ein computergestütztes Verfahren werden diese dann in ein hochaufgelöstes, dreidimensionales Abbild oder „Modell“ des Moleküls umgewandelt. Dieses Modell beschreibt den atomaren Aufbau und die räumliche Struktur des Moleküls. So zeigte sich, dass die E1-Domäne eine starre Faltungseinheit bildet. „Anders als bisher angenommen, stellen die bisher bekannten Funktionsabschnitte, eine Kupferbindungsstelle und ein Wachstumsfaktor-ähnlicher Abschnitt, eine funktionale Einheit dar“, sagt Than.
„Form follows function“ – die Form bestimmt die Funktion – lautet dabei der Leitsatz der Wissenschaftler. „Solche Makromoleküle sind nicht nur spezifisch gefaltet, sie bilden auch ganz unterschiedliche Zusammenlagerungen. Und diese unterschiedlichen Molekülverbände nehmen im Organismus oft verschiedene physiologische Funktionen wahr“, erklärt der Wissenschaftliche Mitarbeiter Sven Dahms. So wird vermutet, dass APP eine Rolle bei der Interaktion zwischen Zellen spielt, aber auch bei der Kommunikation der Zelle mit ihrer Umgebung, der extrazellulären Matrix. Auch als Wachstumsfaktor sowie bei der Übertragung von Signalen in der Zelle scheint APP in Erscheinung zu treten. Womöglich ist das Molekül an der Kappung von Nervenfortsätzen, den Axonen, beteiligt und vermag damit neuronale Verknüpfungen aufzulösen. „Bisher gab es kaum Informationen über die Struktur dieses Membranmoleküls, die mit diesen unterschiedlichsten Funktionen in Verbindung gebracht werden konnten“, erläutert Than.
Das Amyloid-Vorläufer-Protein besteht aus drei Abschnitten, einem Transmembran-Teil, der beide Schichten der Zellmembran durchdringt, einem großen extrazellulären Abschnitt, der aus der Zelle herausragt sowie einem kleineren Bereich im Innern der Zelle. Die untersuchte E1-Domäne ist Teil des extrazellulären Abschnittes. Die Jenaer Proteinkristallographen haben nun herausgefunden, dass sich die E1-Domäne und in Konsequenz das gesamte Protein zu einem Doppelmolekül zusammenlagert, wenn der pharmakologische Wirkstoff Heparin zugegeben wird. Heparin-ähnliche Substanzen kommen im Körper als sogenannte Heparansulfate häufig vor. Als Bestandteil der extrazellulären Matrix sind sie also vor allem außerhalb der Zellen anzutreffen. Solche Doppelmoleküle, auch Dimere genannt, findet man häufig bei Rezeptoren, die bei der Signalübertragung mitwirken. Außerdem werden sie als verbindende Elemente bei der Zusammenlagerung von unterschiedlichen Zellen beobachtet. Die Jenaer Forscher sehen in der Heparin-abhängigen Dimerisierung einen strukturellen Hinweis auf die Rolle von APP bei der Signalübertragung bzw. Zelladhäsion.
Dieses Heparin-vermittelte E1-Dimer konnten die Forscher auch biochemisch nachweisen. Dabei zeigte sich zudem die pH-Abhängigkeit der Wechselwirkung zwischen den E1-Teilbereichen. „Die verschiedenen Erscheinungsformen und unterschiedlichen Funktionen von APP haben die Wissenschaft lange irritiert. Unsere Ergebnisse lassen nun vermuten, dass das Amyloid-Vorläufer-Protein an unterschiedlichen Stellen in der Zelle verschiedene Formen annimmt bzw. in verschiedenen Molekülverbänden auftritt und somit jeweils andere Funktionen erfüllen kann“, erklärt Biochemiker Dahms. Entscheidend für die jeweilige Struktur und Funktion sind womöglich die jeweiligen Zellbereiche und Organellen, in denen das APP seine Wirkung entfaltet. Auch von Gewebe zu Gewebe könnten sich Struktur und Funktion von APP ändern. Verantwortlich dafür sind höchst-wahrscheinlich variierende pH-Werte und Heparansulfatvorkommen.
„In Zukunft wird sich die Forschung daher darauf konzentrieren, die zellort- und organspezifischen Formen und Funktionen von APP aufzuklären“, sagt Than. Doch eines ist jetzt schon klar: APP ist weitaus mehr als nur ein neurotoxischer „bad guy“.
Kontakt:
PD Dr. Manuel E. Than
Leibniz-Institut für Altersforschung – Fritz-Lipmann-Institut (FLI)
Beutenbergstr. 11, D-07745 Jena
Tel. +49 3641 656170, Fax +49 3641 656335, than@fli-leibniz.de
Originalveröffentlichung:
Structure and biochemical analysis of the heparin-induced E1 dimer of the amyloid precursor pro-tein
Sven O. Dahms, Sandra Höfgen, Dirk Röser, Bernhard Schlott, Karl-Heinz Gührs, Manuel E. Than
PNAS, published online before print March 8, 2010, doi:10.1073/pnas.0911326107
Alzheimerforschung am FLI Jena:
Das Amyloid-Vorläufer-Protein (APP) ist durch seine Alzheimer auslösenden Spaltprodukte ein wichtiges Biomolekül des Alterns. Die röntgenkristallographische Aufklärung der atomaren Struktur und des räumlichen Aufbaus des APP-Moleküls wird langfristig dabei helfen, gezielte Alzheimer-Therapien zu entwickeln. Für das Fritz-Lipmann-Institut Jena bedeutet der Wiederaufbau der Proteinkristallographie durch die Arbeitsgruppe Than eine weitere Stärkung der strukturanalytischen Forschungsschwerpunkte in der Altersforschung.
Das Thema Neurodegeneration hat am FLI einen besonders hohen Stellenwert. „Wir bearbeiten dieses Feld mit mehreren Forschungsgruppen und verschiedenen Ansätzen. Forschungsfragen sind neben der Entstehung und Wirkung pathogener Alzheimerfibrillen, der Funktion APP-spaltender Enzyme und der Strukturaufklärung von APP auch die Verknüpfung neurodegenerativer Prozesse mit dem Hormonsystem und der DNA-Reparatur“, so Institutsleiter Prof. Dr. Peter Herrlich. Vernetzt sind diese Forschungsarbeiten auch mit klinisch orientierten Fragestellungen in der Neurologie des Universitätsklinikums Jena.
Media Contact
Weitere Informationen:
http://www.fli-leibniz.de/groups/than.phpAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Entscheidender Durchbruch für die Batterieproduktion
Energie speichern und nutzen mit innovativen Schwefelkathoden. HU-Forschungsteam entwickelt Grundlagen für nachhaltige Batterietechnologie. Elektromobilität und portable elektronische Geräte wie Laptop und Handy sind ohne die Verwendung von Lithium-Ionen-Batterien undenkbar. Das…

Wenn Immunzellen den Körper bewegungsunfähig machen
Weltweit erste Therapie der systemischen Sklerose mit einer onkologischen Immuntherapie am LMU Klinikum München. Es ist ein durchaus spektakulärer Fall: Nach einem mehrwöchigen Behandlungszyklus mit einem immuntherapeutischen Krebsmedikament hat ein…
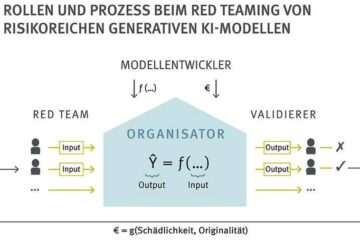
So soll risikoreiche generative KI geprüft werden
Die beschlossene KI-Verordnung der EU sieht vor, dass Künstliche-Intelligenz-Modelle (KI) „für allgemeine Zwecke mit systemischem Risiko“ besonders strikt überprüft werden. In diese Modellkategorie gehören auch populäre generative KI-Modelle wie GPT4…





















