Gehirn im Schwebezustand: Einflüsse der Epigenetik auf die Hirnentwicklung
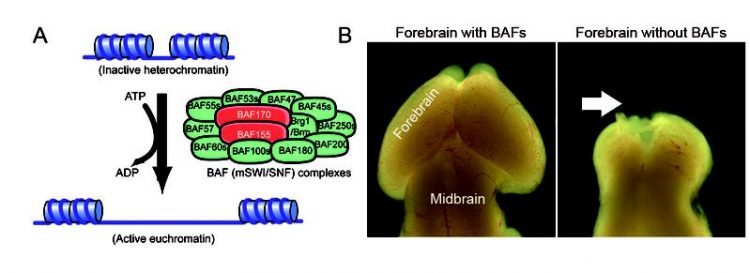
Chromatin-Umbau und Funktion des BAF-Komplexes in der Entwicklung des Vorderhirns. (A) In einem Energieverbrauchenden Prozess beeinflusst der BAF-Multiproteinkomplex durch Anlagerung die Chromatin-Struktur. Die lokale Umwandlung von inaktivem Heterochromatin in die locker gepackte aktive Form (Euchromatin) ermöglicht die Anlagerung von Transkriptionsfaktoren an einzelne Gene und deren Aktivierung bzw. Deaktivierung. (B) Die Proteinuntereinheiten BAF155 und BAF170 dienen als Grundgerüst des gesamten BAF-Komplexes. Mutanten, denen diese Faktoren fehlen, weisen eine massiv gestörte Entwicklung des Vorderhirns auf. Quelle: Tuoc / CNMPB
Die Bildung von Nervenzellen, die sogenannte Neurogenese, läuft beim Menschen und allen anderen Säugern während der Hirnentwicklung auf Hochtouren und ist dann so gut wie abgeschlossen. Allein im Vorderhirn entstehen in bestimmten Regionen auch im erwachsenen Gehirn noch neue Nervenzellen.
Schlüsselmechanismen der Neurogenese sind die sogenannte Epigenetik und der Umbau der Chromatin-Struktur (chromatin remodeling). Sie kontrollieren die Expression von Genen und fördern die Differenzierung von Nervenzellen aus Vorläuferzellen, den neuronalen Stammzellen.
Wie genau das Zusammenspiel von Epigenetik und Chromatin-Umbau die Differenzierung der Stammzellen reguliert, ist bisher noch wenig verstanden. Detailkenntnisse könnten helfen, Strategien zu entwickeln, um die Neubildung von Nervenzellen gezielt anzuregen. Damit eröffnen sich neue Möglichkeiten für die Behandlung von Erkrankungen, bei denen das Gehirn geschädigt ist.
Wissenschaftlern des Exzellenzclusters und des DFG-Forschungszentrums für Mikroskopie im Nanometerbereich und Molekularphysiologie des Gehirns (CNMPB) der Universitätsmedizin Göttingen (UMG), des Max-Planck-Instituts für biophysikalische Chemie (MPIBPC) und des Deutschen Zentrums für Neurodegenerative Erkrankungen (DZNE) am Standort Göttingen ist es nun erstmals gelungen, die Rolle des BAF-Multiproteinkomplexes genauer zu untersuchen.
Dieser Komplex ist in der Entwicklung des Vorderhirns entscheidend daran beteiligt, dass sich neuronale Stammzellen zu Nervenzellen entwickeln. Die Ergebnisse der Göttinger Wissenschaftler liefern erste Belege dafür, dass es einen molekularen Mechanismus gibt, in dem der BAF-Komplex zentral umfassende epigenetische und Genexpressionsprogramme kontrolliert. Die Ergebnisse wurden in der Fachzeitschrift Cell Reports veröffentlicht.
Originalveröffentlichung: Narayanan R, Pirouz M, Kerimoglu C, Kiszka K, Pham L, Wagener R, Rosenbusch J, Kessel M, Fischer A, Stoykova A, Staiger JF, Tuoc T (2014) Loss of the entire multi-subunit BAF (mSWI/SNF) complexes impairs global epigenetic programs in forebrain development. CELL REPORTS, 13(9): 1842-54.
NEUE ERKENNTNISSE ÜBER DEN BAF-KOMPLEX
Nach den neuen Erkenntnissen der Göttinger Forscher aktiviert der BAF-Komplex nicht selbst Genexpressionsprogramme. Vielmehr nimmt er indirekt Einfluss, indem er Abschaltmechanismen in neuronalen Zellen blockiert. Damit während der Hirnentwicklung Differenzierungsprogramme zur Bildung von Nervenzellen schnellst möglich aktiviert werden können, werden bestimmte Gene in einer Art Schwebezustand gehalten. Maßgeblich kontrolliert wird dieser Zustand durch die Präsenz bestimmter epigenetischer Marker, die Transkriptionsprozesse fördern bzw. unterdrücken. Während der Entwicklung interagiert der BAF-Komplex mit diesen Markern und unterstützt das Umschalten von Schwebezustand zu aktiviertem Zustand und initiiert so den Chromatin-Umbau.
BAF-MULTIPROTEINKOMPLEX: HINTERGRUNDINFORMATIONEN
Wie genau werden neuronale Stammzellen dazu gebracht, neue Nervenzellen hervorzubringen? Dies zu verstehen, ist eine der größten Herausforderungen in der Neurobiologie. Bisher konnte nicht umfassend geklärt werden, in welcher Weise der BAF-Multiproteinkomplex genau das Schicksal von neuronalen Vorläuferzellen beeinflusst.
Der BAF-Multiproteinkomplex ist in der Hirnentwicklung das zentrale Steuerelement für die Aktivierung von Programmen, die zur Neubildung von Nervenzellen führen. Seine Anlagerung an bestimmte Abschnitte des Genoms initiiert den Umbau der Chromatin-Struktur. Dabei wird inaktives, kondensiertes Chromatin (Heterochromatin) in die locker gepackte aktive Form (Euchromatin) umgewandelt. Die für die neuronale Differenzierung notwendigen Gene werden dadurch für bestimmte Transkriptionsfaktoren zugänglich und können an- oder abgeschaltet werden. Welche Bereiche des Chromatins einem Umbau unterzogen werden, wird zuvor durch epigenetische Einflüsse gesetzte, chemische Markierungen bestimmt.
ERGEBNISSE IM DETAIL
Den Göttinger Forschern ist es erstmals gelungen, Mäuse zu züchten, mit denen sich die Rolle des BAF-Komplexes für die Hirnentwicklung detailliert untersuchen lässt. Durch gezielte Mutagenese wurden verschiedene Faktoren des Komplexes eliminiert, so dass diese Mäuse über keine funktionellen BAF-Komplexe verfügen. Das Ergebnis: Die Proteinuntereinheiten BAF150 und BAF170 bilden als zentrale Schlüsselfaktoren das Grundgerüst des Komplexes.
Sie dienen als Andockstellen für die bis zu 15 weiteren BAF-Untereinheiten. Dabei regulieren sie nicht nur die Stabilität, sondern auch die Funktionalität des Komplexes. Mäuse, die diese beiden Faktoren nicht ausbilden, zeigen ein massiv gestörtes Wachstum der Vorderhirnstrukturen. Weitere Ergebnisse der Untersuchung: Das Fehlen eines funktionellen BAF-Komplexes verursachte eine massive Reduktion an locker gepacktem Euchromatin, verbunden mit einer dramatischen Abnahme an Genexpressionsereignissen. Gleichzeitig konnte eine starke Zunahme bestimmter Heterochromatin-Marker beobachtet werden.
„Diese Ergebnisse vertiefen unser Verständnis davon, wie Epigenetik und der Chromatin-Regulation das Schicksal neuronaler Vorläuferzellen und die Plastizität in der Hirnentwicklung beeinflussen. Sie werden außerdem dazu beitragen, neue therapeutische Strategien zu entwickeln, um die Neubildung von Nervenzellen im geschädigten Gehirn, beispielsweise bei der Therapie neurodegenerativer Erkrankungen, anzuregen”, sagt Dr. Tuoc Tran, Senior-Autor der Publikation und Wissenschaftler am Institut für Neuroanatomie der UMG.
Weitere Informationen:
http://www.neuroanatomie.uni-goettingen.de/de/home – Homepage des Instituts für Neuroanatomie der Universitätsmedizin Göttingen
http://www.cnmpb.de Exzellenzcluster und DFG-Forschungszentrum für Mikroskopie im Nanometerbereich und Molekularbiologie des Gehirns (CNMPB)
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Nanofasern befreien Wasser von gefährlichen Farbstoffen
Farbstoffe, wie sie zum Beispiel in der Textilindustrie verwendet werden, sind ein großes Umweltproblem. An der TU Wien entwickelte man nun effiziente Filter dafür – mit Hilfe von Zellulose-Abfällen. Abfall…

Entscheidender Durchbruch für die Batterieproduktion
Energie speichern und nutzen mit innovativen Schwefelkathoden. HU-Forschungsteam entwickelt Grundlagen für nachhaltige Batterietechnologie. Elektromobilität und portable elektronische Geräte wie Laptop und Handy sind ohne die Verwendung von Lithium-Ionen-Batterien undenkbar. Das…

Wenn Immunzellen den Körper bewegungsunfähig machen
Weltweit erste Therapie der systemischen Sklerose mit einer onkologischen Immuntherapie am LMU Klinikum München. Es ist ein durchaus spektakulärer Fall: Nach einem mehrwöchigen Behandlungszyklus mit einem immuntherapeutischen Krebsmedikament hat ein…





















