Filmen von Chemie in Echtzeit mit der Hochgeschwindigkeits-Röntgenkamera
Bildung und der Bruch von chemischen Bindungen entlang unterschiedlicher Reaktionswege. Abb.: MBI
Wissenschaftler des Berliner Max-Born-Instituts für Nichtlineare Optik und Kurzzeitspektroskopie (MBI) konnten jetzt zeigen, dass eine ultraschnelle Röntgenkamera nicht nur sensitiv gegenüber von chemisch inerten Rumpfelektronen ist, sondern auch die Bewegung von chemisch aktiven Valenzelektronen visualisieren kann.
Dementsprechend ist die Bewegung von Valenzelektronen zentraler Bestandteil von jeder chemischen Reaktion. Dabei muss beachtet werden, dass lediglich ein Bruchteil dieser Valenzelektronen – oft nur ein kleiner Teil der Ladung eines Elektrons – aktiv an chemischen Reaktionen teilnimmt. Und dies geschieht äußerst schnell:
Die Dauer von vielen wichtigen chemischen Prozessen wie z.B. die ersten Schritte des Sehvorgangs und der Lichtsammlung in biologischen Systemen, beträgt lediglich wenige Femtosekunden (1 Femtosekunde = 10hoch-15 Sekunden). Die Aufnahme dieser chemisch aktiven Valenzelektronen ist daher äußerst anspruchsvoll. Erstens benötigt man eine Kamera mit exzellenter Zeit- und Ortsauflösung.
Zweitens wird eine sehr empfindliche Kamera benötigt, denn man ist nicht nur daran interessiert wie sich die Atome bewegen, sondern auch daran wie chemische Bindungen gebrochen und neue Bindungen gebildet werden – und das bedeutet den Bruchteil an aktiven Valenzelektronen aufzunehmen, welche sich im Meer aller Elektronen bewegen, die an die Atome in Molekülen gebunden sind.
Eine Röntgenkamera genügt leicht der ersten Voraussetzung. Die Streuung von Röntgenstrahlung durch Materie ist seit Entdeckung von Röntgenstrahlung ein unverzichtbares Hilfsmittel der Strukturauflösung mit atomarer Ortsauflösung.
Durch enormen technologischen Fortschritt können nun auch ultrakurze Röntgenblitze generiert werden, welche vorausgehende Untersuchungen um Zeitauflösung im Femtosekundenbereich erweitern können. Diese Röntgenblitze versprechen stroboskopische Schnappschüsse von chemischen und biologischen Prozessen in individuellen Molekülen zu generieren.
Das Erfüllen der zweiten Voraussetzung – Sensibilität gegenüber aktiven Valenzelektronen – gehört allerdings nicht zu den Stärken einer Röntgenkamera. Die Streuung von Röntgenstrahlung durch Moleküle wird immer durch Rumpfelektronen und inerte Valenzelektronen dominiert.
Daher wird generell angenommen, dass der kleine Teil von Valenzelektronen, welcher aktiv an chemischen Reaktionen beteiligt ist, im Gesamtstreusignal untergeht und damit die Aufnahme der ultraschnellen Umlagerung von aktiven Valenzelektronen mittels einer Röntgenkamera nicht möglich ist.
Unsere in Nature Communications veröffentlichte Arbeit schlägt einen Weg vor diese Herausforderung zu lösen. Wir demonstrieren theoretisch eine robuste und effektive Methode, welche es ermöglicht Informationen über chemisch aktive Valenzelektronen aus den Röntgenstreubildern eines einzelnen Moleküls zu extrahieren – ein entscheidender Schritt bei dem Bestreben die Bildung und den Bruch von chemischen Bindungen in Echtzeit mit atomarer Ortsauflösung aufzunehmen.
Unsere Arbeit zeigt wie die Bewegung von chemisch aktiven Valenzelektronen durch eine Kombination der routinemäßigen Analyse von Röntgenstreubildern mit der zusätzlichen Analyse jenes Bereichs der Streubilder, welcher auf einen relativ kleinen Impulstransfer beschränkt ist, sichtbar gemacht werden kann.
Die Arbeit zeigt nicht nur wie chemisch aktive Valenzelektronen mit Röntgenstrahlung aufgenommen werden können, sondern sie liefert auch experimentellen Zugang zu dem viel diskutierten Problem von synchroner gegen asynchrone Bindungsbildung und Bindungsbruch in chemischen Reaktionen. Die ultraschnelle Röntgenkamera bestätigt, dass die Antwort davon abhängt, ob die Atome genügend Energie haben, um die Energiebarriere, welche Reaktanden von Produkten trennt, zu überqueren, oder ob die Atome auf das Quantenphänomen des Tunnels durch die Energiebarriere zurückgreifen müssen.
Im ersten Fall bestätigen wir eine Verzögerungszeit zwischen dem Bruch von alten und der Bildung von neuen Bindungen. Im zweiten Fall beobachten wir keine Verzögerung: Der Bruch der alten und die Bildung der neuen Bindungen ist synchron. Wir hoffen, dass unsere Arbeit neue Einblicke in die Initialisierung und Kontrolle von komplexen chemischen und biologischen Reaktionen bringen wird.
Originalveröffentlichung:
Timm Bredtmann, Misha Ivanov, Gopal Dixit: X-ray imaging of chemically active valence electrons during a pericyclic reaction
Nature Communication doi:10.1038/ncomms6589
Abb. 1: Aufnahme des Bruchs und der Bildung von chemischen Bindungen während einer perizyklischen Reaktion: Wir zeigen theoretisch, dass die ultraschnelle Röntgenkamera nicht nur sensitiv gegenüber von chemisch inerten Rumpfelektronen ist, sondern auch die Bewegung von chemisch aktiven Valenzelektronen visualisieren kann.
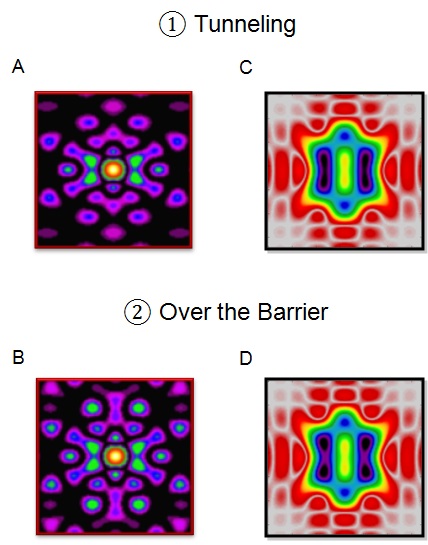
Abb. 2: Die Kombination der routinemäßigen Analyse von Röntgenstreubildern (A, B) mit der zusätzlichen Analyse jenes Bereichs, welcher auf einen relativ kleinen Impulstransfer beschränkt ist, ermöglicht die Bewegung von chemisch aktiven Valenzelektronen während einer perizyklischen Reaktion sichtbar zu machen (C, D). Die Bildung und der Bruch von chemischen Bindungen entlang unterschiedlicher Reaktionswege kann so direkt aufgenommen und analysiert werden.
Kontakt
Dr. Timm Bredtmann Tel: 030 6392 1239
Prof. Micha Ivanov Tel: 030 6392 1210
Dr. Gopal Dixit Tel: 030 6392 1239
Max-Born-Institut für Nichtlineare Optik und Kurzzeitspektroskopie (MBI)
im Forschungsverbund Berlin e.V
Max-Born-Institut
Max-Born-Straße 2A
12489 Berlin
Tel. ++49 30 6392 1505
Fax. ++49 30 6392 1509
E-Mail: mbi@mbi-berlin.de
Das Max-Born-Institut für Nichtlineare Optik und Kurzzeitspektroskopie (MBI) gehört zum Forschungsverbund Berlin e.V. (FVB), einem Zusammenschluss von acht natur-, lebens- und umweltwissenschaftlichen Instituten in Berlin. In ihnen arbeiten mehr als 1.500 Mitarbeiter. Die vielfach ausgezeichneten Einrichtungen sind Mitglieder der Leibniz-Gemeinschaft. Entstanden ist der Forschungsverbund 1992 in einer einzigartigen historischen Situation aus der ehemaligen Akademie der Wissenschaften der DDR.
Weitere Informationen:
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Ideen für die Zukunft
TU Berlin präsentiert sich vom 22. bis 26. April 2024 mit neun Projekten auf der Hannover Messe 2024. Die HANNOVER MESSE gilt als die Weltleitmesse der Industrie. Ihr diesjähriger Schwerpunkt…

Peptide auf interstellarem Eis
Dass einfache Peptide auf kosmischen Staubkörnern entstehen können, wurde vom Forschungsteam um Dr. Serge Krasnokutski vom Astrophysikalischen Labor des Max-Planck-Instituts für Astronomie an der Universität Jena bereits gezeigt. Bisher ging…

Wasserstoff-Produktion in der heimischen Garage
Forschungsteam der Frankfurt UAS entwickelt Prototyp für Privathaushalte: Förderzusage vom Land Hessen für 2. Projektphase. Wasserstoff als Energieträger der Zukunft ist nicht frei verfügbar, sondern muss aufwendig hergestellt werden. Das…





















