DNA: nicht nur gut als Erbgut
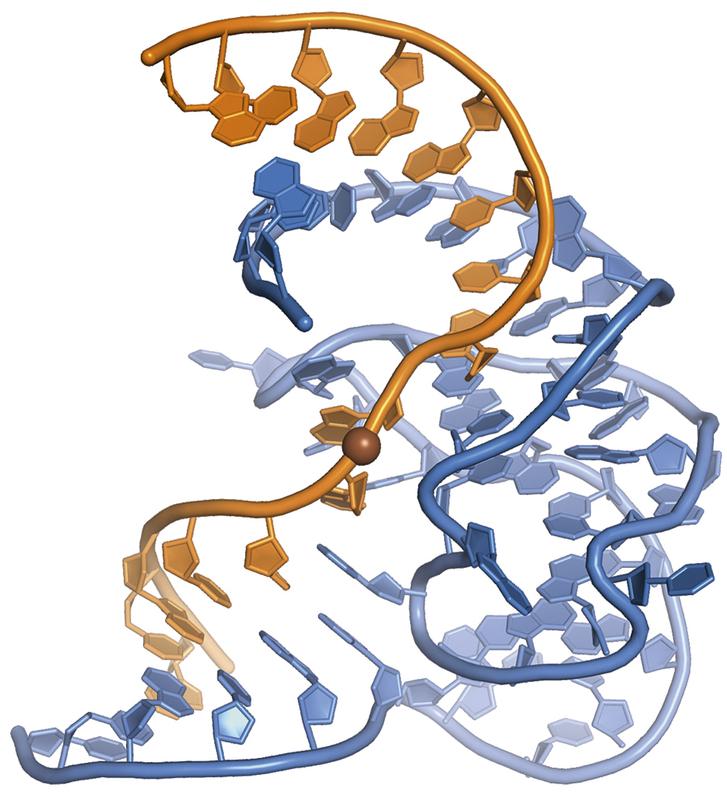
Die erste dreidimensionale Struktur eines DNA-Enzyms. Das Desoxyribozym (blau) hat zwei RNA-Stränge (orange) miteinander verknüpft. Höbartner und Pena / Max-Planck-Institut für biophysikalische Chemie
Göttinger Forscher um Claudia Höbartner und Vlad Pena haben nun erstmals die räumliche Struktur eines DNA-Enzyms im atomaren Detail sichtbar gemacht. Sie erbringen damit den Beweis, dass sich auch DNA zu komplexen dreidimensionalen Formen faltet, um katalytisch aktiv zu sein.
Die neuen Erkenntnisse lösen ein langjähriges Rätsel der Nukleinsäure-Chemie und sind ein wichtiger Schritt, um DNA-Enzyme besser zu verstehen und als Werkzeuge nutzbar zu machen.
Anders als katalytische Proteine und RNAs hat man DNA-Enzyme, auch Desoxyribozyme genannt, bisher in lebenden Zellen nicht gefunden. Wissenschaftler stellen diese künstlich her, indem sie eine Vielzahl einzelner DNA-Stränge produzieren und anschließend jene herausfiltern, die enzymatisch aktiv sind, also chemische Reaktionen katalysieren.
Die Desoxyribozyme können dann als Werkzeuge in der Forschung dienen. Sie werden beispielsweise dafür eingesetzt, RNA-Moleküle an einer definierten Stelle zu schneiden oder zwei RNAs miteinander zu verknüpfen. Außerdem hofft man, sie auch in der Medizin nutzen zu können, um etwa an Krankheiten beteiligte Gene gezielt auszuschalten.
„Um wirksame Desoxyribozyme für einen bestimmten Zweck zu optimieren, müssen wir zunächst mehr darüber lernen, wie sie im Detail funktionieren“, erläutert Claudia Höbartner, Leiterin der Gruppe Nukleinsäurechemie am Göttinger Max-Planck-Institut für biophysikalische Chemie und Professorin am Institut für Organische und Biomolekulare Chemie an der Universität Göttingen.
„Dafür ist es nötig zu verstehen, welche dreidimensionale Struktur der DNA-Strang einnimmt und wie es der DNA gelingt, unter den vielen möglichen Stellen in der RNA genau eine einzige für die Reaktion auszuwählen.“
Eine solche Desoxyribozym-Struktur zu ermitteln versuchen Forscher, seit DNA-Enzyme vor mehr als 20 Jahren entdeckt wurden. Dem Team um Claudia Höbartner und Vlad Pena ist jetzt der Durchbruch gelungen: Sie haben die räumliche Struktur eines Desoxyribozyms mit atomarer Genauigkeit analysiert und damit detaillierte Einblicke in dessen Funktionsweise gewonnen – ein Meilenstein in der Forschung an Nukleinsäure-Enzymen.
Desoxyribozyme falten sich wie Proteine und RNA-Enzyme
Das untersuchte DNA Enzym katalysiert das Ausbilden einer natürlichen chemischen Bindung zwischen zwei RNA-Molekülen, die dadurch zu einem einzigen RNA-Strang verschmelzen. Die Struktur der Göttinger Chemiker zeigt das Desoxyribozym am Ende dieser Reaktion.
„Wie wir sehen konnten, hat sich der DNA-Strang zu einer kompakten Einheit zusammengefaltet. Dadurch kommen bestimmte Bauteile der DNA an einem Punkt mit den Enden der RNA-Stränge zusammen und bilden ein Zentrum, in dem die chemische Reaktion abläuft“, erklärt Vlad Pena, der am MPI für biophysikalische Chemie die Forschungsgruppe Makromolekulare Kristallografie leitet.
Mit der ersten dreidimensionalen Struktur eines Desoxyribozyms zeigen die Göttinger Wissenschaftler jetzt, was lange vermutet, bisher aber nicht belegt werden konnte: DNA-Enzyme nehmen, ebenso wie enzymatische RNAs und Proteine, eine definierte dreidimensionale Struktur ein, um ihre katalytische Aufgabe zu erfüllen. „Daraus ergibt sich die spannende Frage, ob komplexere DNA-Strukturen nicht auch in der Natur eine Rolle spielen könnten, ähnlich wie wir es bisher nur von RNAs und Proteinen kennen“, so Pena.
Die gewonnenen Erkenntnisse der Forscher sind auch hilfreich, um den genauen Ablauf der Reaktion zu verstehen und DNA-Enzyme als Werkzeuge zu verbessern: Dank der neuen Informationen konnten sie das DNA-Enzym so modifizieren, dass es seine „Vorliebe“ für bestimmte RNAs änderte.
Des Weiteren lösten die Chemiker mit der ersten Struktur eines Desoxyribozyms ein Rätsel, das Wissenschaftler beschäftigt hat, seit man von katalytisch aktiven DNA-Molekülen weiß: Die verwandten RNA-Enzyme sind besonders gute Katalysatoren, weil sie an jedem einzelnen DNA-Baustein eine zusätzliche sogenannte Hydroxylgruppe besitzen, die für die Struktur der RNA-Enzyme und für die Katalyse der Reaktionen eine wichtige Rolle spielt. Diese zusätzliche Hydroxylgruppe fehlt der DNA.
Wie also schaffen es Desoxyribozyme, Reaktionen ähnlich gut zu katalysieren wie die chemisch doch viel besser ausgestatteten RNA-Enzyme? „Die Struktur des Desoxyribozyms zeigt, dass die fehlende Hydroxylgruppe für die DNA kein Nachteil ist“, berichtet Almudena Ponce-Salvatierra, Erstautorin der Arbeit. „Ihre Abwesenheit macht den DNA-Strang nämlich viel flexibler. Er kann sich daher zu ganz anderen Formen zusammenfalten, als es einem RNA-Strang möglich wäre. Dadurch hat ein Desoxyribozym noch mehr Möglichkeiten, seine chemischen Bausteine so zusammenzubringen, dass sie Reaktionen katalysieren können.“
In Zukunft will Max-Planck-Forscherin Höbartner noch mehr über diese besonderen Nukleinsäure-Moleküle herausfinden: „Wir werden versuchen, ein Desoxyribozym nicht nur nach, sondern vor oder während der chemischen Reaktion ‚einzufrieren‘ und seine Struktur zu analysieren. Diese würde uns noch mehr Details über den Mechanismus verraten, mit dem das Enzym seine Reaktion katalysiert.“ (fk)
Original-Veröffentlichung:
Almudena Ponce-Salvatierra, Katarzyna Wawrzyniak-Turek, Ulrich Steuerwald, Claudia Höbartner, Vladimir Pena: Crystal structure of a DNA catalyst. Nature 529, 231-234 (2016).
Kontakt:
Prof. Dr. Claudia Höbartner, Gastgruppe Nukleinsäurechemie
Max-Planck-Institut für biophysikalische Chemie, Göttingen, und
Institut für Organische und Biomolekulare Chemie, Universität Göttingen
Tel.: +49 551 201-1685, +49 551 39-20906
E-Mail: claudia.hoebartner@mpibpc.mpg.de
Dr. Vlad Pena, Forschungsgruppe Makromolekulare Kristallografie
Max-Planck-Institut für biophysikalische Chemie, Göttingen
Tel.: +49 551 201-1197
E-Mail: vpena@gwdg.de
Dr. Frederik Köpper, Presse- und Öffentlichkeitsarbeit
Max-Planck-Institut für biophysikalische Chemie, Göttingen
Tel.: +49 551 201-1310
E-Mail: frederik.koepper@mpibpc.mpg.de
http://www.mpibpc.mpg.de/15196506/pr_1601 – Originalpressemitteilung des Max-Planck-Instituts für biophysikalische Chemie, Göttingen
http://www.mpibpc.mpg.de/de/hoebartner – Webseite der Gastgruppe Nukleinsäurechemie am
http://Max-Planck-Institut für biophysikalische Chemie
http://www.mpibpc.mpg.de/de/pena – Webseite der Forschungsgruppe Makromolekulare Kristallografie am Max-Planck-Institut für biophysikalische Chemie
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Ultraleichte selbstglättende Spiegel
…erhöhen die Effizient hochmoderner Teleskope. Schon immer faszinierte den Menschen der Blick in den Sternenhimmmel und nicht minder faszinierend ist es, die Erde aus dem Weltraum zu betrachten. Möglich ist…

Überraschende Umkehr in Quantensystemen
Forschende haben topologisches Pumpen in einem künstlichen Festkörper aus kalten Atomen untersucht. Die Atome wurden mit Laserstrahlen gefangen. Überraschenderweise kam es zu einer plötzlichen Umkehr der Atome an einer Wand…

Magnetisch durch eine Prise Wasserstoff
Neue Idee, um die Eigenschaften ultradünner Materialien zu verbessern. Magnetische zweidimensionale Schichten, die aus einer oder wenigen Atomlagen bestehen, sind erst seit kurzem bekannt und versprechen interessante Anwendungen, zum Beispiel…





















