Halogenbrücken bereichern die Wirkstoffforschung
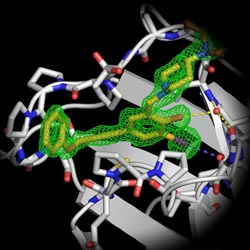
Ein Ausschnitt aus der Kristallstruktur des mutierten Tumorsuppressors p53 (im Komplex mit Verbindung PhiKan5176), die über eine Halogenbrücke (violette Strichlinie) mit der Bindungstasche interagiert. Verbindungen der neuen Substanzklasse reaktivieren p53 in betroffenen Krebszellen. Abbildung: Prof. Frank Böckler<br>
Halogene ‒ besonders die Elemente Chlor, Brom und Iod ‒ besitzen einzigartige Eigenschaften, mit denen sie die Interaktion zwischen Molekülen positiv beeinflussen können. Diese Wechselwirkungen werden mit dem Begriff „Halogenbrücken“ (engl.: „Halogen Bonding“) bezeichnet.
Das Phänomen der Halogenbrücken ist seit Längerem im Bereich der Materialwissenschaften bekannt, hatte aber bisher wenig Bedeutung in den Lebenswissenschaften. Dabei können solche Halogenbrücken gerade auch die Erkennung von kleinen therapeutisch einsetzbaren Molekülen durch ihre biologischen Zielstrukturen beeinflussen.
Tübinger Wissenschaftler zeigen nun erstmals, wie Halogenbrücken für Krebstherapien nutzbar gemacht werden könnten. Professor Frank Böckler und seine Mitarbeiter präsentierten dabei ein neues Konzept für eine moderne Methode der Wirkstoffforschung, die „Fragmentbasierte Leitstruktur-Entwicklung“. Bei dieser werden Substanzbibliotheken bestehend aus kleinen chemischen Fragmenten in einem Screening-Verfahren an biologischen Zielstrukturen wie Proteinen oder DNA getestet, um neue Startpunkte für die Entwicklung von Wirkstoffen zu finden.
Bisher waren Halogene, besonders die schwereren Elemente Brom und Iod, in entsprechenden Bibliotheken chemischer Fragmente stark unterrepräsentiert. Die Wissenschaftler aus dem Pharmazeutischen Institut der Universität Tübingen beschreiben nun im „Journal of the American Chemical Society“ (DOI: 10.1021/ja301056a) zum ersten Mal das Design und die Anwendung von mit Halogenen angereicherten Fragment-Bibliotheken, bezeichnet mit dem Akronym „HEFLibs“. Es war ihnen gelungen, mit HEFLibs eine defekte Form des Transkriptionsfaktors p53 in Zellen zu reaktivieren. Dieser nimmt eine zentrale Rolle in der Krebsprävention und – abwehr ein.
p53 sorgt dafür, dass Proteine gebildet werden, die wichtige Vorgänge der Zelle steuern, beispielsweise die Reparatur von DNA oder die Not-Abschaltung der Zelle durch Apoptose ‒ den programmierten Zelltod. Die Schädigung von p53 durch Mutation kann zum Verlust dieser Kontrollfunktionen und somit zur Entwicklung verschiedener Krebsarten führen. Verbindungen, die in der Lage sind, das mutierte p53 zu reaktivieren, könnten deshalb großes Potential für die Tumortherapie besitzen.
Durch Anwendung des neuen HEFLibs-Konzepts konnten nun Verbindungen identifiziert werden, welche die p53 Krebs-Mutante Y220C erkennen, stabilisieren und damit reaktivieren können. Diese Verbindungen ‒ 2-(Aminomethyl)-4-ethynyl-6-iodophenole ‒ stellen somit einen interessanten Startpunkt für die weitere Optimierung dar. „Diese Ergebnisse sind das Resultat einer langjährigen engen Zusammenarbeit mit Dr. Andreas Jörger und Prof. Sir Alan Fersht vom MRC Laboratory of Molecular Biology in Cambridge/UK“, berichtet Prof. Böckler.
„Die Idee, Halogenbrücken gezielt durch HEFLibs zu induzieren und dieses Konzept an mutiertem p53 zu erproben, ist vor allem das Verdienst von Dr. Rainer Wilcken, der für seine in Tübingen angefertigte Doktorarbeit mit dem Merckle-Promotionspreis 2011 ausgezeichnet wurde“, so Böckler. „In den Kristallstrukturen der Protein-Ligand-Komplexe der von uns entwickelten Verbindungsklasse zeigt sich die wesentliche Bedeutung der durch Iod vermittelten Halogenbrücke für die molekulare Erkennung. Die Ergebnisse geben Anlass zu der Hoffnung, dass HEFLibs großes Potential für die Anwendung als neue Strategie für die Identifikation von Leitstrukturen haben, bei einer Vielzahl von therapeutisch relevanten Proteinen. Die Editoren von JACS haben deshalb unsere Veröffentlichung als JACS Spotlight ausgewählt.“
Publikation: Rainer Wilcken, Xiangrui Liu, Markus O. Zimmermann, Trevor J. Rutherford, Alan R. Fersht, Andreas C. Joerger* & Frank M. Boeckler*: „Halogen-Enriched Fragment Libraries as Leads for Drug Rescue of Mutant p53“. J. Am. Chem. Soc., 2012, 134 (15), pp 6810–6818 (DOI: 10.1021/ja301056a)
Kontakt:
Prof. Dr. Frank Böckler
Universität Tübingen
Mathematisch-Naturwissenschaftliche Fakultät
Fachbereich Pharmazie & Biochemie/ Labor für Molekulares Design & Pharm. Biophysik
Telefon + 49 7071 29-74567
Telefax + 49 7071 29-5637
frank.boeckler[at]uni-tuebingen.de
Media Contact
Weitere Informationen:
http://www.uni-tuebingen.deAlle Nachrichten aus der Kategorie: Medizin Gesundheit
Dieser Fachbereich fasst die Vielzahl der medizinischen Fachrichtungen aus dem Bereich der Humanmedizin zusammen.
Unter anderem finden Sie hier Berichte aus den Teilbereichen: Anästhesiologie, Anatomie, Chirurgie, Humangenetik, Hygiene und Umweltmedizin, Innere Medizin, Neurologie, Pharmakologie, Physiologie, Urologie oder Zahnmedizin.
Neueste Beiträge

Neue universelle lichtbasierte Technik zur Kontrolle der Talpolarisation
Ein internationales Forscherteam berichtet in Nature über eine neue Methode, mit der zum ersten Mal die Talpolarisation in zentrosymmetrischen Bulk-Materialien auf eine nicht materialspezifische Weise erreicht wird. Diese „universelle Technik“…

Tumorzellen hebeln das Immunsystem früh aus
Neu entdeckter Mechanismus könnte Krebs-Immuntherapien deutlich verbessern. Tumore verhindern aktiv, dass sich Immunantworten durch sogenannte zytotoxische T-Zellen bilden, die den Krebs bekämpfen könnten. Wie das genau geschieht, beschreiben jetzt erstmals…

Immunzellen in den Startlöchern: „Allzeit bereit“ ist harte Arbeit
Wenn Krankheitserreger in den Körper eindringen, muss das Immunsystem sofort reagieren und eine Infektion verhindern oder eindämmen. Doch wie halten sich unsere Abwehrzellen bereit, wenn kein Angreifer in Sicht ist?…