Erlanger Wissenschaftler entwickeln neue Medikamenten-Generation gegen Herpesviren

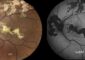
Computer-basierte Vorhersage der dreidimensionalen Struktur des aktiven Zentrums des viralen Enzyms pUL97. Das Strukturmodel basiert auf einem Vergleich mit der bekannten Struktur des verwandten zellulären Enzyms CDK2. Quelle: Romaker et al., 2006, J. Med. Chem. 49, 7044-7053<br>
Die Forschergruppe um Prof. Manfred Marschall am Virologischen Institut des Universitätsklinikums Erlangen will daher eine ganz neue Strategie der Medikamenten-Entwicklung anwenden, welche innovative Technologien einbindet. Ziel ist es, die Vermehrung der Erreger zu blockieren und gleichzeitig deren Resistenzbildung gegen die Medikamente zu unterbinden. Diese neue Technologie-Basis soll helfen, Medikamente maßzuschneidern und damit besonders wirkungsvoll zu gestalten.
Die Infektion mit dem humanen Cytomegalovirus stellt bei Personen mit eingeschränktem Immunsystem eine erhebliche, zum Teil lebensbedrohliche Gefahr dar. Dies gilt insbesondere für Transplantat-Empfänger, Patienten unter einer Tumor-Chemotherapie und für Neugeborene. Die zugelassenen antiviralen Medikamente führen häufig zu Nebenwirkungen und zur Resistenzbildung bei den Viren. Eine Resistenz, also eine erworbene Unempfindlichkeit gegenüber Medikamenten, bilden Viren zum Beispiel, indem sie ihre molekularen Angriffspunkte so verändern, dass die Wirkstoffe ihrer nicht mehr habhaft werden können. „Die Lösung des Problems der Medikamentenresistenz stellt bislang eine der Kernfragen der antiviralen Therapie dar“, erläutert Prof. Manfred Marschall.
Das Forschungsvorhaben der Erlanger stellt diesem Resistenzproblem einen neuen Entwicklungsansatz für Medikamente gegenüber. Sie wollen Wirkstoffe finden und weiterentwickeln, die an unveränderbare Strukturen des Virus binden. Damit hätte das Virus keine Möglichkeit, eine Resistenz zu entwickeln. Das Projektvorhaben vereint zu diesem Zweck erstmals neue molekulare Technologien wie z.B. hochauflösende Mikroskopieverfahren und Proteinstruktur-Analysen, die in der Entwicklung antiviraler Medikamente bisher noch nicht in dieser Form zum Einsatz kamen. Ziel dieser methodischen Innovation ist es, eine nächste Generation von anti-herpesviralen Medikamenten bereitzustellen.
Die Arbeitsgruppe und ihre Kooperationspartner konnten bereits nachweisen, dass das betreffende virale Enzym, die sogenannte Proteinkinase pUL97, durch bestimmte neue Wirkstoffe blockiert werden kann. Die Virusvermehrung kann unter dem Einsatz ganz bestimmter Inhibitoren auf eine Weise unterdrückt werden, dass es nicht zu einer Resistenzbildung kommt. Mithilfe der erprobten Wirkstoffe wollen die Virologen die Wechselwirkung zwischen einem künftigen Medikament und dem Zielmolekül voraussagen. „Die genaue Kenntnis der Wechselwirkung, vor allem mit Blick auf die räumlichen Struktur des viralen Enzyms, würde der Therapie-Entwicklung eine neue Richtung geben“, beschreibt Prof. Manfred Marschall die Motivation für das Projekt.
Die Wilhelm Sander-Stiftung fördert dieses Forschungsprojekt mit rund 190.000 Euro. Stiftungszweck ist die Förderung der medizinischen Forschung, insbesondere von Projekten im Rahmen der Krebsbekämpfung. Seit Gründung der Stiftung wurden insgesamt über 190 Mio. Euro für die Forschungsförderung in Deutschland und der Schweiz bewilligt. Die Stiftung geht aus dem Nachlass des gleichnamigen Unternehmers hervor, der 1973 verstorben ist.
Prof. Manfred Marschall bearbeitet dieses Projekt zusammen mit Dr. Corina Hutterer am Virologischen Institut des Universitätsklinikums Erlangen. Unterstützung erfahren die Virologen durch Prof. Vahid Sandoghdar vom Max-Planck-Institut Erlangen für die Physik des Lichts. Die wissenschaftlichen Leistungen der beiden Arbeitsgruppen umfassen die Disziplinen der medizinischen und molekularen Virologie, verschiedene Bereiche der Molekularbiologie sowie der Biophotonik und Nanooptik. Zahlreiche für dieses Projekt relevante Aspekte und Vorarbeiten wurden von ihnen in der jüngsten Vergangenheit in wissenschaftlichen Journalen publiziert.
Kontakt:
Prof. Dr. Manfred Marschall
Virologisches Institut des Universitätsklinikums Erlangen, Universität Erlangen-Nürnberg
Telefon: +49 (0)9131 8526089
E-Mail: manfred.marschall@viro.med.uni-erlangen.de
Homepage: www.virologie.uni-erlangen.de
Media Contact
Weitere Informationen:
http://www.wilhelm-sander-stiftung.deAlle Nachrichten aus der Kategorie: Medizin Gesundheit
Dieser Fachbereich fasst die Vielzahl der medizinischen Fachrichtungen aus dem Bereich der Humanmedizin zusammen.
Unter anderem finden Sie hier Berichte aus den Teilbereichen: Anästhesiologie, Anatomie, Chirurgie, Humangenetik, Hygiene und Umweltmedizin, Innere Medizin, Neurologie, Pharmakologie, Physiologie, Urologie oder Zahnmedizin.
Neueste Beiträge

Neue universelle lichtbasierte Technik zur Kontrolle der Talpolarisation
Ein internationales Forscherteam berichtet in Nature über eine neue Methode, mit der zum ersten Mal die Talpolarisation in zentrosymmetrischen Bulk-Materialien auf eine nicht materialspezifische Weise erreicht wird. Diese „universelle Technik“…

Tumorzellen hebeln das Immunsystem früh aus
Neu entdeckter Mechanismus könnte Krebs-Immuntherapien deutlich verbessern. Tumore verhindern aktiv, dass sich Immunantworten durch sogenannte zytotoxische T-Zellen bilden, die den Krebs bekämpfen könnten. Wie das genau geschieht, beschreiben jetzt erstmals…

Immunzellen in den Startlöchern: „Allzeit bereit“ ist harte Arbeit
Wenn Krankheitserreger in den Körper eindringen, muss das Immunsystem sofort reagieren und eine Infektion verhindern oder eindämmen. Doch wie halten sich unsere Abwehrzellen bereit, wenn kein Angreifer in Sicht ist?…