Basler Forschenden gelingen neue Einsichten in der Allergiebekämpfung
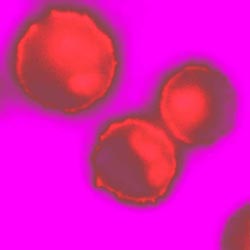
Mastzellen, die eine fluoresziende Probe enthalten, die spezifisch das Membranlipid PtdIns(3,4,5)P3 bindet. Dieses Lipid gibt Auskunft über den Aktivierungszustand der Mastzellen.<br>
Dies berichten Forschende vom Departement für Biomedizin der Universität Basel. In kürzlich publizierten Arbeiten erläutern sie die physiologische Funktion eines bestimmten Enzyms bei der Wanderung und der Aktivierung von Mastzellen und beschreiben einen neuen, unerwarteten Aktivierungsmodus dieses Enzyms.
Allergische Reaktionen sind Überreaktionen des Immunsystems und Grundlage vieler entzündlicher Krankheiten. Dabei kommt den Mastzellen eine zentrale Rolle zu, indem sie durch Immunglobulin E (IgE) Rezeptoren und daran gebundenes IgE Antigene erkennen können. Die Bindung eines Antigens an die IgE Moleküle auf der Mastzelle führt zur Aggregation der Rezeptoren, dadurch zu einer Signalübertragung an die Innenseite der Zellmembran und letztlich zur Degranulation der Mastzelle – das heisst, die Zelle setzt Histamin frei.
Histamin wirkt dann auf umliegendes Gewebe, etwa auf Blutgefässe und Bronchien. Abgesehen von dieser schnellen Antwort produzieren aktivierte Mastzellen langfristig wirkende, entzündliche Botenstoffe, die Zytokine. Prominente Vertreter dieser Zytokine sind der «Tumor Necrosis Faktor-alpha» (TNF-alpha) und IL-6, welche die Endothelzellen der Blutgefässe aktivieren können.
In zwei kürzlich erschienenen Arbeiten zeigt die Forschungsgruppe von Prof. Matthias Wymann vom Departement für Biomedizin der Universität Basel, dass die Lipidkinase PI3K-gamma (Phosphoinositide 3-kinase-gamma) physiologisch zentral für die Mastzellwanderung und Aktivierung ist, und beschreibt dabei einen unerwarteten Aktvierungsmodus dieses Enzyms.
Vorläufer blockieren
Bisherige anti-allergische Therapien verhindern entweder die Freisetzung von Histamin aus Mastzellen im Gewebe oder die Wirkung des Histamins. Emilie Collmann und Thomas Bohnacker konnten nun zeigen, dass die PI3K-gamma schon die Degranulation von Mastzellen kontrolliert, dass allergische Prozesse aber noch besser unterdrückt werden können, indem die Einwanderung von Mastzell-Vorläufern aus der Blutbahn ins Gewebe blockiert wird. Ist die PI3K-gamma in Mastzell-Vorläufern inaktiviert, können diese nicht an durch TNF-alpha aktivierte Endothelzellen haften und ins Gewebe gelangen.
Diese genetisch erarbeiteten Erkenntnisse konnten die Forscher mit einem neuen, PI3K-gamma-selektiven Hemmstoff (Inhibitor) bestätigen. Eine repetitive Dosierung des Hemmstoffes während der IgE-Exposition verhinderte die Einwanderung der Mastzell-Vorläufer. Dabei konnte die verabreichte Menge des Hemmstoffs auf ein Zehntel jener Menge reduziert werden, die für die Unterbindung der Degranulation von Gewebemastzellen nötig war.
«Umprogrammierung» des Enzyms
Romy Walser dokumentierte darauf die Kopplung des IgE-Rezeptors an die PI3K-gamma. Bisher wurde die PI3K-gamma nur mit G-Protein-gekoppelten Rezeptoren in Verbindung gebracht. In Mastzellen mit IgE- und Antigen-Exposition führt die Aggregation der IgE-Rezeptoren zu einem Anstieg der intrazellulären Kalziumionen (Ca2+), wodurch das Enzym Protein-Kinase C (PKC-beta) aktiviert wird. PKC-beta bringt dann einen Phosphatrest auf die PI3K-gamma, der wie ein molekularer Schalter wirkt. Die PI3K-gamma ist jetzt aktiv, kann aber nicht mehr durch G-Protein-gekoppelte Rezeptoren kontrolliert werden.
Wymann und seine Mitarbeiter hatten bereits früher gezeigt, dass die Hemmung von PI3K-gamma in chronischen Entzündungsmodellen, kardiovaskulären Prozessen und sogar bei der Einlagerung überschüssiger Kalorien ins Fettgewebe eine wichtige Rolle spielt. Die neu entdeckten Aktivierungsmechanismen für PI3K-gamma zeigen damit Wege auf, wie man die Lipidkinase langfristig zellspezifisch angreifen kann.
Originalbeiträge
Collmann et al.
Transient targeting of phosphoinositide 3-kinase acts as a roadblock in mast cells' route to allergy
J. Allergy Clin. Immunol. 2013 May 14. doi:pii: S0091-6749(13)00428-4.10.1016/j.jaci.2013.03.008. [Epub ahead of print]]
Walser et al.
PKC? Phosphorylates PI3K-gamma to Activate It and Release It from GPCR Control
PLOS Biol 11(6): e1001587. doi:10.1371/journal.pbio.1001587
Weitere Auskünfte
Prof. Matthias Wymann, Departement für Biomedizin der Universität Basel, Tel. +41 (0)61 695 30 46, E-Mail: matthias.wymann@unibas.ch
Weitere Informationen:
http://www.jacionline.org/article/S0091-6749%2813%2900428-4/abstract
– Abstract Collmann et al.
http://www.plosbiology.org/article/info%3Adoi%2F10.1371%2Fjournal.pbio.1001587
– Abstract Walser et al.
Media Contact
Weitere Informationen:
http://www.unibas.chAlle Nachrichten aus der Kategorie: Medizin Gesundheit
Dieser Fachbereich fasst die Vielzahl der medizinischen Fachrichtungen aus dem Bereich der Humanmedizin zusammen.
Unter anderem finden Sie hier Berichte aus den Teilbereichen: Anästhesiologie, Anatomie, Chirurgie, Humangenetik, Hygiene und Umweltmedizin, Innere Medizin, Neurologie, Pharmakologie, Physiologie, Urologie oder Zahnmedizin.
Neueste Beiträge

Bakterien für klimaneutrale Chemikalien der Zukunft
Forschende an der ETH Zürich haben Bakterien im Labor so herangezüchtet, dass sie Methanol effizient verwerten können. Jetzt lässt sich der Stoffwechsel dieser Bakterien anzapfen, um wertvolle Produkte herzustellen, die…

Batterien: Heute die Materialien von morgen modellieren
Welche Faktoren bestimmen, wie schnell sich eine Batterie laden lässt? Dieser und weiteren Fragen gehen Forschende am Karlsruher Institut für Technologie (KIT) mit computergestützten Simulationen nach. Mikrostrukturmodelle tragen dazu bei,…

Porosität von Sedimentgestein mit Neutronen untersucht
Forschung am FRM II zu geologischen Lagerstätten. Dauerhafte unterirdische Lagerung von CO2 Poren so klein wie Bakterien Porenmessung mit Neutronen auf den Nanometer genau Ob Sedimentgesteine fossile Kohlenwasserstoffe speichern können…





















