Wissenschaftler isolieren Nischenzellen aus Blutstammzellen
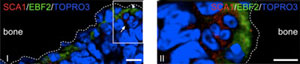
In disem Schnitt durch den Knochen einer Maus erkennt man die Knochenmatrix (schwarz), die Knochenmarkszellen (blau) und die EBF2-positiven Nischenzellen (grün). In der Vergrößerung des Bildes (rechts) sind auch rot-gefärbte Blutstammzellen ersichtlich. Bild: Max-Planck-Institut für Immunbiologie<br>
Wissenschaftler des Max-Planck Instituts für Immunbiologie in Freiburg und des Helmholtz Zentrums München ist es erstmals gelungen, gezielt Nischenzellen für Blutstammzellen, so genannte hämatopoietische Stammzellen, zu isolieren.
Die spezialisierten Nischenzellen bieten diesen Blutstammzellen geeignete Bedingungen, damit sie sich entwickeln, vermehren und ausdifferenzieren können. Die Ergebnisse könnten langfristig dazu beitragen, die Entstehung mancher Leukämien zu erklären und Blutzellen zur Transfusion zu züchten. (Cell Stem Cell, 8. Oktober 2010).
Knochenmark ist sehr heterogen, es besteht aus etwa 100 verschiedenen Zellen. Um Nischenzellen daraus zu isolieren, die nur in geringer Anzahl darin vorkommen, haben Rudolf Grosschedl und Gergana Dobreva vom Max Planck Institut für Immunbiologie in Freiburg gemeinsam mit Matthias Kieslinger und Silvia Hiechinger vom Helmholtz Zentrum München Knochenmarkzellen von Mäusen verwendet, bei denen ein Transkriptionsfaktor (EBF2) an ein spezielles Protein gekoppelt ist. Transkriptionsfaktoren bewerkstelligen generell die Regulation von Genen. Die EBF2-positiven Nischenzellen wurden angefärbt, von einem Gerät erkannt und aus der Vielzahl unterschiedlicher Zellen aussortiert.
Nischenzellen sind für die Blutbildung essentiell: Sie versorgen die Blutstammzellen mit optimalen Bedingungen, um zu reifen und die verschiedenen Typen von Blut- und Immunzellen ausbilden zu können. Das Wissen um die richtige Umgebung von Blutstammzellen eröffnet den Forschern neue Möglichkeiten bei der Vermehrung der Zellen in Kultur. So können die Wechselwirkungen der Nischenzellen mit den Blutstammzellen und die daran beteiligten Faktoren wesentlich besser untersucht werden.
Eine konkrete Anwendung wird von den Wissenschaftlern bereits erforscht: „Bei krankhaften Blutzellveränderungen, wie der chronisch lymphatischen Leukämie, könnten die Nischenzellen auch die Entwicklung von malignen hämatopoietischen Zellen beeinflussen“, sagt Matthias Kieslinger. Nach Ansicht von Rudolf Grosschedl wird „die Möglichkeit, Nischenzellen zu isolieren, auch für die Erforschung der Wechselwirkung mit Blutstammzellen und für das Verständnis der Balance zwischen Selbsterneuerung und Differenzierung von Stammzellen wichtig sein.“
Das Max-Planck-Institut für Immunbiologie in Freiburg ist ein interdisziplinäres Forschungsinstitut der Max-Planck-Gesellschaft. Der aktuelle Forschungsrahmen umfasst verschiedene Bereiche der modernen Immun- und Entwicklungsbiologie sowie der Epigenetik. Hierzu gehört der evolutionäre Ursprung des Immunsystems, die Entwicklung lymphoider Organe, Signalprozesse durch Antigen-Rezeptor Komplexe, Wirt/Pathogen-Interaktionen, entwicklungsbiologische Signalwege, die Regulation der Genexpression und der Chromatinstruktur, Zell-Zell-Interaktionen und die Zelldifferenzierung. Diese Forschung hilft, die Mechanismen der Bildung und der Funktion des Immunsystems und anderer biologischer Strukturen aufzuklären.
Das Helmholtz Zentrum München ist das deutsche Forschungszentrum für Gesundheit und Umwelt. Als führendes Zentrum mit der Ausrichtung auf Environmental Health erforscht es chronische und komplexe Krankheiten, die aus dem Zusammenwirken von Umweltfaktoren und individueller genetischer Disposition entstehen. Das Helmholtz Zentrum München beschäftigt rund 1.700 Mitarbeiterinnen und Mitarbeiter. Der Hauptsitz des Zentrums liegt in Neuherberg im Norden Münchens auf einem 50 Hektar großen Forschungscampus. Das Helmholtz Zentrum München gehört der größten deutschen Wissenschaftsorganisation, der Helmholtz-Gemeinschaft an, in der sich 16 naturwissenschaftlich-technische und medizinisch-biologische Forschungszentren mit etwa 30.000 Beschäftigten zusammengeschlossen haben. www.helmholtz-muenchen.de
Originalveröffentlichung:
Matthias Kieslinger, Silvia Hiechinger, Gergana Dobreva, G. Giacomo Consalez, Rudolf Grosschedl
Early B Factor 2 Regulates Homeostasis of Hematopoietic Stem Cells in a Cell Non-Autonomous Manner
Cell Stem Cells, 8. Oktober 2010
Weitere Informationen erhalten Sie von:
Prof. Dr. Rudolf Grosschedl,
Max-Planck-Institut für Immunbiologie, Freiburg
Tel.: +49 761 5108-711
Fax: +49 761 5108-799
E-Mail: grosschedl@immunbio.mpg.de
Dr. Matthias Kieslinger
Helmholtz Zentrum München – Deutsches Forschungszentrum für Gesundheit und Umwelt (GmbH), Neuherberg
Tel.: +49 89 7099-515
E-Mail: matthias.kieslinger@helmholtz-muenchen.de
Media Contact
Weitere Informationen:
http://www.mpg.deAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Anlagenkonzepte für die Fertigung von Bipolarplatten, MEAs und Drucktanks
Grüner Wasserstoff zählt zu den Energieträgern der Zukunft. Um ihn in großen Mengen zu erzeugen, zu speichern und wieder in elektrische Energie zu wandeln, bedarf es effizienter und skalierbarer Fertigungsprozesse…

Ausfallsichere Dehnungssensoren ohne Stromverbrauch
Um die Sicherheit von Brücken, Kränen, Pipelines, Windrädern und vielem mehr zu überwachen, werden Dehnungssensoren benötigt. Eine grundlegend neue Technologie dafür haben Wissenschaftlerinnen und Wissenschaftler aus Bochum und Paderborn entwickelt….

Dauerlastfähige Wechselrichter
… ermöglichen deutliche Leistungssteigerung elektrischer Antriebe. Überhitzende Komponenten limitieren die Leistungsfähigkeit von Antriebssträngen bei Elektrofahrzeugen erheblich. Wechselrichtern fällt dabei eine große thermische Last zu, weshalb sie unter hohem Energieaufwand aktiv…





















