Wie viel Signal braucht es, damit Immunzellen angreifen?
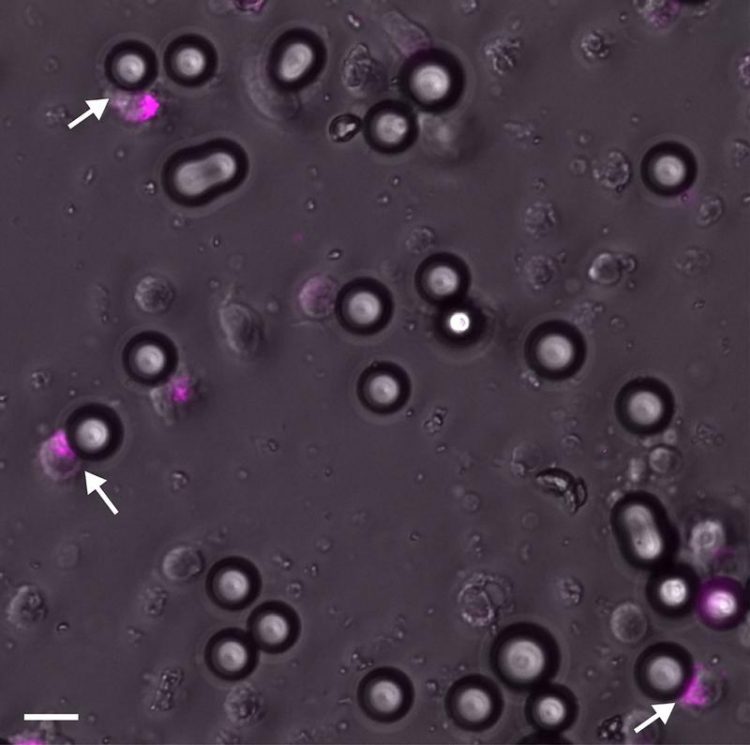
NK-Zellen und mit Antikörper beladenen Beads: Ein Aktivierungsmarker (pink) zeigt, dass diese NK-Zellen so viel Signal von den Beads erhalten haben, dass ihr Tötungsmechanismus eingeleitet wurde. Foto: Urlaub/IfADo
Natürliche Killerzellen sind Teil des angeborenen Immunsystems. Sie verdanken ihren Namen der Tatsache, dass sie virusinfizierte Zellen oder Tumorzellen sofort beim ersten Kontakt abtöten können. NK-Zellen besitzen also eine natürliche Zelltoxizität, was sie relevant für die Erforschung von Immuntherapien gegen Krebs macht.
Auf der Oberfläche der NK-Zellen befinden sich zahlreiche Rezeptoren. Das sind Sensoren, die mit Proteinen auf anderen Zellen interagieren und dann entweder über ein positives („abtöten“) oder negatives („nicht abtöten“) Signal die Aktivität der NK-Zellen beeinflussen.
Während man bestimmen kann, welches grundsätzliche Signal ein bekannter Rezeptor weiterleitet, ist unklar, wie stark ein Signal sein muss, um NK-Zellen zu steuern.
Immunologinnen und Immunologen des IfADo haben nun in einer Studie die Signalstärke quantitativ untersucht. Dazu haben sie „Latex Beads“ verwendet, Kügelchen in der Größe einer Immunzelle. Die Kügelchen haben die Forschenden mit sechs verschiedenen Antikörpern beladen.
Jeder der eingesetzten Antikörper richtet sich spezifisch gegen einen bestimmten aktivierenden Rezeptor auf der NK-Zelle. Durch die Bindung an diese Rezeptoren erhält die NK-Zelle ein positives Signal. Die Forschenden stellten für jede Antikörpersorte Varianten von Kügelchen mit unterschiedlich vielen Antikörpern her.
Die genaue Anzahl von Antikörpern pro Kügelchen haben sie mithilfe eines speziellen Messkits unter Einsatz der Durchflusszytometrie gemessen. Anschließend wurden die Kügelchen-Varianten zu im Labor kultivierten NK-Zellen von mehreren freiwilligen Blutspendern gegeben.
NK-Zellen haben unterschiedlich effektive Rezeptoren
„Wir wissen so genau, was und wie viel auf jedem Kügelchen ist und können untersuchen, wie reaktiv die NK-Zellen sind. So ein gut kontrollierbares, stabiles System kann mit Tumorzellen, die unzählige, teilweise noch unbekannte Oberflächenproteinen haben, nicht dargestellt werden“, erklärt Dr. Doris Urlaub, wissenschaftliche Mitarbeiterin in der IfADo-Forschungsabteilung Immunologie.
Das quantitative Vorgehen ergab u.a., dass die aktivierenden Rezeptoren unterschiedlich effektiv darin sind, NK-Zellen anzuregen. So fiel ein Rezeptor auf, der schon bei vergleichsweise niedriger Antikörperanzahl eine maximale NK-Zell-Aktivität auslöste.
Die Stimulation eines anderen Rezeptors konnte die NK-Zellen hingegen kaum dazu anregen, ihren Tötungsprozess einzuleiten. Wie die Forschenden zeigen konnten, stand die unterschiedliche Effektivität der Rezeptoren nicht in Verbindung mit der Anzahl der Rezeptoren auf den NK-Zellen.
Weiterhin ergaben die Daten, dass nur eine bestimmte Gruppe von Rezeptoren in der Lage war, dass NK-Zellen sowohl ihren Tötungsmechanismus einleiten, als auch Proteine ausschütten, die im Körper wichtig für die weitere Immunantwort sind.
Nächster Schritt: Kügelchen mit Liganden beladen
Mit der aktuellen Veröffentlichung konnten die IfADo-Forschenden zeigen, dass ihr Ansatz funktioniert.
„Um die Stimulation der NK-Zellen jedoch natürlicher zu gestalten, möchten wir die Kügelchen nun anstatt mit Antikörpern mit den deutlich aufwendiger herzustellenden Proteinen (Liganden) beladen, die etwa auf kranken Zellen zu finden sind. Die Liganden gehen eine spezifische Bindung mit aktivierenden Rezeptoren der NK-Zellen ein“, erklärt Doris Urlaub.
Langfristig wollen die Forschenden mit ihrem Ansatz dazu beitragen, umfassend quantitativ zu beurteilen, welcher Rezeptor in welcher Weise zur NK-Zellaktivität beiträgt. Dieses Wissen könnte es zukünftig ermöglichen, die Reaktion von NK-Zellen auf Tumorzellen vorherzusagen.
Prof. Dr. Carsten Watzl
Leiter der IfADo-Forschungsabteilung „Immunologie“
Telefon: + 49 231 1084-233
E-Mail: watzl@ifado.de
Dorsch, M., Urlaub, D., Bönnemann, V., Bröder, P., Sandusky, M., Watzl, C.: Quantitative analysis of human NK cells reactivity using latex beads coated with defined amounts of antibodies. Eur. J. Immunol. 2020. 00: 1–10. doi: https://doi.org/10.1002/eji.201948344
https://www.ifado.de/2020/03/16/nk-zellen-signal-messen/ IfADo-Pressemitteilung
https://www.ifado.de/immunologie/ Immunologie-Forschungsabteilung IfADo
https://doi.org/10.1002/eji.201948344 Originalpublikation (Open Access)
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Anlagenkonzepte für die Fertigung von Bipolarplatten, MEAs und Drucktanks
Grüner Wasserstoff zählt zu den Energieträgern der Zukunft. Um ihn in großen Mengen zu erzeugen, zu speichern und wieder in elektrische Energie zu wandeln, bedarf es effizienter und skalierbarer Fertigungsprozesse…

Ausfallsichere Dehnungssensoren ohne Stromverbrauch
Um die Sicherheit von Brücken, Kränen, Pipelines, Windrädern und vielem mehr zu überwachen, werden Dehnungssensoren benötigt. Eine grundlegend neue Technologie dafür haben Wissenschaftlerinnen und Wissenschaftler aus Bochum und Paderborn entwickelt….

Dauerlastfähige Wechselrichter
… ermöglichen deutliche Leistungssteigerung elektrischer Antriebe. Überhitzende Komponenten limitieren die Leistungsfähigkeit von Antriebssträngen bei Elektrofahrzeugen erheblich. Wechselrichtern fällt dabei eine große thermische Last zu, weshalb sie unter hohem Energieaufwand aktiv…





















