Protonentransfer: Forscher finden molekularen Schutzmechanismus gegen lichtinduzierte Schädigungen
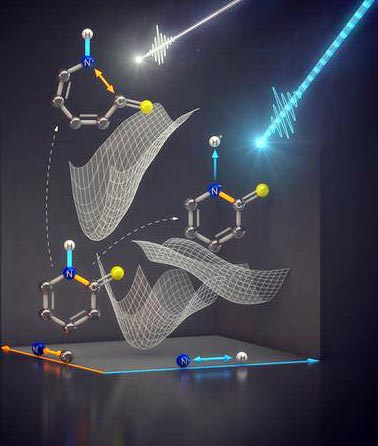
Die Experimente zeigen: Lichtpulse können Wasserstoffkerne ablösen, ohne weitere Bindungen im Molekül zu zerstören. Bild: Th. Splettstösser/HZB
Biomoleküle wie die Erbsubstanz DNA benötigen Schutzmechanismen gegen energiereiches Licht. Denn UV-Anteile aus dem Sonnenlicht würden sonst rasch dazu führen, dass Bindungen brechen und Moleküle zerfallen. Der so genannte Protonentransfer spielt dabei eine wichtige Rolle. Mit ihm kann ein DNA-Molekül die über das Licht eingestrahlte Energie wieder abgeben – dabei löst sich ein einzelnes Proton (Wasserstoffkern) – und andere chemische Bindungen bleiben erhalten.
Um den Prozess im Detail zu untersuchen, hat eine internationale Kooperation um Prof. Dr. Alexander Föhlisch, Institutsleiter am Helmholtz-Zentrum Berlin, in Kalifornien am LCLS-Laser des SLAC National Accelerator Laboratory und an der Berliner Synchrotronquelle BESSY II des HZB Experimente durchgeführt: Sie untersuchten ein verhältnismäßig einfaches Molekül, das 2-Thiopyridon (2-TP). Dieses Molekül hat ähnliche Eigenschaften wie die Bausteine der DNA und dient in der Bioforschung deshalb als Modellmolekül.
Die Forschergruppe regte zunächst gezielt das Stickstoff-Atom im Molekül mit sehr kurzen Röntgenpulsen im Femtosekundenbereich (10 -15 s) an. Die Ergebnisse, die nun im Fachblatt Angewandte Chemie publiziert sind, zeigen im Detail, wie sich nach der Anregung mit dem Lichtpuls das an das Stickstoff-Atom gebundene Proton ablöst.
„Erst einmal wollten wir diese Prozesse an einem einfachen Modellsystem untersuchen,” sagt Erstautor Sebastian Eckert, der bei Alexander Föhlisch an der Universität Potsdam und am Helmholtz-Zentrum Berlin seine Doktorarbeit schreibt. “ Das Modellsystem 2-Thiopyridon ist geeignet, weil das Molekül klein genug ist, um es zu verstehen und nur ein einziges Stickstoff-Atom besitzt.
Nur durch den Vergleich zwischen den FEL-Messungen und Experimenten am Synchrotron BESSY II ließ sich der Mechanismus eindeutig zuordnen.“ Dabei hatte das Team erstmals auch die Methode der so genannten inelastischen Röntgenstreuung, RIXS, an BESSY II angewandt, um molekulare Veränderungen um das Stickstoff-Atom herum zu beobachten, die mit dem raschen Protonentransfer zusammenhängen und extrem schnell, innerhalb von Femtosekunden, ablaufen.
Durch die Kombination der Experimente mit theoretischen Simulationen konnte letzlich der Reaktionspfad herausgearbeitet werden. Diese Berechnungen führte der Doktorand Jesper Norell und Prof. Dr. Michael Odelius der Universität Stockholm im Rahmen des Helmholtz Virtuellen Instituts „Dynamic Pathways in Multidimensional Landscapes“ durch.
Zur Publikation in Angewandte Chemie, International Edition, 2017, doi:10.1002/anie.201700239:“Ultrafast Independent N-H and N-C Bond Deformation Investigated with Resonant Inelastic X-ray Scattering“ Sebastian Eckert;, Jesper Norell;, Piter S. Miedema, Martin Beye,Mattis Fondell, Wilson Quevedo, Brian Kennedy, Markus Hantschmann,Annette Pietzsch, Benjamin Van Kuiken, Matthew Ross,Michael P. Minitti, Stefan P. Moeller, William F. Schlotter, Munira Khalil, Michael Odelius, Alexander Föhlisch.
Zur Kooperation: Die Kooperation besteht aus Wissenschaftlern der Universität Potsdam, des Helmholtz-Zentrum Berlin, der Universität Stockholm, der Universität Washington und LCLS (SLAC National Accelerator Laboratory, operated by Stanford University for the U.S. Department of Energy's Office of Science). Sebastian Eckert promoviert im Rahmen des ERC Advanced Grants EDAX von Prof. Dr. Alexander Föhlisch an der Universität Potsdam. Jesper Norell und Michael Odelius kollaborieren in Rahmen des Virtuellen Instituts VI419 „Dynamic Pathways in Multidimensional Landscapes“ der Helmholtz-Gemeinschaft.
Kontakt zum Experten:
Prof. Dr. Alexander Föhlisch
Tel: (030) 8062-14985
E-Mail: alexander.foehlisch@helmholtz-berlin.de
Pressestelle HZB
Dr. Antonia Rötger
Tel. (030) 8062-43733
E-Mail: antonia.roetger@helmholtz-berlin.de
http://www.helmholtz-berlin.de/pubbin/news_seite?nid=14646&sprache=de&ty…
http://onlinelibrary.wiley.com/doi/10.1002/anie.201700239/abstract;jsessionid=E1…
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Bakterien für klimaneutrale Chemikalien der Zukunft
Forschende an der ETH Zürich haben Bakterien im Labor so herangezüchtet, dass sie Methanol effizient verwerten können. Jetzt lässt sich der Stoffwechsel dieser Bakterien anzapfen, um wertvolle Produkte herzustellen, die…

Batterien: Heute die Materialien von morgen modellieren
Welche Faktoren bestimmen, wie schnell sich eine Batterie laden lässt? Dieser und weiteren Fragen gehen Forschende am Karlsruher Institut für Technologie (KIT) mit computergestützten Simulationen nach. Mikrostrukturmodelle tragen dazu bei,…

Porosität von Sedimentgestein mit Neutronen untersucht
Forschung am FRM II zu geologischen Lagerstätten. Dauerhafte unterirdische Lagerung von CO2 Poren so klein wie Bakterien Porenmessung mit Neutronen auf den Nanometer genau Ob Sedimentgesteine fossile Kohlenwasserstoffe speichern können…





















