Ohne Eisen-Schwefel-Cluster geht nichts
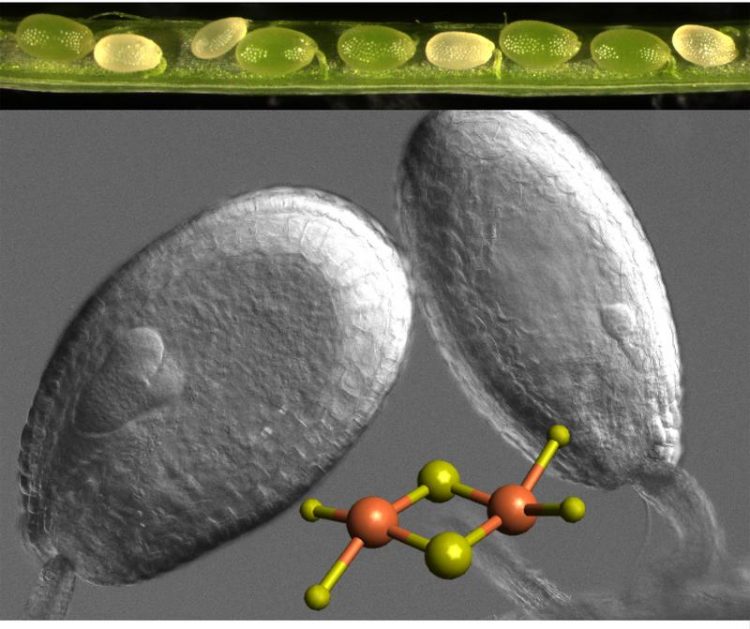
Oben: Geöffnete Schote einer Glutaredoxin S15- Arabidopsis-Mutante. Die weißen Samen sterben ab. Unten: Zwei Samenanlagen mit sich entwickelndem Embryo (links: Wildtyp; rechts: Mutante). © Darstellung: AG Meyer/Uni Bonn
Bei einem Brand bilden die Nachbarn eine Kette und reichen den Wassereimer von Hand zu Hand bis zum Brandherd. Ähnliche Ketten gibt es in den Zellen auch. Statt Wasser werden in ihnen Elektronen weitergereicht.
Die einzelnen Kettenglieder bestehen aus Proteinen. Um Elektronen an das nächste Glied übergeben zu können, benötigen sie einen mineralischen Komplex aus Eisen und Schwefel, der dem Katzengold Pyrit ähnelt. Dieser Komplex kann kurzzeitig mit Elektronen „befüllt“ werden; diesen Vorgang bezeichnet man als Reduktion. Er kann diese Elektronen aber auch wieder abgeben; Chemiker nennen das Oxidation.
Derartige Redoxketten wurden schon sehr früh im Laufe der Evolution erfunden. Es gibt sie in allen Lebewesen, egal ob in Pflanzen, Tieren oder Bakterien. Sie finden sich vor allem dort, wo Energie umgesetzt wird. Wenn wir etwa zur Energiegewinnung Zucker zu Wasser und Kohlendioxid „verbrennen“ (= oxidieren), werden dabei Elektronen übertragen. Bei der Fotosynthese läuft dieser Vorgang in Gegenrichtung ab.
Weitgehend ungeklärt war bislang, wie die Proteine mit dem Eisen-Schwefel-Komplex versehen werden, den sie zur Weitergabe der Elektronen benötigen. Das Forscherteam aus Bonn, Marburg, Düsseldorf und Nancy hat nun ein Protein identifiziert, das vermutlich diesen Transferschritt vermittelt. Fündig wurden sie in bestimmten Zellbestandteilen der Ackerschmalwand Arabidopsis thaliana, den so genannten Mitochondrien. Mitochondrien gelten als „Kraftwerke“ der Zelle: In ihnen finden verschiedene metabolische Prozesse zur Oxidation von Nährstoffen und damit letztlich zur Energiegewinnung statt, unter anderem der so genannte Zitratzyklus.
Tödliche Mutation
Damit diese Abläufe im Kraftwerk funktionieren, braucht die Pflanze augenscheinlich ein Protein namens Glutaredoxin S15. „Wir konnten zeigen, dass die Ackerschmalwand ohne Glutaredoxin S15 nicht lebensfähig ist“, erklärt Prof. Dr. Andreas J. Meyer vom Institut für Nutzpflanzenwissenschaften und Ressourcenschutz der Uni Bonn. „Um zu untersuchen, warum die Pflanze stirbt, haben wir das defekte Glutaredoxin S15 durch eine Kopie mit verminderter Aktivität ersetzt. Dabei entstanden Pflanzen, in denen wesentliche Komponenten des Zitratzyklus nicht funktionierten.“
Möglicherweise bringt Glutaredoxin S15 die Eisen-Schwefel-Cluster zu den Zielproteinen, die sie als Katalysator benötigen. Ein solcher Zusammenhang wurde schon lange vermutet; ein Beweis dafür stand aber noch aus. „Unsere Ergebnisse untermauern die Bedeutung des Glutaredoxin S15 bei diesem Prozess“, erklärt Anna Moseler, Doktorandin in der Arbeitsgruppe von Prof. Meyer.
Eisen-Schwefel-Cluster haben eine grundlegende Bedeutung für die gesamte Bioenergetik. Die an der Modellpflanze Ackerschmalwand gewonnenen Erkenntnisse sind daher auch für Nutzpflanzen enorm wichtig. Darüber hinaus tragen die Ergebnisse zu einem besseren Verständnis des Mineralstoffhaushalts in Pflanzen bei. Glutaredoxine sind zudem anfällig für stressbedingte oxidative Veränderungen. Daher könnten die Erkenntnisse langfristig auch dabei helfen, Pflanzen mit verbesserter Stresstoleranz zu züchten. „Das wäre ein wichtiger Schritt auf dem Weg zu Nutzpflanzen-Sorten, die in der Lage sind, sich bei widrigen Bedingungen selbst zu helfen, und so zur Sicherung der Nahrungsmittelversorgung beitragen“, betont Meyer.
Publikation: Anna Moseler, Isabel Aller, Stephan Wagner, Thomas Nietzel, Jonathan Przybyla-Toscano, Ulrich Mühlenhoff, Roland Lill, Carsten Berndt, Nicolas Rouhier, Markus Schwarzländer, and Andreas J. Meyer: The mitochondrial monothiol glutaredoxin S15 is essential for iron-sulfur protein maturation in Arabidopsis thaliana; PNAS Early Edition; DOI: 10.1073/pnas.1510835112
Kontakt für die Medien:
Prof. Dr. Andreas Meyer
Institut für Nutzpflanzenwissenschaften und Ressourcenschutz
Universität Bonn
Tel. 0228/73-60331 oder -60353
E-Mail: andreas.meyer@uni-bonn.de
Media Contact
Weitere Informationen:
http://www.uni-bonn.de/Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Merkmale des Untergrunds unter dem Thwaites-Gletscher enthüllt
Ein Forschungsteam hat felsige Berge und glattes Terrain unter dem Thwaites-Gletscher in der Westantarktis entdeckt – dem breiteste Gletscher der Erde, der halb so groß wie Deutschland und über 1000…

Wasserabweisende Fasern ohne PFAS
Endlich umweltfreundlich… Regenjacken, Badehosen oder Polsterstoffe: Textilien mit wasserabweisenden Eigenschaften benötigen eine chemische Imprägnierung. Fluor-haltige PFAS-Chemikalien sind zwar wirkungsvoll, schaden aber der Gesundheit und reichern sich in der Umwelt an….

Das massereichste stellare schwarze Loch unserer Galaxie entdeckt
Astronominnen und Astronomen haben das massereichste stellare schwarze Loch identifiziert, das bisher in der Milchstraßengalaxie entdeckt wurde. Entdeckt wurde das schwarze Loch in den Daten der Gaia-Mission der Europäischen Weltraumorganisation,…