Geschwindigkeitskontrolle auf der DNA
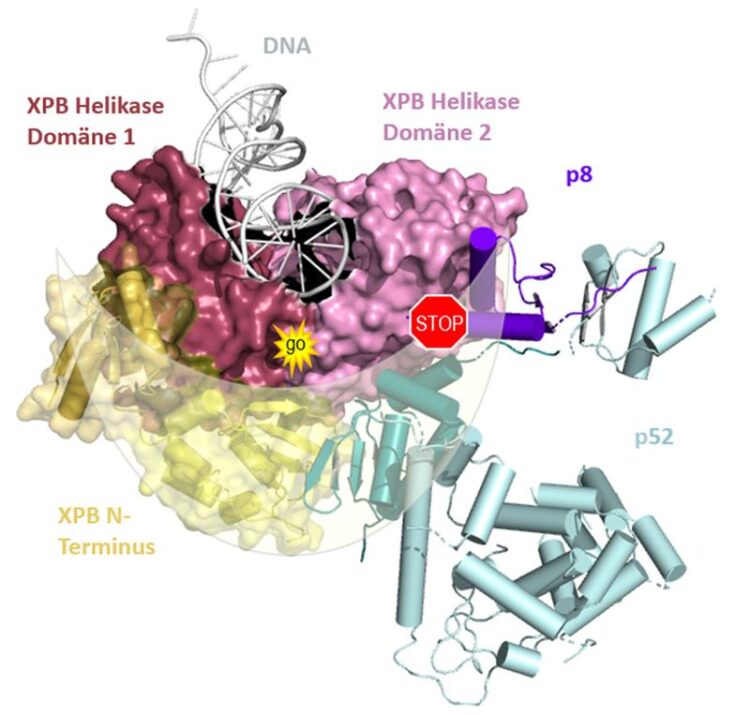
The two enzymatically active domains of XPB (pink/red) are enclosed by a lunate-like ring formed by p52/p8 (turquoise/purple). This activates the enzyme and simultaneously restricts its mobility, i.e. slows down the activity.
AG Kisker, RVZ
Für essentielle zelluläre Funktionen wie das Ablesen der Gene oder die Reparatur von DNA-Schäden, ist unter anderem der Proteinkomplex TFIIH zuständig. Diese Vorgänge müssen extrem präzise ablaufen, um schwere Krankheiten, wie beispielsweise die Entstehung von Krebs, zu vermeiden. Das Enzym XPB ist Teil des TFIIH Komplexes und unabdingbar für beide Prozesse. Wie XPB durch seine Interaktionspartner p8/p52 innerhalb des TFIIH Komplexes gleichzeitig aktiviert und gebremst wird, konnte eine Würzburger Forschungsgruppe nun zeigen. Die Ergebnisse verbessern das genaue Verständnis der Funktion dieses Komplexes und wurden im Fachjournal Nucleic Acids Research veröffentlicht.
DNA-Schäden, die repariert werden müssen, und Gene, die abgelesen werden sollen: für beide Prozesse ist das Enzym XPB, das Teil des TFIIH Komplexes ist, essentiell. Wie wichtig ein korrekt arbeitendes XPB ist zeigt, dass eine Fehlfunktion desselben zu den schweren Krankheiten Xeroderma Pigmentosum und Trichothiodystrophie führen kann.
Die Forschungsgruppe von Prof. Caroline Kisker vom Rudolf-Virchow-Zentrum – Center for Integrative and Translational Bioimaging der Universität Würzburg konnte nun zeigen, dass die TFIIH Untereinheiten p52/p8 die Funktionalität des Enzyms XPB kontrollieren, indem sie es einerseits aktivieren und andererseits dafür sorgen, dass es nicht zu schnell arbeitet. Diese Ergebnisse verbessern das Verständnis des Proteinkomplexes TFIIH und seiner wichtigen Funktionen.
Feinjustierung der Geschwindigkeit von XPB
Während der Transkription bindet XPB an die Doppelhelix der DNA, wandert an ihr entlang und bewirkt somit, dass die beiden Stränge aufgetrennt werden, damit die Gene abgelesen werden können. Um das Enzym zu aktivieren, müssen die beiden Untereinheiten von XPB (im Bild rosa und rot) in enge räumliche Nähe zueinander gebracht werden. Diese Annäherung wird zum einen dadurch erreicht, dass p8/p52 an XPB bindet, oder, in noch stärkerem Ausmaß, wenn DNA gebunden wird.
„Sind beide aktivierenden Faktoren simultan gebunden, würde man eigentlich vermuten, dass die stärkere Aktivierung sich durchsetzt, das Gegenteil ist aber der Fall“, sagt Dr. Jochen Kuper der als Postdoktorand in der Arbeitsgruppe forscht. „Mit unserer Struktur- und Funktionsanalyse konnten wir zeigen, dass durch p52/p8 die Beweglichkeit der Enzymuntereinheiten eingeschränkt wird. P52/p8 wirkt also wie eine Bremsbacke und verlangsamt die Geschwindigkeit von XPB“, erklärt Kisker.
Dadurch wird sichergestellt, dass XPB korrekt arbeitet, denn während der Transkription und während der DNA Reparatur ist eine exakte Regulierung des Enzyms essentiell. In der vorgelegten Arbeit hat das Forscherteam nun p52/p8 als Masterregulatoren von XPB identifiziert. „Unsere Ergebnisse erklären auch, warum eine Mutation in so einer winzigen Untereinheit wie p8, so schwerwiegende Folgen haben kann, wie die Erkrankung an Trichothiodystrophie“, sagt Jeannette Kappenberger, Doktorandin in der Arbeitsgruppe Kisker und Erstautorin der Studie.
Die Wissenschaftlerinnen und Wissenschaftler planen nun weitere strukturelle und funktionale Untersuchungen der Proteine. Außerdem möchten sie herausfinden, wie der Komplex mittels Inhibitoren gezielt beeinflusst werden kann.
Personen
Jeannette Kappenberger forscht als Doktorandin in der Arbeitsgruppe von Prof. Dr. Caroline Kisker am Rudolf-Virchow-Zentrum – Center for Integrative and Translational Bioimaging der Universität Würzburg.
Dr. Jochen Kuper (Postdoktorand) forscht in der Arbeitsgruppe von Prof. Dr. Caroline Kisker am Rudolf-Virchow-Zentrum – Center for Integrative and Translational Bioimaging der Universität Würzburg.
Prof. Dr. Caroline Kisker ist unter anderem Leiterin des Lehrstuhls für Strukturbiologie und Dekanin der Graduate School of Life Sciences der Universität Würzburg. Sie ist die Sprecherin des Rudolf-Virchow-Zentrum – Center for Integrative and Translational Bioimaging der Universität Würzburg. Mehr Informationen: https://www.uni-wuerzburg.de/rvz/lehrstuehle/lehrstuhl-fuer-strukturbiologie/abo…
Wissenschaftliche Ansprechpartner:
Prof. Dr. Caroline Kisker (Rudolf-Virchow-Zentrum, Universität Würzburg)
Tel.: +49 (0)931 31 80381, caroline.kisker@virchow.uni-wuerzburg.de
Originalpublikation:
Kappenberger J., Koelmel W., Schoenwetter E., Scheuer T., Woerner, J., Kuper J., Kisker C. How to limit the speed of a motor: The intricate regulation of the XPB ATPase and Translocase in TFIIH Nucleic Acids Research (November 2020) doi: 10.1093/nar/gkaa911
Weitere Informationen:
https://www.uni-wuerzburg.de/de/rvz/neuigkeiten/single/news/geschwindigkeitskont…
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Anlagenkonzepte für die Fertigung von Bipolarplatten, MEAs und Drucktanks
Grüner Wasserstoff zählt zu den Energieträgern der Zukunft. Um ihn in großen Mengen zu erzeugen, zu speichern und wieder in elektrische Energie zu wandeln, bedarf es effizienter und skalierbarer Fertigungsprozesse…

Ausfallsichere Dehnungssensoren ohne Stromverbrauch
Um die Sicherheit von Brücken, Kränen, Pipelines, Windrädern und vielem mehr zu überwachen, werden Dehnungssensoren benötigt. Eine grundlegend neue Technologie dafür haben Wissenschaftlerinnen und Wissenschaftler aus Bochum und Paderborn entwickelt….

Dauerlastfähige Wechselrichter
… ermöglichen deutliche Leistungssteigerung elektrischer Antriebe. Überhitzende Komponenten limitieren die Leistungsfähigkeit von Antriebssträngen bei Elektrofahrzeugen erheblich. Wechselrichtern fällt dabei eine große thermische Last zu, weshalb sie unter hohem Energieaufwand aktiv…





















