Der Sonnenschutz der DNA
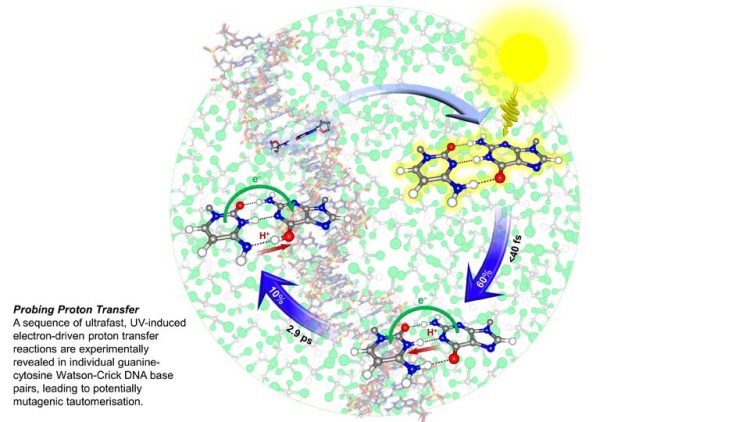
Die Studie aus Kiel und Bristol wird das Innencover der Fachzeitschrift Angewandte Chemie zieren. Es zeigt den untersuchten Prozess, wie die DNA sich vor ultravioletter Strahlung schützt. Angewandte Chemie, John Wiley & Sons
UV-Strahlung zählt zu den häufigsten Ursachen für Schäden an unserem Erbgut. Forscherinnen und Forscher der Christian-Albrechts-Universität zu Kiel (CAU) und der Universität Bristol, Großbritannien, haben nun erstmals beobachtet, was in DNA-Bausteinen passiert, wenn sie mit ultraviolettem Licht angeregt werden und wie sie sich dabei vor ihrer Zerstörung schützen.
Die Ergebnisse zeigen: Mit der aufgenommenen Energie setzen die Moleküle eine völlig ungefährliche Reaktion in Gang, die Veränderungen der Gene verhindert. Die Studie erscheint in der aktuellen Ausgabe der Fachzeitschrift Angewandte Chemie.
In unserer DNA treten die Basen Adenin, Guanin, Cytosin und Thymin auf. Mit ultrakurzen Lichtblitzen schossen die Chemikerinnen und Chemiker auf mit UV-Licht angeregte Basenpaare aus Guanin und Cytosin. Nur mit Hilfe dieser als Femtosekundenspektroskopie bezeichneten Methode konnten sie den schützenden molekularen Mechanismus offenlegen. Denn dieser spielt sich innerhalb weniger Billiardstel Sekunden ab.
In dem sogenannten elektronengetriebenen Protonentransfer-Prozess (EDPT) wird ein Wasserstoff-Atom innerhalb der Molekülverbindung verschoben. Das Basenpaar kehrt daraufhin aber durch den gleichen Vorgang sofort wieder zur Ausgangsstruktur zurück. „Die Natur nutzt die Reaktion, um die Lichtbeständigkeit des Erbguts um Größenordnungen zu verstärken – sie ist sozusagen der Sonnenschutz der DNA“, sagt Professor Friedrich Temps, Leiter des Kieler Forschungsteams vom Institut für Physikalische Chemie.
„Die DNA-Bausteine selbst entlasten dadurch die enorm aufwändigen und nur sehr langsamen aktiven Reparaturmechanismen der Zellen durch Enzyme, für deren Entdeckung in diesem Jahr gerade der Nobelpreis für Chemie verliehen wurde. Ohne die von uns beobachteten passiven Prozesse wären die aktiven Reparaturmaschinen der Zellen hoffnungslos überlastet“, ergänzt Professor Andrew Orr-Ewing, Leiter des Teams in Bristol.
In einigen Fällen gelingt es dem Basenpaar jedoch nicht, zur Ausgangssituation zurückzukehren. Hier führt der EDPT dazu, dass zwei Wasserstoffatome verschoben werden. „Das Produkt könnte eine mutagene Vorstufe sein und zu Schäden an der DNA führen“, erklärt Dr. Katharina Röttger von der englischen Arbeitsgruppe, die in Kiel ihren Doktortitel erhielt. Was allerdings mit diesem Molekül weiter passiert, müssen zukünftige Experimente zeigen. „Wir können nur sagen, dass das potenziell mutagene Molekül den Zeitrahmen unserer Messungen von einer Nanosekunde (= eine Milliardstel Sekunde) überlebt“, sagt Röttger.
Die Wissenschaftlerinnen und Wissenschaftler wollen nun herausfinden, ob die gleichen Prozesse auch in einem langen DNA-Strang passieren. Kompliziert machen dieses Unterfangen aber die vielen Wechselwirkungen innerhalb und zwischen den Molekülen und in den Wasserstoffbrücken. Oft werden extrem schnelle Reaktionen von langsameren überdeckt. Professor Temps und Professor Orr-Ewing sind zuversichtlich, dass die Analysewerkzeuge ihrer Arbeitsgruppen bald so weit sein werden, auch dieses Rätsel zu lösen.
Originalpublikation
K. Röttger, H. J. B. Marroux, M. P. Grubb, P. M. Coulter, H. Böhnke, A. S. Henderson, M. C. Galan, F. Temps, A. J. Orr-Ewing, G. M. Roberts, „Ultraviolet Absorption Induces Hydrogen-Atom Transfer in G∙C Watson-Crick DNA Base Pairs in Solution“, Angew. Chem. Int. Ed. 54, (2015). DOI: 10.1002/anie.201506940
Link: http://onlinelibrary.wiley.com/doi/10.1002/anie.201506940/abstract
Bildmaterial steht zum Download bereit:
http://www.uni-kiel.de/download/pm/2015/2015-368-1.png
Bildunterschrift: Katharina Röttger, Fakultätspreisträgerin 2014 der Universität Kiel, untersuchte mittels extrem kurzer Lichtpulse gemeinsam mit Kolleginnen und Kollegen einen chemischen Prozess in DNA-Basenpaaren.
Foto/Copyright: Jürgen Haacks, Uni Kiel
http://www.uni-kiel.de/download/pm/2015/2015-368-2.jpg
Bildunterschrift: Friedrich Temps entwickelt in Kiel Methoden, mit denen sich ultraschnelle chemische Prozesse beobachten lassen.
Foto/Copyright: Denis Schimmelpfennig, Uni Kiel
http://www.uni-kiel.de/download/pm/2015/2015-368-3.jpg
Bildunterschrift: Die Studie aus Kiel und Bristol wird das Innencover der Fachzeitschrift Angewandte Chemie zieren. Es zeigt den untersuchten Prozess, wie die DNA sich vor ultravioletter Strahlung schützt.
Abbildung/Copyright: Angewandte Chemie, John Wiley & Sons
Weitere Informationen (in Englisch):
http://www.temps.phc.uni-kiel.de/en
Details, die nur Millionstel Millimeter groß sind: Damit beschäftigt sich der Forschungsschwerpunkt „Nanowissenschaften und Oberflächenforschung“ (Kiel Nano, Surface and Interface Science – KiNSIS) an der Christian-Albrechts-Universität zu Kiel (CAU). Im Nanokosmos herrschen andere, nämlich quantenphysikalische, Gesetze als in der makroskopischen Welt. Durch eine intensive interdisziplinäre Zusammenarbeit zwischen Materialwissenschaft, Chemie, Physik, Biologie, Elektrotechnik, Informatik, Lebensmitteltechnologie und verschiedenen medizinischen Fächern zielt der Schwerpunkt darauf ab, die Systeme in dieser Dimension zu verstehen und die Erkenntnisse anwendungsbezogen umzusetzen. Molekulare Maschinen, neuartige Sensoren, bionische Materialien, Quantencomputer, fortschrittliche Therapien und vieles mehr können daraus entstehen. Mehr Informationen auf www.kinsis.uni-kiel.de
Kontakt:
Professor Dr. Friedrich Temps
Institut für Physikalische Chemie
Tel.: 0431/880 7800
E-Mail: temps@phc.uni-kiel.de
Media Contact
Weitere Informationen:
http://www.uni-kiel.deAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Entscheidender Durchbruch für die Batterieproduktion
Energie speichern und nutzen mit innovativen Schwefelkathoden. HU-Forschungsteam entwickelt Grundlagen für nachhaltige Batterietechnologie. Elektromobilität und portable elektronische Geräte wie Laptop und Handy sind ohne die Verwendung von Lithium-Ionen-Batterien undenkbar. Das…

Wenn Immunzellen den Körper bewegungsunfähig machen
Weltweit erste Therapie der systemischen Sklerose mit einer onkologischen Immuntherapie am LMU Klinikum München. Es ist ein durchaus spektakulärer Fall: Nach einem mehrwöchigen Behandlungszyklus mit einem immuntherapeutischen Krebsmedikament hat ein…
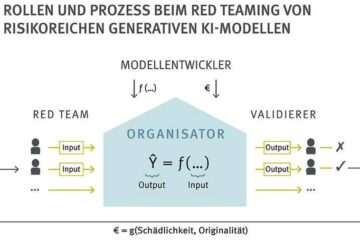
So soll risikoreiche generative KI geprüft werden
Die beschlossene KI-Verordnung der EU sieht vor, dass Künstliche-Intelligenz-Modelle (KI) „für allgemeine Zwecke mit systemischem Risiko“ besonders strikt überprüft werden. In diese Modellkategorie gehören auch populäre generative KI-Modelle wie GPT4…





















