Blick ins Innere einer Zell-Antenne
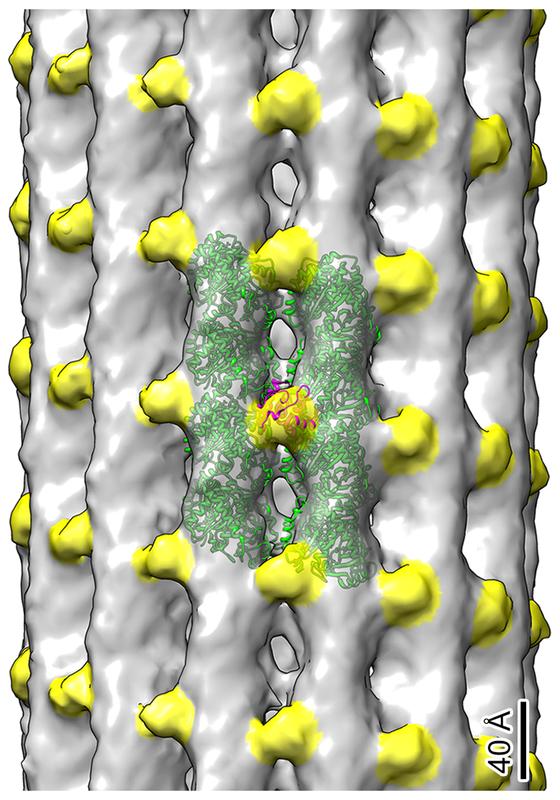
Cryo-electron tomography showing tubulin dimers (in green) and EB1 proteins (in yellow) located along the microtubules of the kidney primary cilium. The functional role of this peculiar distribution of EB1 is now under investigation.
Kiesel et al. in Nature Structural & Molecular Biology / MPI-CBG
Dresdner Forscher entwickeln neue Methode und entdecken damit neue Merkmale von primären Zilien, wenig verstandene antennenartige Strukturen, die aus Zellen herausragen.
Zellen tasten ihre Umgebung ab und senden Signale an andere Zellen. Das ist wichtig, damit eine Zelle richtig funktionieren kann. Das verantwortliche „Organ“ für diese Aufgaben ist das Zilium, eine antennenartige Struktur, die aus den meisten Zellen von Wirbeltieren herausragt. Es gibt zwei Arten von Zilien: bewegliche und nicht bewegliche. Während die beweglichen Zilien umfassend erforscht wurden, sind die dreidimensionale Architektur und die molekulare Zusammensetzung der nicht-beweglichen Zilien, auch primäre Zilien genannt, weitgehend unbekannt.
Nahezu alle Zelltypen von Säugetieren haben ein primäres Zilium. Die Forschungsgruppe von Gaia Pigino am Max-Planck-Institut für molekulare Zellbiologie und Genetik (MPI-CBG) in Dresden hat nun eine Methode entwickelt, um die Struktur der primären Zilien mit molekularer Auflösung mittels Kryo-Elektronentomographie zu untersuchen. Diese Arbeit liefert wichtige Einblicke in die Biologie der primären Zilien und einen methodischen Ansatz zur weiteren Untersuchung dieser Organellen unter verschiedenen gesunden und krankhaften Bedingungen.
Als Menschen verlassen wir uns auf unsere Sinne, wie Hören, Sehen, Schmecken oder Riechen, um unsere Umwelt zu erkunden. Einzelne Zellen dagegen nehmen ihre Umwelt durch Zilien wahr, antennenartige Strukturen, die aus den meisten Wirbeltierzellen herausragen. Zilien ermöglichen es den Zellen, sich zu bewegen, zu kommunizieren und molekulare Signale zu interpretieren.
Im Inneren eines Ziliums befindet sich ein auf Mikrotubuli beruhendes Zytoskelett, das bei beweglichen Zilien bisher ziemlich umfassend untersucht wurde. Das Gegenteil trifft auf die primären Zilien zu, die lange Zeit als ein Überbleibsel der Evolution und fälschlicherweise als eine vereinfachte Version der beweglichen Zilien angesehen wurden. Aber im Gegensatz zu den beweglichen Zilien, die sich nur auf einigen Zelltypen in unserem Körper befinden, haben die meisten unserer Zellen primäre Zilien.
Die Riech- und Sinneszilien zum Beispiel ermöglichen es uns zu riechen und die Fotorezeptor-Zilien nehmen Licht wahr und wir können sehen. Angesichts dieser zentralen Rolle der Zilien in unserem Körper, können Fehlfunktionen ein breites Spektrum an menschlichen Krankheiten verursachen, einschließlich Netzhautdegeneration, polyzystischer Nierenerkrankung, Bardet-Biedl-Syndrom oder Herzerkrankungen.
Es ist daher entscheidend, die primären Zilien besser zu verstehen. Bis heute gibt es nur wenig mechanistisches Wissen darüber, wie die primären Zilien ihre Funktionen erfüllen. Bisher hindern uns fehlende Methoden daran, sie besser zu verstehen und ihre Struktur bei molekularer Auflösung zu erforschen.
Mit dieser Zielsetzung machten sich die Forschungsgruppenleiterin Gaia Pigino und ihr Team am MPI-CBG daran, die Struktur der primären Zilien zu erforschen. Sie begannen, eine Methode zu entwickeln, die es ihnen ermöglichen würde, die molekulare Struktur der primären Zilien in hoher Auflösung zu sehen. Die Herausforderung bestand darin, die Zilien von den Zellen zu trennen, ohne ihre vielen feinen Strukturdetails zu zerstören, und sie dann unter einem besonders leistungsfähigen Elektronenmikroskop zu beobachten.
Petra Kiesel, die Laborassistentin der Forschungsgruppe und diejenige, die die Methode entwickelte, erklärt: „Wir kombinierten eine Abwandlung einer bestehenden chemischen Methode mit einer mechanischen, um die Zilien aus Nierenzellen direkt auf dem Mikroskopie-Träger zu isolieren, um sie dann mit unserem bevorzugten Elektronenmikroskop sichtbar zu machen.“ Dazu verwendeten die Forscher eine Methode namens Kryo-Elektronentomographie (Kryo-EM), ein spezielles Verfahren, um gefrorene biologische Proben so abzubilden, dass vollständige 3D-Modelle ihrer Molekularstruktur erstellt werden können.
Mit dieser Methode konnten die Forscher nun primäre Zilien mit einer so hohen Auflösung beobachten, dass einzelne Proteine identifizierbar waren. Gonzalo Alvarez Viar, Doktorand in der Forschungsgruppe, berichtet: „Die Strukturen, die wir fanden, unterscheiden sich stark von denen, die wir von den beweglichen Zilien kennen. Ihr Zytoskelett ist weniger geordnet und hat eine weniger symmetrische Struktur. Von den beweglichen Zilien ist bekannt, dass sie eine neunfache Symmetrie haben, um sich fortzubewegen, das konnten wir bei den primären Zilien aber nicht beobachten.“
Aber nicht nur die Struktur bekannter Komponenten erweist sich als anders. Die primären Zilien überraschten auch mit einer Reihe anderer Besonderheiten, zum Beispiel mit dem Vorkommen von Aktinfilamenten. Aktin-Filamente kommen im Zytoplasma eukaryotischer Zellen vor und bilden einen Teil des Zytoskeletts. „Es war für uns eine große Überraschung, filamentöses Aktin in Zilien zu finden. Es wurde zwar gelegentlich durch andere Experimente angedeutet, aber nur wenige Leute glaubten wirklich daran, da es nie handfeste Beweise dafür gab“, sagt Gaia Pigino, die die Studie leitete.
Diese Ergebnisse, die eine Menge bisher unbekannter Fakten und überraschende Unterschiede zwischen den gut untersuchten beweglichen Zilien und den kaum erforschten primären Zilien aufzeigen, wurden nun in Nature Structural and Molecular Biology veröffentlicht. „Unsere Methode wird den Weg für viele tief greifende Untersuchungen der primären Zilien ebnen und es uns im Umkehrschluss ermöglichen, diese wichtigen Organellen bei Tier und Mensch, hinsichtlich Gesundheit und Krankheit besser zu verstehen“, so Gaia Pigino abschließend.
Wissenschaftliche Ansprechpartner:
Dr. Gaia Pigino
+49 (0) 351 210 2450
pigino@mpi-cbg.de
Originalpublikation:
Petra Kiesel, Gonzalo Alvarez Viar, Nikolai Tsoy, Riccardo Maraspini, Peter Gorilak, Vladimir Varga, Alf Honigmann, Gaia Pigino: “The molecular structure of mammalian primary cilia revealed by cryo-electron tomography”, Nat Struct Mol Biol, 28. September 2020. Doi: 10.1038/s41594-020-0507-4
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Mehr Prozess- und Produktinnovationen in Deutschland als im EU-Durchschnitt
Mehr als jedes 3. Unternehmen (36 %) in Deutschland hat zwischen 2018 und 2020 (aktuellste Zahlen für die EU-Länder) neue Produkte entwickelt, Neuerungen von Wettbewerbern imitiert oder eigene Produkte weiterentwickelt….

Nanofasern befreien Wasser von gefährlichen Farbstoffen
Farbstoffe, wie sie zum Beispiel in der Textilindustrie verwendet werden, sind ein großes Umweltproblem. An der TU Wien entwickelte man nun effiziente Filter dafür – mit Hilfe von Zellulose-Abfällen. Abfall…

Entscheidender Durchbruch für die Batterieproduktion
Energie speichern und nutzen mit innovativen Schwefelkathoden. HU-Forschungsteam entwickelt Grundlagen für nachhaltige Batterietechnologie. Elektromobilität und portable elektronische Geräte wie Laptop und Handy sind ohne die Verwendung von Lithium-Ionen-Batterien undenkbar. Das…





















