Neue Hoffnung für Schlaganfall-Patienten
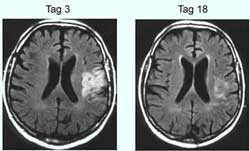
Bessere Heilung: Das Gehirn eines mit Erythropoietin behandelten Patienten, aufgenommen im Magnetresonanz-Tomographen 3 und 18 Tage nach einem Schlaganfall. Die geschädigten Regionen sind weiß zu sehen. Während sich Schlaganfall-Patienten in der Regel nur zögernd erholen, zeigen Patienten, die mit Erythropoietin behandelt wurden, wesentlich bessere Fortschritte. <br> <br>Fotos: Max-Planck-Institut für experimentelle Medizin <br>
Max-Planck-Forschern gelingt erste erfolgreiche neuroprotektive Behandlung von Schlaganfallpatienten mit Erythropoietin
Für Schlaganfall gibt es derzeit keine andere wirksame Behandlung als die Auflösung des Blutgerinnsels (die so genannte „Lyse“) mit dem Wirkstoff rTPA (rekombinanter Tissue Plasminogen Activator). Doch die Lysetherapie ist komplikationsreich und eignet sich nur für etwa fünf Prozent der Schlaganfall-Patienten. Ein Forscherteam um Prof. Hannelore Ehrenreich am Max-Planck-Institut für experimentelle Medizin in Göttingen hat jetzt einen neuen Ansatz für eine Schlaganfall-Therapie vorgestellt. Die neue Therapie setzt auf den Wirkstoff Erythropoietin (EPO) und soll das Nervengewebe selbst vor den Wirkungen eines Schlaganfalls schützen. Die erste maßgeschneiderte klinische Pilotstudie verlief sehr erfolgreich: EPO, rasch nach einem solchen Infarkt verabreicht, ist bestens verträglich und reduziert deutlich die neurologischen Ausfälle sowie die Größe des vom Infarkt geschädigten Hirngewebes (Molecular Medicine 8: 495-505, 2002). EPO kann bei Schlaganfall eingesetzt werden, wenn auch die Mitte Dezember 2002 startende zweite klinische Studie mit 500 Patienten erfolgreich verläuft.
Erythropoietin (EPO) ist seit vielen Jahren bekannt als ein Eiweißstoff, der in der Niere gebildet wird und maßgeblich die Blutbildung beeinflusst. Erythropoietin und sein Rezeptor sind im normalen erwachsenen Gehirn nur schwach nachweisbar, werden jedoch als Antwort auf Sauerstoffmangel (Hypoxie) und Stoffwechsel-Stress von Nervenzellen vermehrt gebildet. Dass Erythropoietin und seinem Rezeptor eine wesentliche Rolle bei der embryonalen Hirnentwicklung zukommt, wurde erst vor kurzem auch durch Untersuchungen der Göttinger Wissenschaftler deutlich. Das Erythropoietin-System im Gehirn kann als ontogenetisch frühes Schutzsystem betrachtet werden, das mit dem Fortschreiten der Hirnentwicklung vom Embryo zum Erwachsenen in einen weitgehenden Ruhezustand eintaucht, aus dem es erst dann reaktiviert wird, wenn Nervenzellen in Bedrängnis geraten und vor Schaden geschützt werden müssen. Es handelt sich somit um ein körpereigenes System zum Schutz der Nervenzellen vor Degeneration.
Im Tiermodell konnte bereits nachgewiesen werden, dass Erythropoietin zahlreiche therapeutische Wirkungen hat. Diese reichen vom Neurotrauma über entzündliche Erkrankungen bis hin zu Rückenmarksverletzungen, von Epilepsie bis Parkinson. In zahlreichen Tests zeigten nun die Göttinger Forscher, dass Erythropoietin beim Menschen antitoxisch wirkt, Nervenzellen vor dem Tod (Apoptose) schützt, zerstörerische Radikale im Blut abfängt und entzündungshemmend wirkt. Zudem fördert es Wachstum und Verzweigung von Nervenzellen sowie die Bildung und Verästelung von Blutgefäßen.
Von daher ist Erythropoietin ein interessanter Kandidat für neuroprotektive, also Nervengewebe erhaltende Therapien bei einer ganzen Reihe von Hirnerkrankungen. Dies um so mehr, da Erythropoietin in den vergangenen 15 Jahren bereits vielfältig in den Kliniken zum Einsatz gekommen ist, vor allem bei Blutarmut infolge von Nierenversagen, bei Tumoranämie oder bei der Gewinnung von Blutkonserven aus Eigenblut. Dabei hat es sich bei Millionen von Menschen als ausgesprochen gut verträglich und sicher erwiesen.
Was versteht man unter Neuroprotektion? Bei der Neuroprotektion versucht man, die Interaktionen zwischen Nervenzellen im Gehirn auf einem möglichst hohen Niveau zu halten und die Gehirnfunktionen selbst zu schützen. Bei Schlaganfall (cerebrale Ischämie) gab es in der Vergangenheit bereits zahlreiche neuroprotektive Therapieversuche mit verschiedenen Substanzen, jeweils in der Hoffnung, potentiell noch lebendes Hirngewebe in der so genannten Penumbra, also der Region im Gehirn, die die Kernzone des nicht mehr mit Blut versorgten Gewebes umgibt, vor dem Tod zu retten. Doch im Gegensatz zu den im Tierversuch erreichten Ergebnissen haben bisher sämtliche neuroprotektive Therapieansätze beim menschlichen Schlaganfall versagt.
Den Max-Planck-Wissenschaftlern ist nun mit dem Einsatz von Erythropoietin in einer klinischen Studie bei Patienten die erste erfolgreiche neuroprotektive Behandlung von Schlaganfall gelungen. Die „Göttinger EPO-Schlaganfall-Studie“, eine Pilotstudie vor der Zulassung für den klinischen Einsatz („proof-of-concept-Studie“), wurde in einem geradezu experimentellen Zuschnitt durchgeführt. Ziel der Forscher war es, bei der klinischen Studie am Patienten eine ähnlich hohe Aussagekraft wie bei Tierexperimenten zu erreichen. Denn viele Feld-Studien am Menschen haben den Nachteil, dass eine zu große Variabilität und Inhomogenität der eingeschlossenen Patientenpopulation die Auswertung sehr erschwert.
Deshalb hatten die Max-Planck-Forscher für ihre Studie sehr restriktiv definiert, welche Patienten in die Studie einbezogen werden sollen, auch wenn sich dadurch die zeitliche Dauer der Studie verlängert. So begann die Vorbereitung dieser Studie bereits 1997. 1998 wurde der erste und Ende 2001 der letzte Patient aufgenommen. Insbesondere zwei Kriterien dieser Studie sind bislang einzigartig für klinische Schlaganfall-Untersuchungen: (1) Es wurden nur Patienten eingeschlossen, die einen Schlaganfall im Gebiet der mittleren Hirnarterie erlitten hatten (Media-Ischämie). Das verbesserte die Vergleichbarkeit der klinischen und bildgebenden Befunde zwischen den verschiedenen Patienten. (2) Es wurden nur Patienten aufgenommen, bei denen in der Akutsituation mit Hilfe der diffusionsgewichteten Magnetresonanz-Tomographie zuvor ausgeschlossen werden konnte, dass andere oftmals schwer abzugrenzende Krankheitsbilder vorlagen, wie eine kurzfristige Durchblutungsstörung oder eine Lähmung nach einem Epilepsie-Anfall. Im Ergebnis wurden dann lediglich 53 von insgesamt 500 Patienten in die Studie eingeschlossen. Dieses strikte Aufnahmeverfahren war wichtig, damit die Studie eine möglichst hohe Aussagekraft erreicht.
Die EPO-Studie gliederte sich in zwei nacheinanderfolgende Teile, eine Sicherheitsstudie und eine Studie zum Nachweis der Wirksamkeit von EPO. In der Sicherheitsstudie behandelte man 13 Patienten nach der Diagnose eines akuten ischämischen Schlaganfalls intravenös einmal täglich mit hochdosiertem rekombinanten menschlichen Erythropoietin über drei Tage. Daran schloss sich eine so genannte „doppelblinde“ Wirksamkeitsstudie mit 40 Patienten an. Doppelblind heißt, dass weder die Patienten noch die behandelnden Ärzte wussten, wer in diesen drei Tagen mit Erythropoietin und wer mit einem Placebo (Kochsalzlösung) behandelt wurde. Bei diesen Patienten wurden dann die Entwicklung ihrer neurologischen Symptome, der Infarktgröße sowie das Niveau von Schadensmarkern im Blut gemessen.
Die Sicherheitsstudie ergab keinerlei unerwünschte Nebenwirkungen. Bei den Patienten stieg die Konzentration von Erythropoietin innerhalb der Hirnflüssigkeit auf das 60-fache über normal (Konzentration nicht behandelter Schlaganfallpatienten) an. Damit gelang den Wissenschaftlern der Nachweis, dass intravenös verabreichtes Erythropoietin über die Blut-Hirn-Schranke ins Gehirn gelangen kann. Dieser Fakt war für den weiteren Verlauf der Studie sehr wichtig, da man bei einem Molekulargewicht von ca. 34 000 Dalton nicht ohne weiteres mit einem Übertritt nennenswerter Mengen an Erythropoietin über die Blut-Hirn-Schranke rechnen konnte. Auf Grund ihrer bisherigen Testergebnisse vermuten die Göttinger Forscher, dass für Erythropoietin an der Blut-Hirn-Schranke spezielle Aufnahmemechanismen bestehen, die sogar bei gesunden Menschen einen Transfer ins Gehirn erlauben.
In der Wirksamkeitsstudie zeigt sich nach Offenlegung, welche Patienten mit Erythropoietin und welche mit einem Placebo behandelt wurden, dass man beide Gruppen im Hinblick auf alle wesentlichen Patientencharakteristika und vor allem auch hinsichtlich der Schwere des Schlaganfalls optimal vergleichen konnte. Die Patienten erhielten Erythropoietin innerhalb einer mittleren Zeit von fünf Stunden nach Einsetzen der Schlaganfall- Symptome (2:40-5:55 Std:Min). In der Analyse zeigte sich eine signifikante Überlegenheit der mit Erythropoietin behandelten Patienten im Vergleich zur Kontrollgruppe: Dazu gehörten bessere klinische Symptome, deutlich kleinere durchschnittliche Größe der Gehirnläsion und ein geringerer Anstieg eines zirkulierenden Schadensmarkers im Vergleich zu den Placebo-Patienten sowie eine viel schnellere Rückkehr dieses Blutspiegels auf Kontrollniveau.
Mit ihrem „experimentellen Design“, das heißt einer relativ homogenen Patienten-Gruppe dank strenger Auswahlkriterien, hat die Göttinger Studie – trotz der relativ geringen Zahl an Patienten – bereits wichtige Ergebnisse geliefert. Sie zeigt, dass eine Erythropoietin-Behandlung eine deutliche Verbesserung bei den Patienten bewirkt. Prof. Hannelore Ehrenreich sagt dazu: „Die Tatsache, dass mit einer rein neuroprotektiven Studie ein so positiver Effekt bei Schlaganfall erzielt werden konnte, ist überaus ermutigend. Natürlich soll die Erythropoietin-Therapie die Lyse-Therapie nicht ersetzen. Eine erfolgreiche Schlaganfalltherapie der Zukunft wird eine kombinierte Therapie sein. Neben spezifischen Wirkstoffen gehören dazu auch unterstützende Maßnahmen. Doch mit unseren Ergebnissen besteht jetzt erstmals ein hoffnungsvoller Grundstock für den neuroprotektiven Teil einer künftigen Kombinationsstrategie bei Schlaganfall.“ Erythropoietin ist also keine Konkurrenz für die Lysetherapie mit rTPA oder verwandten Substanzen, sondern dazu komplementär. Doch bei jenen Patienten, für die eine Lysetherapie nicht geeignet ist, und das sind über 95 Prozent aller Schlaganfälle, stellt Erythropoietin eine wichtige Alternative dar. Und Erythropoietin hat noch einen Vorteil: Bei einem Notfall könnte es – im Gegensatz zur Lyse-Therapie – sofort oder bereits beim Transport in die Klinik eingesetzt werden.
Um die Daten der ersten Göttinger Pilotstudie zu erhärten, startet im Dezember 2002 in Deutschland die weltweit erste, auf verschiedene Kliniken verteilte Studie „Erythropoietin bei Schlaganfall“. Auch diese Studie wird von Frau Prof. Hannelore Ehrenreich aus dem Max-Planck-Institut für experimentelle Medizin geleitet. Sollte diese Studie ebenfalls erfolgreich verlaufen, könnte Erythropoietin bereits in zwei bis drei Jahren regulärer Bestandteil einer neuen Schlaganfall-Therapie sein.
Weitere Informationen erhalten Sie von:
Prof. Dr. Dr. Hannelore Ehrenreich
Max-Planck-Institut für experimentelle Medizin
Hermann-Rein-Str. 3, 37075 Göttingen
Tel.: (05 51) 38 99 – 6 28
Fax: (05 51) 38 99 – 6 15
E-Mail: ehrenreich@em.mpg.de
Media Contact
Alle Nachrichten aus der Kategorie: Agrar- Forstwissenschaften
Weltweite, wissenschaftliche Einrichtungen forschen intensiv für eine zukunftsfähige Land- und Forstwirtschaft.
Der innovations-report bietet Ihnen hierzu interessante Berichte und Artikel, unter anderem zu den Themen: Bioenergie, Treibhausgasreduktion, Renaturierung und Landnutzungswandel, Tropenwälder, Klimaschäden, Waldsterben, Ernährungssicherung, neue Züchtungstechnologien und Anbausysteme, Bioökonomie, Wasserressourcen und Wasserwiederverwendung, Artenvielfalt, Pflanzenschutz, Herbizide und Pflanzenschädlinge, digitale Land- und Forstwirtschaft, Gentechnik, tiergerechte Haltungssysteme und ressourcenschonende Landwirtschaft.
Neueste Beiträge

Ideen für die Zukunft
TU Berlin präsentiert sich vom 22. bis 26. April 2024 mit neun Projekten auf der Hannover Messe 2024. Die HANNOVER MESSE gilt als die Weltleitmesse der Industrie. Ihr diesjähriger Schwerpunkt…

Peptide auf interstellarem Eis
Dass einfache Peptide auf kosmischen Staubkörnern entstehen können, wurde vom Forschungsteam um Dr. Serge Krasnokutski vom Astrophysikalischen Labor des Max-Planck-Instituts für Astronomie an der Universität Jena bereits gezeigt. Bisher ging…

Wasserstoff-Produktion in der heimischen Garage
Forschungsteam der Frankfurt UAS entwickelt Prototyp für Privathaushalte: Förderzusage vom Land Hessen für 2. Projektphase. Wasserstoff als Energieträger der Zukunft ist nicht frei verfügbar, sondern muss aufwendig hergestellt werden. Das…





















