Kollagen: Ein Protein sorgt für Spannung
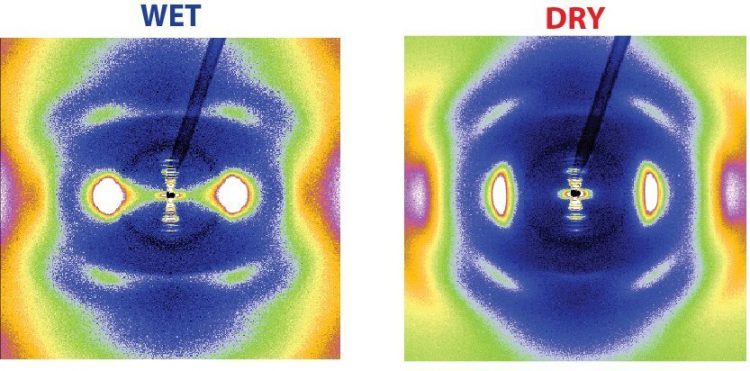
Röntgenblick auf Kollagen: Aus den Mustern der zweidimensionalen Röntgenbeugung lassen sich Informationen über Änderungen in der molekularen und nanoskopischen Kollagenstruktur gewinnen, wenn das Protein trocknet. Die Struktur des Kollagens ist für die Krafterzeugung ausschlaggebend. © Nature Communications 2015 / MPI für Kolloid- und Grenzflächenforschung
Die Körper von Menschen und Tieren verdanken ihre Festigkeit vor allem einem faserbildenden Protein, dem Kollagen. Knochen, Sehnen, Bänder oder die Haut enthalten es in großen Mengen. Ein Stoff, der mit Festigkeit wenig assoziiert wird, nämlich Wasser, entpuppt sich nun als integraler Bestandteil des Kollagens, wie Forscher des Max-Planck-Instituts für Kolloid- und Grenzflächenforschung in Potsdam-Golm, in Zusammenarbeit mit Forschern von dem Massachusetts Institute of Technology in Cambridge (USA), zeigten.
Das Team um Admir Masic und Luca Bertinetti entfernte Wasser aus Kollagenfasern, was sich dramatisch auswirkte. Die Fasern zogen sich zusammen und erreichten dadurch eine 300-Mal stärkere Spannung, als Muskeln sie auszuüben vermögen. Dieses Wissen könnte für neuartige, aktive Materialien genutzt werden. Die Ergebnisse deuten aber auch darauf hin, dass Kollagen in Lebewesen mehr Funktionen übernehmen kann, als bisher angenommen. Demnach spielt es nicht nur eine passive Rolle, nämlich als eine Art Stützapparat für den Organismus. Es kann auch eine aktive Rolle spielen, etwa bei der Bildung von Knochen.
Einem Gebäude ähnlich ist Kollagen hierarchisch aus einer komplexen Anordnung von Einzelbausteinen aufgebaut. Der Basisbaustein ist das Kollagenmolekül. Es erinnert an ein Seil: Drei kettenförmige Proteine winden sich umeinander und bilden so eine Dreifachhelix. Viele dieser „Seile“ wiederum verbinden sich zu dickeren „Tauen“, so genannten Kollagenfibrillen. Mit rund 100–500 Nanometern Dicke sind die Fibrillen allerdings 100 000 Mal dünner als wirkliche Taue. In den Fibrillen liegen benachbarte Kollagenmoleküle nicht bündig aneinander, sondern versetzt, sodass eine gestaffelte Anordnung entsteht. Das führt entlang der Fibrille zu einander abwechselnden dichteren und weniger dichten Zonen. Viele Fibrillen wiederum bündeln sich zu Kollagenfasern.
Welche Eigenschaften Kollagen aufweist und vor allem wie das in ihm enthaltene Wasser seine Funktion beeinflusst, haben nun Wissenschaftler des Max-Planck-Instituts für Kolloid- und Grenzflächenflächenforschung in Potsdam-Golm untersucht. Das Besondere an der Studie des Golmer Teams: Es kombinierte erstmals verschiedene Messmethoden, um Kollagen auf verschiedenen Ebenen seines hierarchischen Aufbaus zu untersuchen, und kontrollierte dabei in einer Feuchtigkeitskammer den Wassergehalt des Naturstoffes. Eine spezielle Vorrichtung in der Kammer maß die Spannungskräfte, die auf das aus Rattenschwänzen gewonnene Kollagen wirkten.
Wasser ist ein wesentlicher Bestandteil des Kollagens
Die Messergebnisse brachten die Golmer Forscher in Einklang mit Computermodellen von Kollagenmolekülen, entwickelt von Wissenschaftlern des Massachusetts Institute of Technology in Cambridge (USA). So kam es der Rolle des Wassers im Kollagen bis ins Detail auf die Spur.
„Wasser ist ein integraler Bestandteil von Kollagen“, sagt Admir Masic. Im natürlichen Zustand macht es rund 60 Gewichtsprozent des Kollagens aus. Wassermoleküle fügten sich so nahtlos in das Kollagen ein, dass sie dessen Helixform folgen, berichtet Masic. Das fand das Team durch Untersuchungen mit Röntgenbeugung heraus. Mit dieser Methode lassen sich Details der Helixstruktur erforschen, etwa die Neigung der Windungen oder der Durchmesser der Helix.
Bei dem hohen Wassergehalt verwundert es nicht, dass sich der Entzug von Wasser dramatisch auswirkt. Nimmt die relative Luftfeuchtigkeit von 95 auf 5 Prozent ab, trocknet man das Kollagen also praktisch aus, ziehen sich Kollagenmoleküle um 1,3 Prozent und die entsprechenden Fibrillen um 2,5 Prozent zusammen. Trotz dieser relativ geringen Längenänderung entsteht dabei ein Zug von 100 Megapascal, was über 300 Mal mehr ist, als ein Muskel an Zug erzeugt.
Dichte Regionen der Fibrillen dehnen sich, dünne ziehen sich zusammen
Auch dem Mechanismus dieser Kontraktion kamen die Forscher um Masic und Bertinetti auf die Spur. Dafür nutzten sie die Raman-Spektroskopie, mit der sie die Konformation der Molekülketten des Kollagens untersuchten. Mit „Konformation“ ist die Lage gemeint, die Atome zueinander einnehmen. Dabei zeigte sich, dass die Verkürzung durch Änderungen der Konformation hervorgerufen wird. Vorstellen kann man sich das mit einem zunächst gestreckten Seil, das in Wellen geworfen wird, sodass die Enden näher zusammenrücken. Ein interessantes Detail des Mechanismus: Die dichten Regionen der Fibrillen dehnten sich, während sich die dünneren zusammenzogen. Unterm Strich ergab sich so eine Kontraktion.
„Mit diesem Wissen könnten Materialien entwickelt werden, die sich bei Entzug von Wasser gegensätzlich verhalten“, sagt Luca Bertinetti. Er denkt dabei zum Beispiel an aufeinander geklebte Schichten von zwei Materialien, von denen sich das eine bei Entzug von Wasser dehnt und das andere zusammenzieht. Die Doppelschicht würde sich dann biegen. Die Messergebnisse des Teams zeigen, dass solche Werkstoffe große Kräfte ausüben könnten. Auch für die Produktion von Leder oder Pergamentpapier könnten die neuen Erkenntnisse aufschlussreich sein.
Potenzielle und noch unerforschte aktive Funktion von Kollagenfibrillen
Doch nicht nur für die Technik sind die Ergebnisse aus Golm interessant. Zwar kommt ein so starker Wasserentzug wie in der Feuchtigkeitskammer der Forscher unter physiologischen Bedingungen im Körper eines Lebewesens nicht vor. Doch Masic’s und Bertinetti’s Team hat festgestellt, dass der Wasserentzug auch unter biologischen Verhältnissen groß genug sein kann, damit das Kollagen eine ebenso große Zugspannung aufbaut wie ein Muskel.
Daher könnte das Biomolekül statt einer passiven, nämlich der mechanischen Stabilisierung des Körpers, auch eine aktive Rolle spielen. „Während des Aufbaus von Knochen könnte dem darin enthaltenen Kollagen Wasser entzogen werden, so dass es sich zusammenzieht“, sagt der Direktor des Institutes, Peter Fratzl, der diese Forschungsarbeit koordiniert hat. Dadurch werde der Knochen zusammengedrückt, was verhindere, dass das eigentlich spröde Material durch Zugspannungen auseinandergerissen werden kann. Eine ähnliche Rolle spiele der Stahl im Stahlbeton, vergleicht Fratzl.
Unterstützt wird diese Annahme dadurch, dass der Abstand zwischen den dichten Zonen der Kollagenfibrillen in Knochen der gleiche ist wie in getrocknetem Kollagen und dass die Zugfestigkeit von Knochen in etwa der Spannung von getrocknetem Kollagen entspricht.
In nächster Zukunft wollen die Golmer Forscher die mögliche physiologische Rolle der Kollagenkontraktion in verschiedenen Geweben erforschen.
Ansprechpartner
Dr. Admir Mašić
Max-Planck-Institut für Kolloid- und Grenzflächenforschung, Potsdam-Golm
Telefon: +49 331 567-9419
E-Mail: admir.masic@mpikg.mpg.de
Prof. Dr. Peter Fratzl
Max-Planck-Institut für Kolloid- und Grenzflächenforschung, Potsdam-Golm
Telefon: +49 331 567-9401
Fax: +49 331 567-9402
E-Mail: gabbe@mpikg.mpg.de
Originalpublikation
Admir Masic, Luca Bertinetti, Roman Schuetz, Shu-Wei Chang, Hartmut Metzger, Markus J. Buehler & Peter Fratzl
Osmotic pressure induced tensile forces in tendon collagen
Nature Communications; 22 January 2015; DOI: 10.1038/ncomms6942
Media Contact
Alle Nachrichten aus der Kategorie: Materialwissenschaften
Die Materialwissenschaft bezeichnet eine Wissenschaft, die sich mit der Erforschung – d. h. der Entwicklung, der Herstellung und Verarbeitung – von Materialien und Werkstoffen beschäftigt. Biologische oder medizinische Facetten gewinnen in der modernen Ausrichtung zunehmend an Gewicht.
Der innovations report bietet Ihnen hierzu interessante Artikel über die Materialentwicklung und deren Anwendungen, sowie über die Struktur und Eigenschaften neuer Werkstoffe.
Neueste Beiträge

Bakterien für klimaneutrale Chemikalien der Zukunft
Forschende an der ETH Zürich haben Bakterien im Labor so herangezüchtet, dass sie Methanol effizient verwerten können. Jetzt lässt sich der Stoffwechsel dieser Bakterien anzapfen, um wertvolle Produkte herzustellen, die…

Batterien: Heute die Materialien von morgen modellieren
Welche Faktoren bestimmen, wie schnell sich eine Batterie laden lässt? Dieser und weiteren Fragen gehen Forschende am Karlsruher Institut für Technologie (KIT) mit computergestützten Simulationen nach. Mikrostrukturmodelle tragen dazu bei,…

Porosität von Sedimentgestein mit Neutronen untersucht
Forschung am FRM II zu geologischen Lagerstätten. Dauerhafte unterirdische Lagerung von CO2 Poren so klein wie Bakterien Porenmessung mit Neutronen auf den Nanometer genau Ob Sedimentgesteine fossile Kohlenwasserstoffe speichern können…





















