Getarntes Virus für die Gentherapie von Krebs

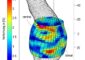
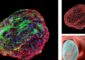
Das Adenovirus (links) tarnt sich dank Schutzhülle (rechts) vor der Immunabwehr. UZH
Viren besitzen eigenes genetisches Material und können menschliche Zellen sehr gezielt infizieren. Dank der eingeschleusten Gene vermehren sich die Viren dann auf Kosten ihrer Wirtszelle. Diese Eigenschaften machen sie zu interessanten «Genfähren», um Erbkrankheiten oder Krebs zu behandeln.
Von den unzähligen Viren hat insbesondere das humane Adenovirus 5, das normalerweise Erkältungen verursacht, gewichtige Vorteile: Sein Genom lässt sich vollständig durch ein synthetisches ersetzen, das nur noch «nützliche» Erbfaktoren enthält. So kann sich das Virus nicht mehr vermehren und eine Krankheit verursachen. Sein Genom ist zudem sehr gross und lagert sich nicht in menschliche Chromosomen ein.
Tumorzellen infizieren dank spezifischen Adaptermolekülen
Doch bisher war der Einsatz von Adenoviren gegen Krebserkrankungen sehr eingeschränkt. Ihnen fehlt die Fähigkeit, Krebszellen zu infizieren und die genetischen Baupläne für die Wirkstoffe einzuschleusen, um die kranken Zellen zu bekämpfen. Zudem werden Adenoviren vom Immunsystem effizient eliminiert und von der Leber sehr schnell aus der Blutbahn entfernt.
Forschenden unter der Leitung von Andreas Plückthun, Professor am Biochemischen Institut der Universität Zürich, ist es nun gelungen, die Viren so umzubauen, dass sie Tumorzellen erfolgreich erkennen und befallen. «Dazu benutzten wir Moleküle, die als Adapter zwischen dem Virus und der Krebszelle funktionieren», erklärt Markus Schmid, Erstautor der Studie.
Die Adapter, die sich fest an die Virushülle klammern, binden – je nach Version – verschiedene Oberflächenmoleküle auf der Tumorzelle. Getestet haben die Wissenschaftler Adaptermoleküle für mehrere Rezeptoren wie HER2 und EGFR, die auf diversen Arten von Krebszellen vorhanden sind. Nur Viren, die mit diesen Adaptern ausgestattet sind, konnten die Tumorzellen infizieren.
Neuartige Proteinhülle tarnt und schützt vor Immunsystem
Im nächsten Schritt haben die Forschenden das Virus unter einer neuartigen Proteinhülle versteckt, mit der sich die Genfähre tarnt und vor den Angriffen des Immunsystems schützt. Als Basis für die Schutzhülle verwendeten sie einen bereits bestehenden Antikörper gegen das Virus und bauten diesen um. Im Rahmen der interdisziplinären Zusammenarbeit der beteiligten Forschungsgruppen konnte der genaue Aufbau dieser Proteinhülle in nahezu atomarem Detail beschrieben werden.
Die Hülle schützt das umgebaute Virus nicht nur vor den Abwehrzellen, sondern verhindert gleichzeitig seine Neutralisation durch die Leber. Diese fischt unveränderte Adenoviren normalerweise sehr rasch aus der Blutbahn, was therapeutische Anwendungen meist verunmöglicht. Das mithilfe von Protein-Engineering aufwändig umgebaute Virus funktioniert: Dank Hülle und Adapter erkennen und befallen die viralen Genfähren in Laborexperimenten und Tierversuchen die Tumorzellen sehr effizient.
Wertvolles Instrument für Gentherapie aggressiver Krebsarten
Mithilfe dieser getarnten Genfähren wollen die UZH-Wissenschaftler in Zukunft neuartige Therapien für verschiedene Tumorerkrankungen entwickeln. Die vielen Vorteile des Adenovirus dürften helfen, eines der grossen Probleme der Krebsmedizin anzugehen: die Entwicklung von Resistenzen gegen Medikamente. Biochemiker Andreas Plückthun ist optimistisch: «Mit dieser Genfähre eröffnen sich vielversprechende Perspektiven, um aggressive Krebsarten zukünftig wirksamer behandeln zu können, da sich gleichzeitig eine ganze Reihe von Medikamenten direkt im Tumor produzieren lassen».
Literatur:
Markus Schmid, Patrick Ernst, Annemarie Honegger, Maarit Suomalainen, Martina Zimmermann, Lukas Braun, Sarah Stauffer, Cristian Thom, Birgit Dreier, Matthias Eibauer, Anja Kipar, Viola Vogel, Urs F. Greber, Ohad Medalia, and Andreas Plückthun, Adenoviral vector with shield and adapter increases tumor specificity and escapes liver and immune control. Nature Communications. January 31, 2018. DOI: 10.1038/s41467-017-02707-6
Schweizerischer Nationalfonds unterstützt interdisziplinäre Forschung
Das Team um Andreas Plückthun vom Biochemischen Institut der Universität Zürich arbeitete zusammen mit weiteren Forschenden der UZH, der ETH Zürich und dem Tierspital Zürich. Die Arbeit wurde ermöglicht dank der langjährigen Unterstützung durch den Schweizerischen Nationalfonds, insbesondere durch das Programm «Sinergia». Dieses fördert die Zusammenarbeit von zwei bis vier Forschungsgruppen, die interdisziplinär und mit Aussicht auf bahnbrechende Erkenntnisse forschen.
Kontakt:
Prof. Dr. Andreas Plückthun
Biochemisches Institut
Universität Zürich
Tel. +41 44 635 55 70
E-Mail: plueckthun@bioc.uzh.ch
http://www.media.uzh.ch/de/medienmitteilungen//2018/Adenovirus-Gentherapie.html
Media Contact
Alle Nachrichten aus der Kategorie: Interdisziplinäre Forschung
Aktuelle Meldungen und Entwicklungen aus fächer- und disziplinenübergreifender Forschung.
Der innovations-report bietet Ihnen hierzu interessante Berichte und Artikel, unter anderem zu den Teilbereichen: Mikrosystemforschung, Emotionsforschung, Zukunftsforschung und Stratosphärenforschung.
Neueste Beiträge

Anlagenkonzepte für die Fertigung von Bipolarplatten, MEAs und Drucktanks
Grüner Wasserstoff zählt zu den Energieträgern der Zukunft. Um ihn in großen Mengen zu erzeugen, zu speichern und wieder in elektrische Energie zu wandeln, bedarf es effizienter und skalierbarer Fertigungsprozesse…

Ausfallsichere Dehnungssensoren ohne Stromverbrauch
Um die Sicherheit von Brücken, Kränen, Pipelines, Windrädern und vielem mehr zu überwachen, werden Dehnungssensoren benötigt. Eine grundlegend neue Technologie dafür haben Wissenschaftlerinnen und Wissenschaftler aus Bochum und Paderborn entwickelt….

Dauerlastfähige Wechselrichter
… ermöglichen deutliche Leistungssteigerung elektrischer Antriebe. Überhitzende Komponenten limitieren die Leistungsfähigkeit von Antriebssträngen bei Elektrofahrzeugen erheblich. Wechselrichtern fällt dabei eine große thermische Last zu, weshalb sie unter hohem Energieaufwand aktiv…