Zielgenau gegen Autoimmunkrankheiten und chronische Entzündungen
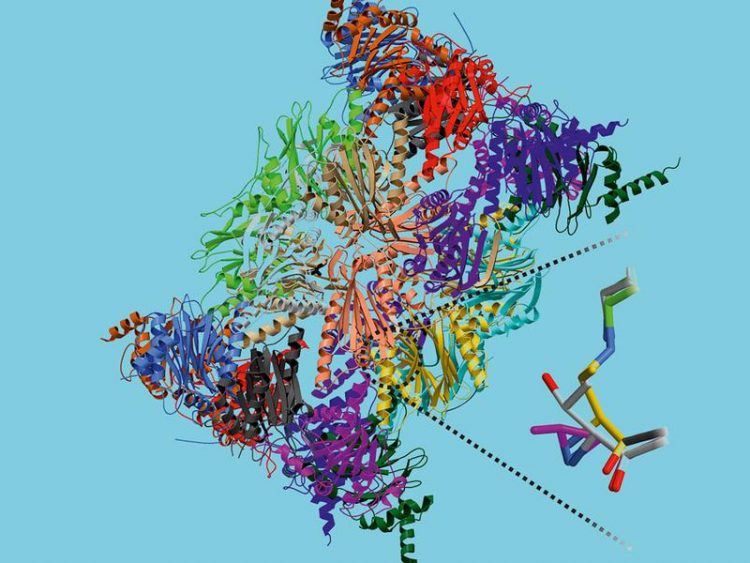
Die Kristallstruktur des Immunoproteasoms. Rechts ein Schema des durch den Inhibitor zerstörten aktiven Zentrums Bild: Lehrstuhl für Biochemie / TUM
Eine Schlüsselrolle spielt dabei das Immunoproteasom, das dem Abwehrsystem Informationen über die Vorgänge in der Zelle liefert. Chemiker der Technischen Universität München (TUM) haben nun einen Weg entdeckt, dessen Funktion mithilfe eines neuartigen Mechanismus zu hemmen und legen damit die Grundlage für die mögliche Optimierung bestehender Wirkstoffe.
Das Immunsystem fungiert als Polizei des Körpers und schützt uns vor Eindringlingen wie Bakterien und Viren. Um zu erfahren, was in der Zelle vor sich geht, benötigt es aber Informationen über den Fremdkörper. Diese Aufgabe übernimmt das sogenannte Immunoproteasom. Es handelt sich dabei um einen zylinderförmigen Proteinkomplex, der Eiweißstrukturen des Eindringlings in Bruchstücke zerlegt und diese dem Abwehrsystem zur Verfügung stellt.
„Bei Autoimmunerkrankungen wie Rheuma, Diabetes Typ I und Multipler Sklerose oder schweren Entzündungen ist oftmals eine deutlich erhöhte Konzentration des Immunoproteasoms in der Zelle messbar“, erklärt Professor Michael Groll vom Lehrstuhl für Biochemie der TUM. „Eine Inaktivierung dieser Abbaumaschinerie unterdrückt die Neubildung von Immunbotenstoffen, was wiederum eine übermäßige Immunreaktion verhindert.“
Feine, aber wesentliche Unterschiede
Bereits seit Längerem sind Wissenschaftler auf der Suche nach neuen Wirkstoffen, die das Immunoproteasom gezielt hemmen, ohne das ebenfalls in der Zelle vorkommende, sogenannte konstitutive Proteasom zu beeinträchtigen. Dieses baut gezielt fehlerhafte oder nicht mehr benötigte Eiweiße ab und übernimmt damit das zelluläre Recycling. Werden sowohl das konstitutive Proteasom als auch das Immunoproteasom gehemmt, führt dies zum Tod der Zelle.
Eine Voraussetzung für das Design eines spezifischen Wirkstoffs schuf die Forschergruppe um Groll Anfang 2012: Sie entschlüsselte die Kristallstruktur des Immunoproteasoms. So war es möglich, die feinen, aber wesentlichen Unterschiede zwischen den nahezu identisch aufgebauten Strukturen zu erkennen.
Besonderer Wirkmechanismus
Der potenzielle Wirkstoff, den die Wissenschaftler nun entwickelten, basiert auf dem Epoxyketon ONX 0914, einem Immunoproteasom-Hemmer, der bereits klinisch getestet wurde. Die Forscher ersetzten das Epoxyketon durch eine Sulfonylfluorid-Gruppe und veränderten deren Positionierung am Inhibitor. Als Ergebnis erhielten sie eine neue Verbindung, die speziell das Immunoproteasom hemmt und auf das konstitutive Proteasom kaum Einfluss hat.
Die Besonderheit des entdeckten Mechanismus erklärt Erstautor Christian Dubiella: „Normalerweise verstopfen Inhibitoren das aktive Zentrum des Enzyms und legen somit dessen Funktion lahm. Die von uns synthetisierte Substanz jedoch bindet an ihr Ziel, veranlasst das aktive Zentrum, sich selbst zu zerstören, und spaltet sich nach verrichteter Arbeit wieder ab.“ Vor allem Einblicke in den atomaren Mechanismus, welcher mittels Röntgenstrukturanalyse aufgeklärt wurde, ermöglicht die maßgeschneiderte Entwicklung von neuen Immunoproteasom-Inhibitoren. Damit könnte der Weg für eine zukünftige Generation an Wirkstoffen offen stehen.
Die Forschung wurde in Zusammenarbeit mit den Arbeitsgruppen um Prof. Stephan Sieber vom Lehrstuhl für Organische Chemie II, Prof. Achim Krüger vom Institut für Experimentelle Onkologie und Therapieforschung der TUM sowie Prof. Robert Liskamp von der Universität Glasgow durchgeführt. Die Arbeiten wurden mit Mitteln der Deutschen Forschungsgemeinschaft (SFB 1035/A2 & DFG GR 1861/10-1) sowie des Exzellenzclusters Center for Integrated Protein Science Munich (CIPSM) gefördert. Die röntgenkristallographischen Messungen wurden an der PXI-Beamline des Paul Scherrer Instituts in Villigen (Schweiz) durchgeführt.
Publikation:
Selective Inhibition of the Immunoproteasome by Ligand-Induced Crosslinking of the Active Site, Christian Dubiella, Haissi Cui, Malte Gersch, Arwin J. Brouwer,Stephan A. Sieber, Achim Krüger, Rob M. J. Liskamp, Michael Groll, Angewandte Chemie, Early view, 22. September 2014
DOI: 10.1002/ange.201406964
http://onlinelibrary.wiley.com/doi/10.1002/ange.201406964/abstract
Kontakt:
Prof. Dr. Michael Groll
Technische Universität München
Lehrstuhl für Biochemie
Tel.: +49 89 289 13361
E-Mail: michael.groll@tum.de
Media Contact
Weitere Informationen:
http://www.tum.deAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Merkmale des Untergrunds unter dem Thwaites-Gletscher enthüllt
Ein Forschungsteam hat felsige Berge und glattes Terrain unter dem Thwaites-Gletscher in der Westantarktis entdeckt – dem breiteste Gletscher der Erde, der halb so groß wie Deutschland und über 1000…

Wasserabweisende Fasern ohne PFAS
Endlich umweltfreundlich… Regenjacken, Badehosen oder Polsterstoffe: Textilien mit wasserabweisenden Eigenschaften benötigen eine chemische Imprägnierung. Fluor-haltige PFAS-Chemikalien sind zwar wirkungsvoll, schaden aber der Gesundheit und reichern sich in der Umwelt an….

Das massereichste stellare schwarze Loch unserer Galaxie entdeckt
Astronominnen und Astronomen haben das massereichste stellare schwarze Loch identifiziert, das bisher in der Milchstraßengalaxie entdeckt wurde. Entdeckt wurde das schwarze Loch in den Daten der Gaia-Mission der Europäischen Weltraumorganisation,…