Warum Champignons leicht braun werden
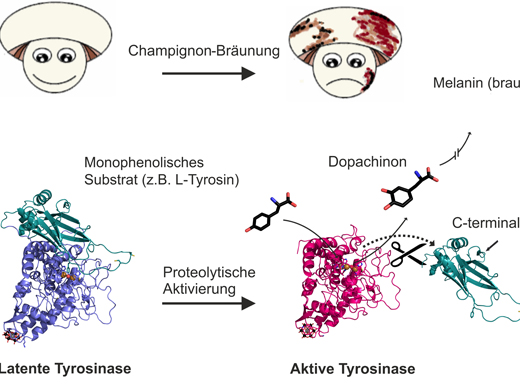
Schematische Darstellung der zeitlichen bzw. durch mechanischen Zellschaden induzierten enzymkatalysierten Bräunungsreaktion. A. Rompel/Universität Wien
Das Verständnis der Wirkungsweise des Pigmentierung-Enzyms Tyrosinase ist sowohl von medizinischem, als auch technologischem Interesse. Das Kupfer enthaltende Enzym gilt bei Tieren und Menschen als unentbehrlich für den Schutz vor UV-Strahlung und liefert zugleich auch Informationen zur Verhinderung des Verderbs von Lebensmitteln. Champignons sind dabei aufgrund ihrer niedrigen Kosten und der guten Verfügbarkeit eine wertvolle Quelle für die WissenschafterInnen. Vor allem wegen ihres hohen Enzymgehaltes werden die Pilze für Untersuchungen an der Tyrosinase geschätzt. Die Champignons dienen daher auch als Modellorganismus zur Untersuchung von Bräunungsreaktionen.
Bildung in inaktiver Vorstufe
Seit 2012 ist bekannt, dass sechs verschiedene Tyrosinasen (PPO1 bis 6) im Champignon existieren, von denen zwei in größeren Mengen vorkommen (PPO3 und PPO4). Das für die Bräunungsreaktion verantwortliche Enzym wird dabei in sogenannten Eukaryoten (Lebewesen, die einen Zellkern besitzen) in einer inaktiven Vorstufe des Entwicklungsprozesses gebildet. Diese Vorstufe wird dann durch eine Spaltung aktiviert. Dabei wird der das aktive Zentrum abdeckende Teil des Enzyms entfernt und die Substrate (Tyrosin und andere Monophenole) können umgesetzt werden.
Neuer Isolierungsweg und eine außergewöhnliche Reagenz führten zum Erfolg
Keiner der bis dahin in der Literatur bekannten Isolierungswege konnte für PPO4 erfolgreich angewendet werden. Im Institut für Biophysikalische Chemie wurde nun eine Methode entwickelt, die es erstmals erlaubt, die latente Tyrosinase aus deren natürlicher Quelle zu isolieren. Die Enzym-Charakterisierung fand in enger Zusammenarbeit mit dem Massenspektrometriezentrum der Universität Wien der Fakultät für Chemie unter der Leitung von Andreas Rizzi statt. Nachdem genügend große Mengen von reinem PPO4 extrahiert werden konnten, gelang es den WissenschafterInnen, Kristallisationsbedingungen zu finden und zu optimieren, unter denen das Protein Einkristalle bildet. Dieses gelang nur unter dem Einsatz eines relativ außergewöhnlichen Co-Kristallisation Reagenz, einem Polyoxometallat des Anderson-Typs.
Wesentlich für Medizin und Biotechnologie
Der Dissertant Stephan Mauracher hat das Projekt im Rahmen des Initiativkollegs „Functional Molecules“ der Universität Wien bearbeitet. „Es ist gelungen, das Enzym in ausreichender Menge zu reinigen und zu charakterisieren. Ulrich Kortz von der Jacobs University Bremen hat das Polyoxometallat synthetisiert und als Additiv für die Proteinkristallisation vorgeschlagen. Das Forschungsvorhaben wurde sodann als FWF Einzelprojekt weiter geführt. So gelang die Kristallisation und die drei-dimensionale Strukturlösung von PPO4“, so Rompel abschließend.
Publikation in Phytochemistry:
S. G. Mauracher, C. Molitor, C. Michael, M. Kragl, A. Rizzi and A. Rompel „High level protein-purification allows the unambiguous polypeptide determination of latent isoform PPO4 of mushroom tyrosinase.“ Phytochemistry 99 (2014) 14–25.
Publikation in Acta Crystallographica Section F – Structural Biology and Crystallization Communication:
S. G. Mauracher, C. Molitor, R. Al-Oweini, U. Kortz and A. Rompel „Crystallization and preliminary X-ray crystallographic analysis of latent isoform PPO4 mushroom (Agaricus bisporus) tyrosinase“ Acta Cryst. F70 (2014) 263-266.
Publikation in Acta Crystallographica Section D – Biological Crystallography:
S. G. Mauracher, C. Molitor, R. Al-Oweini, U. Kortz and A Rompel: Latent and active abPPO4 mushroom tyrosinase cocrystallized with hexatungstotellurate(VI) in a single crystal.
Wissenschaftlicher Kontakt
Univ.-Prof. Dr. Annette Rompel
Institut für Biophysikalische Chemie
Fakultät für Chemie
Universität Wien
T +43-1-4277-525 02
annette.rompel@univie.ac.at
www.bpc.univie.ac.at
Rückfragehinweis
Mag. Alexandra Frey
Pressebüro der Universität Wien
Forschung und Lehre
1010 Wien, Universitätsring 1
T +43-1-4277-175 33
M +43-664-602 77-175 33
alexandra.frey@univie.ac.at
Die Universität Wien ist eine der ältesten und größten Universitäten Europas: An 15 Fakultäten und vier Zentren arbeiten rund 9.700 MitarbeiterInnen, davon 6.900 WissenschafterInnen. Die Universität Wien ist damit auch die größte Forschungsinstitution Österreichs sowie die größte Bildungsstätte: An der Universität Wien sind derzeit rund 92.000 nationale und internationale Studierende inskribiert. Mit über 180 Studien verfügt sie über das vielfältigste Studienangebot des Landes. Die Universität Wien ist auch eine bedeutende Einrichtung für Weiterbildung in Österreich. 1365 gegründet, feiert die Alma Mater Rudolphina Vindobonensis im Jahr 2015 ihr 650-jähriges Gründungsjubiläum. www.univie.ac.at
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Ideen für die Zukunft
TU Berlin präsentiert sich vom 22. bis 26. April 2024 mit neun Projekten auf der Hannover Messe 2024. Die HANNOVER MESSE gilt als die Weltleitmesse der Industrie. Ihr diesjähriger Schwerpunkt…

Peptide auf interstellarem Eis
Dass einfache Peptide auf kosmischen Staubkörnern entstehen können, wurde vom Forschungsteam um Dr. Serge Krasnokutski vom Astrophysikalischen Labor des Max-Planck-Instituts für Astronomie an der Universität Jena bereits gezeigt. Bisher ging…

Wasserstoff-Produktion in der heimischen Garage
Forschungsteam der Frankfurt UAS entwickelt Prototyp für Privathaushalte: Förderzusage vom Land Hessen für 2. Projektphase. Wasserstoff als Energieträger der Zukunft ist nicht frei verfügbar, sondern muss aufwendig hergestellt werden. Das…





















